Clear Sky Science · sv
KDM3A katalyserar oxidering av acetyl-lysine till hydroxyacetyl-lysine på histon H3K9
Hur celler finjusterar gener med små kemiska strömbrytare
Varje cell i din kropp bär på samma DNA, ändå beter sig hjärt-, hjärn- och hudceller mycket olika. En orsak är att celler dekorerar sina DNA-förpackande proteiner, så kallade histoner, med små kemiska taggar som fungerar som strömbrytare för att slå gener på eller av. Denna artikel avslöjar en överraskande ny typ av strömbrytare på en viktig histonposition och visar att den styrs direkt av syre, vilket kopplar hur celler läser sina gener till hur de känner av luften de andas.
En ny vinkel på en välkänd histontagg
Histoner är spolar runt vilka DNA är lindat. Celler fäster kemiska grupper som acetyl- eller metylgrupper på specifika platser på histoner för att lossa eller snärta åt DNA, vilket påverkar vilka gener som är aktiva. En välkänd hotspot är lysin 9 på histon H3 (H3K9), där acetylering tenderar att främja genaktivitet medan vissa metylmärken förknippas med genavstängning. Enzymer kallade histonacetyltransferaser lägger till acetylgrupper, och deacetylaser tar bort dem; andra enzymer lägger till eller tar bort metylgrupper. Hittills trodde man att dessa förändringar var ”redox-neutrala” – att de inte uttryckligen berodde på syre. 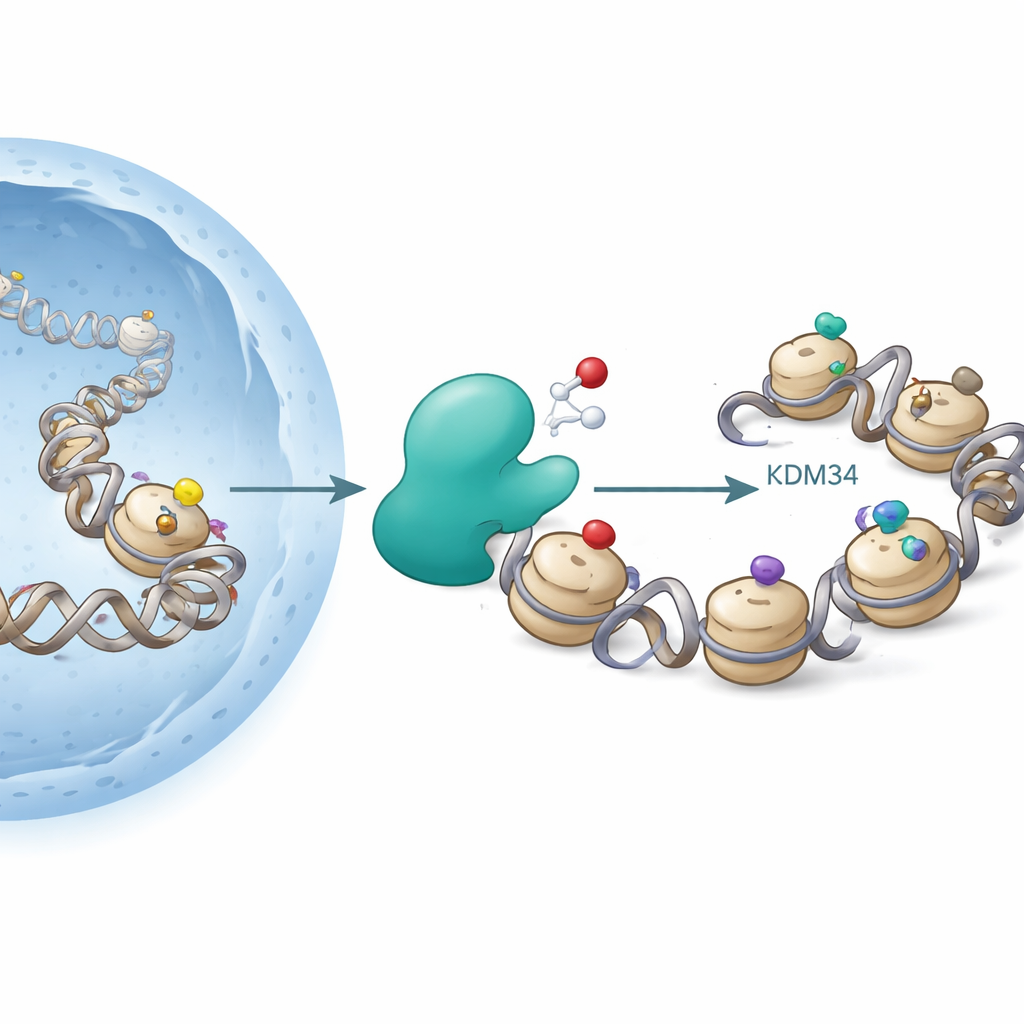
Att upptäcka ett syre-kopplat histonmärke
Författarna fokuserade på KDM3A, ett enzym redan känt för att ta bort metylgrupper från H3K9. KDM3A tillhör en familj av syreberoende enzymer som kräver järn och en liten kofaktor (2-oxoglutarat) för att fungera, liknande de enzymer som känner av låg syrehalt (hypoxi) i våra vävnader. När forskarna screenade olika modifierade histonfragment som möjliga KDM3A-mål bekräftade de att KDM3A effektivt raderade vissa metylmärken på H3K9. Överraskande nog fann de också att renat KDM3A kunde oxidera acetylgruppen på H3K9 och omvandla den till en ny form kallad hydroxyacetyl-lysine. Denna förändring motsvarar att lägga till ett syreatom till acetylgruppen, och ytterligare experiment visade att enzymet under vissa förhållanden kan oxidera ännu längre, vilket antyder en väg till mer exotisk kemi.
Bevisa att det nya märket finns i celler
Att hitta en ny kemisk produkt i ett provrör är bara första steget; teamet behövde också visa att hydroxyacetyl-lysine förekommer på histoner inne i levande celler. De skapade ett specifikt antikroppsverktyg som känner igen H3K9 med hydroxyacetylgruppen men inte den vanliga acetylformen. Med detta verktyg visade de att tillsats av renat KDM3A till isolerade histoner ökade signalen för det nya märket, medan kända metylmärken på H3K9 minskade, vilket var väntat utifrån KDM3A:s dubbla aktivitet. Överuttryck av KDM3A i humana celler gav liknande effekter: metylmärken sjönk och hydroxyacetyl-signalen ökade på bulk-histoner och på enskild cellnivå. Masspektrometri, en mycket känslig teknik för att väga molekyler, bekräftade oberoende att den precisa H3K9-peptiden som bär hydroxyacetyl-lysine finns i celler när KDM3A är aktiv.
Var det nya märket sitter i genomet
För att se var detta märke förekommer längs DNA utförde forskarna ChIP-seq, en genombred kartläggningsmetod. De fann att H3K9-hydroxyacetylering klustrar kring genstartplatser, särskilt vid gener som redan är högt uttryckta. Dess mönster följer nära klassiska ”aktiva” markörer såsom H3K9-acetylering och H3K4-trimetylering, vilket tyder på att den nya taggen också tillhör verktygslådan för aktiv kromatin. Behandling av celler med en histondeacetylashämmare, en typ av läkemedel som redan används i cancerterapi, ökade både standardacetylering och det nya hydroxyacetylmärket, sannolikt genom att öka substrattillgängligheten för KDM3A och bromsa borttagningen av dessa acylgrupper. 
Hur andra proteiner läser och bearbetar det nya märket
Studien testade också hur befintliga kromatin ”läsare” och ”raderare” reagerar på den nya taggen. En läsardomän från proteinet AF9, som normalt känner igen acetyl- och crotonyl-taggar, binder hydroxyacetyl-versionen med endast måttligt minskad affinitet, vilket antyder att kända läsare kan upptäcka denna modifiering. Två deacetylerande enzymer, SIRT1 och HDAC8, bearbetade hydroxyacetyl-lysine olika: SIRT1 var mycket mindre effektiv på att ta bort den nya taggen än den vanliga acetylgruppen, medan HDAC8 visade liten preferens. Dessa skillnader tyder på att hydroxyacetylering subtilt kan ändra hur länge ett märke består och vilka enzymer som engageras, och därigenom finjustera kromatinlandskapet.
Varför denna syreberoende strömbrytare är viktig
Sammanfattningsvis avslöjar arbetet H3K9-hydroxyacetylering som ett tidigare okänt histonmärke som produceras av KDM3A, och troligen i vissa sammanhang av dess nära släkting KDM3B. Eftersom KDM3A själv aktiveras av låg syrehalt via hypoxi-inducerbara faktorer skapar detta en direkt kemisk koppling mellan syrenivåer och histonacetyleringstillstånd. Enkelt uttryckt kan enzymet både ta bort repressiva metyltaggar och omvandla aktiverande acetyltaggar till en något annorlunda syreinnehållande form på samma histonposition, vilket potentiellt omformar genprogram under stress, utveckling eller cancer. Upptäckten vidgar vår syn på vad ”demetylas”-enzymer kan göra och öppnar dörren för att undersöka liknande hydroxyacetylmärken på andra proteiner, samt deras roller i hälsa och sjukdom.
Citering: Belle, R., Bukowski, JP., Schiller, R. et al. KDM3A catalyses the oxidation of acetyl-lysine to hydroxyacetyl-lysine on histone H3K9. Nat. Chem. 18, 823–834 (2026). https://doi.org/10.1038/s41557-026-02112-x
Nyckelord: histonmodifiering, epigenetik, syresensing, KDM3A-enzym, genreglering