Clear Sky Science · ar
KDM3A يحفز أكسدة أستيل-اللايسين إلى هيدروكسيأستيل-اللايسين على الهيستون H3K9
كيف تعدل الخلايا الجينات بمفاتيح كيميائية صغيرة
تحمل كل خلية في جسمك نفس الحمض النووي، ومع ذلك تعمل خلايا القلب والدماغ والجلد بشكل مختلف تماماً. أحد الأسباب هو أن الخلايا تزين بروتينات تغليف الحمض النووي، المسماة الهيستونات، بعلامات كيميائية صغيرة تعمل كمفاتيح لتشغيل أو إيقاف الجينات. تكشف هذه الورقة عن نوع مفاجئ جديد من المفاتيح في موقع هيستون رئيسي وتظهر أنه يتحكم به بشكل مباشر الأكسجين، مما يربط بين كيفية قراءة الخلايا لجيناتها وكيفية استشعارها للهواء الذي تتنفسه.
لمسة جديدة على علامة هيستون معروفة
الهيستونات تشبه بكرات يلتف حولها الحمض النووي. تضع الخلايا مجموعات كيميائية مثل مجموعة الأستيل أو الميثيل على مواقع محددة في الهيستونات لتفكيك أو تشديد لف الحمض النووي، مؤثرةً على أي الجينات تكون نشطة. بقعة شهيرة هي اللايسين 9 على الهيستون H3 (H3K9)، حيث تميل الأستلة إلى تعزيز نشاط الجين، بينما ترتبط بعض علامات الميثلة بكتم الجين. تضيف إنزيمات تُسمى ناقلات الأستيل مجموعات الأستيل، وتُزيلها ناقلات الأستيلاز؛ وإنزيمات أخرى تضيف أو تمحو علامات الميثيل. حتى الآن، كان يُعتقد أن هذه التغييرات «محايدة من الناحية التأكسدية» — أي أنها لا تعتمد صراحةً على الأكسجين. 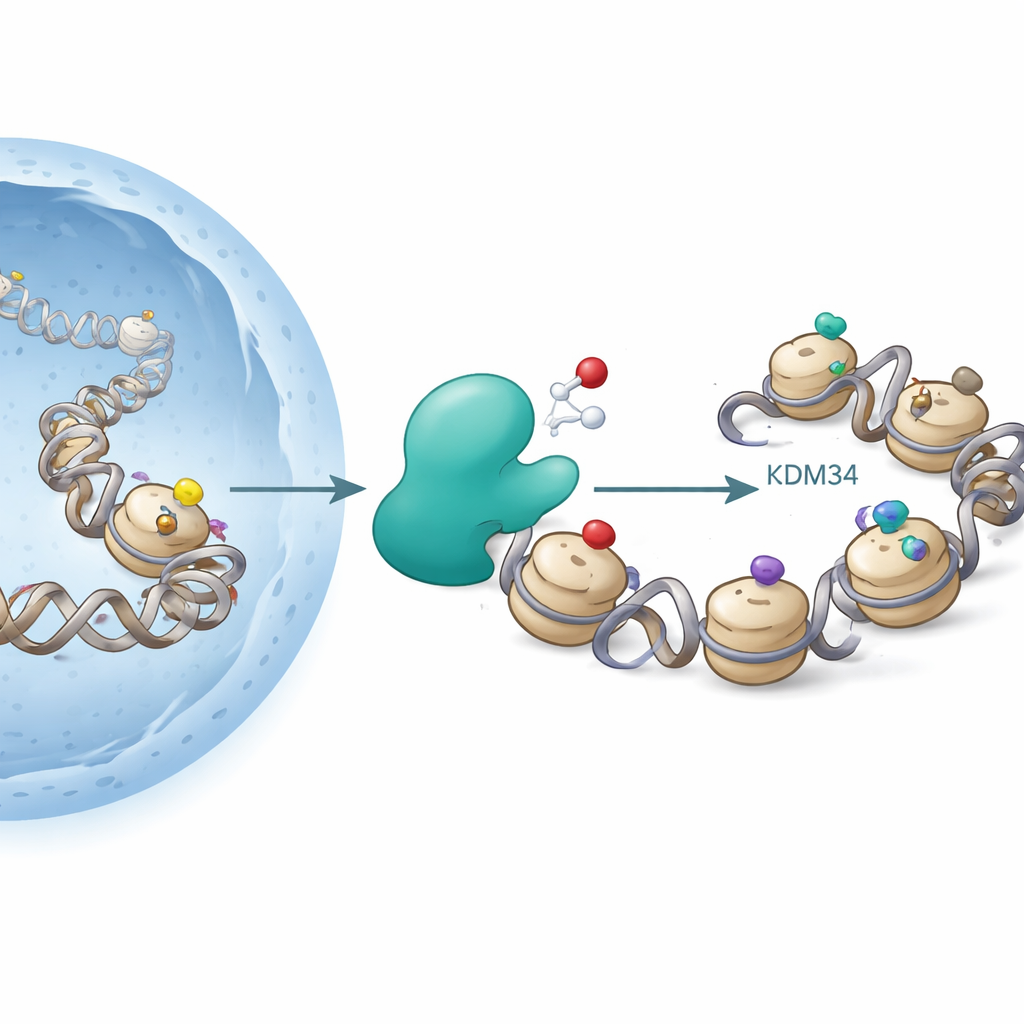
اكتشاف علامة هيستون مرتبطة بالأكسجين
ركز المؤلفون على KDM3A، إنزيم معروف بالفعل بإزالة مجموعات الميثيل من H3K9. ينتمي KDM3A إلى عائلة من الإنزيمات المعتمدة على الأكسجين والتي تحتاج إلى الحديد وجزيء مساعد صغير (2-أوكسوغلوتارات) للعمل، على غرار الإنزيمات التي تستشعر نقص الأكسجين (نقص التأكسج) في أنسجتنا. عندما فحص الباحثون شظايا هيستون مُعدلة مختلفة كأهداف محتملة لـKDM3A، أكدوا أن KDM3A يزيل بكفاءة بعض علامات الميثيل على H3K9. وبشكل غير متوقع، وجدوا أيضاً أن KDM3A المنقى يمكنه أكسدة مجموعة الأستيل على H3K9، محولاً إياها إلى شكل جديد يسمى هيدروكسيأستيل-اللايسين. تتوافق هذه التغيير مع إضافة ذرة أكسجين إلى مجموعة الأستيل، وأظهرت تجارب إضافية أنه في ظل ظروف معينة يمكن للإنزيم أن يؤكسد أكثر من ذلك، مما يُشير إلى مسار نحو كيميائيات أكثر غرابة.
إثبات وجود العلامة الجديدة داخل الخلايا
إيجاد منتج كيميائي جديد في إناء اختبار هو خطوة أولى فقط؛ احتاج الفريق أيضاً إلى إظهار أن هيدروكسيأستيل-اللايسين يظهر على الهيستونات داخل الخلايا الحية. أنتجوا جسم مضاد مخصص يتعرف على H3K9 الحامل لمجموعة الهيدروكسيأستيل لكنه لا يتعرف على الشكل الأستيل القياسي. باستخدام هذه الأداة، أظهروا أن إضافة KDM3A المنقى إلى هيستونات معزولة زادت الإشارة للعلامة الجديدة، في حين انخفضت علامات الميثيل المعروفة على H3K9، كما كان متوقعاً من نشاط KDM3A المزدوج. أدى الإفراط في التعبير عن KDM3A في خلايا بشرية إلى تأثيرات مماثلة: انخفضت علامات الميثيل وارتفعت إشارة الهيدروكسيأستلة على الهيستونات العامة وعلى مستوى الخلية الوحيدة. وأكدت القياسات الطيفية الكتلية، وهي تقنية حساسة للغاية لوزن الجزيئات، بشكل مستقل أن الببتيد الدقيق لـH3K9 الحامل للهيدروكسيأستيل-اللايسين موجود في الخلايا عندما يكون KDM3A نشطاً.
مكان وجود العلامة الجديدة على الجينوم
لرؤية أين تظهر هذه العلامة على طول الحمض النووي، أجرى الباحثون تجارب ChIP-seq، وهي طريقة رسم خرائط على مستوى الجينوم. وجدوا أن هيدروأستلة H3K9 تتجمع حول مواقع بدء الجينات، خاصة عند الجينات التي تكون معبَّرة بنشاط بالفعل. يتتبع نمطها عن كثب علامات «نشطة» كلاسيكية مثل أستلة H3K9 وثلاثية ميثلة H3K4، مما يوحي بأن الوسم الجديد ينتمي أيضاً إلى مجموعة أدوات الكروماتين النشط. أدى علاج الخلايا بمثبط ناقلات إزالة الأستيل من الهيستون، وهو نوع من الأدوية يُستخدم حالياً في علاج السرطان، إلى زيادة كل من الأستلة القياسية والعلامة الجديدة الهيدروأستيلية، على الأرجح عن طريق زيادة توفر الركيزة لـKDM3A وإبطاء إزالة هذه مجموعات الأسيلي.
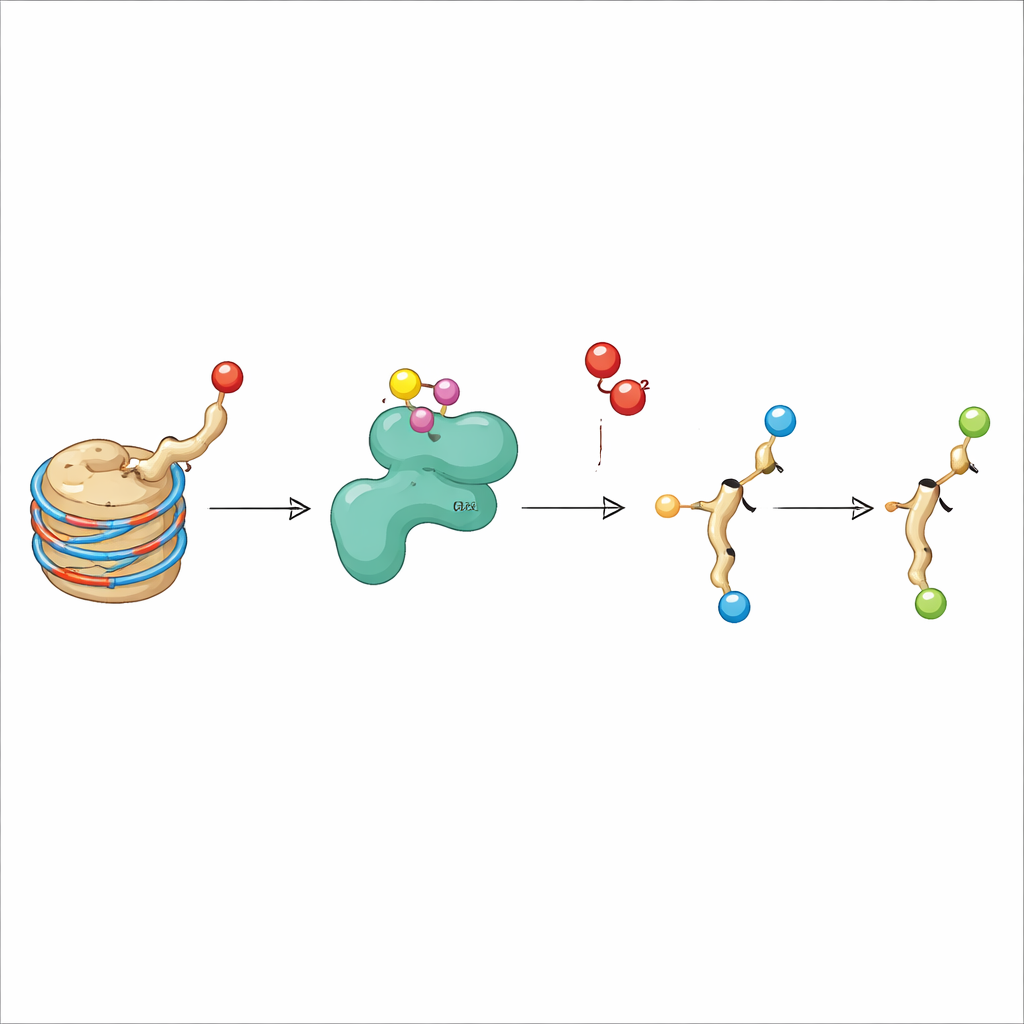
كيف تقرأ وتُعالج البروتينات الأخرى الوسم الجديد
اختبرت الدراسة أيضاً كيف تستجيب بروتينات «القراءة» و«المحو» الموجودة للوسم الجديد. مجال قارئ من بروتين AF9، الذي يتعرف عادة على علامات الأستيل والكرونويل، ارتبط بشكل النسخة الهيدروأستيلية مع انخفاض طفيف في الألفة، ما يوحي بأن القارئين المعروفين يمكنهم استشعار هذا التعديل. عالجان مزيلان للأستيلة، SIRT1 وHDAC8، عالجا هيدروأستيل-اللايسين بطرق مختلفة: كانت SIRT1 أقل كفاءة بكثير في إزالة الوسم الجديد مقارنة بالمجموعة الأستيلية القياسية، بينما لم تُظهر HDAC8 تفضيلاً واضحاً. تشير هذه الاختلافات إلى أن الهيدروأستلة يمكن أن تغير قليلاً طول بقاء العلامة وأي الإنزيمات تتعامل معها، مضبوطةً بذلك مشهد الكروماتين بدقة.
لماذا تهم هذه المفاتيح المعتمدة على الأكسجين
بشكل عام، تكشف هذه الدراسة عن هيدروأستلة H3K9 كعلامة هيستون لم تكن معروفة من قبل وينتجها KDM3A، وعلى الأرجح في بعض السياقات إنزيمه الشقيق KDM3B. بما أن KDM3A نفسه يُفعل استجابة لانخفاض الأكسجين عبر مسار العامل القابل للتكاثر في نقص الأكسجة، فإن ذلك يخلق رابطاً كيميائياً مباشراً بين مستويات الأكسجين وحالات أستلة الهيستون. ببساطة، يمكن للإنزيم أن يزيل علامات الميثيل الكابحة ويحوّل في الوقت نفسه علامات الأستيل المنشِّطة إلى شكل يحتوي على الأكسجين في نفس موقع الهيستون، مما قد يعيد تشكيل برامج الجينات أثناء الإجهاد أو التطور أو السرطان. يوسّع الاكتشاف رؤيتنا لما يمكن أن تفعله إنزيمات «مزيلات الميثيل» ويفتح الباب لاستكشاف علامات هيدروأستيل المماثلة على بروتينات أخرى، فضلاً عن أدوارها في الصحة والمرض.
الاستشهاد: Belle, R., Bukowski, JP., Schiller, R. et al. KDM3A catalyses the oxidation of acetyl-lysine to hydroxyacetyl-lysine on histone H3K9. Nat. Chem. 18, 823–834 (2026). https://doi.org/10.1038/s41557-026-02112-x
الكلمات المفتاحية: تعديل الهيستون, علم فوق الجينات, استشعار الأكسجين, إنزيم KDM3A, تنظيم الجينات