Clear Sky Science · tr
Hücre dışı matris kaynaklı hasta sınıflandırması ve ağ modellemesi, muhtemel klinik sonuçları olan farklı moleküler dereceler ortaya koyuyor
Neden tümörün çevresi önemlidir
Kanseri düşünürken genellikle kontrolden çıkan hücreleri hayal ederiz. Ancak bu hücreler, hücre dışı matris adı verilen, proteinler ve şekerlerden oluşan karmaşık bir komşulukta yaşar. Bu iskelet pasif olmaktan çok uzaktır. Sertleşebilir, kalınlaşabilir ve tümörlerin büyümesine veya tedaviden kaçınmasına yardımcı olan sinyaller gönderebilir. Bu çalışmada araştırmacılar, akciğer tümörlerindeki bu iskelenin bileşiminin hastaları anlamlı gruplara ayırmak ve tedavi seçimlerine rehberlik etmek için kullanılıp kullanılamayacağını sordular.
Tümörleri yapısal “iskeleleme”lerine göre ayırmak
Ekip, yaygın bir akciğer kanseri türü olan akciğer adenokarsinomuna odaklandı ve tümörleri DNA, RNA ve protein düzeyinde derinlemesine profillendirilmiş 101 hastayı analiz etti. Matrisi oluşturan ve düzenleyen genlerden oluşturulmuş kürate bir liste kullanarak her hasta için bir “ECM barkodu” oluşturdular. Bu barkod, her tümörün matriksinin o hastanın yakınındaki normal akciğer dokusundan ne kadar farklı olduğunu yakaladı. Bu barkodlara göre hastaları gruplayınca, neredeyse normal görünümlü matrislerden yoğun, karmaşık bir ağla sarılmış tümörlere kadar uzanan dört ayrı “ECM derecesi” ortaya çıktı.
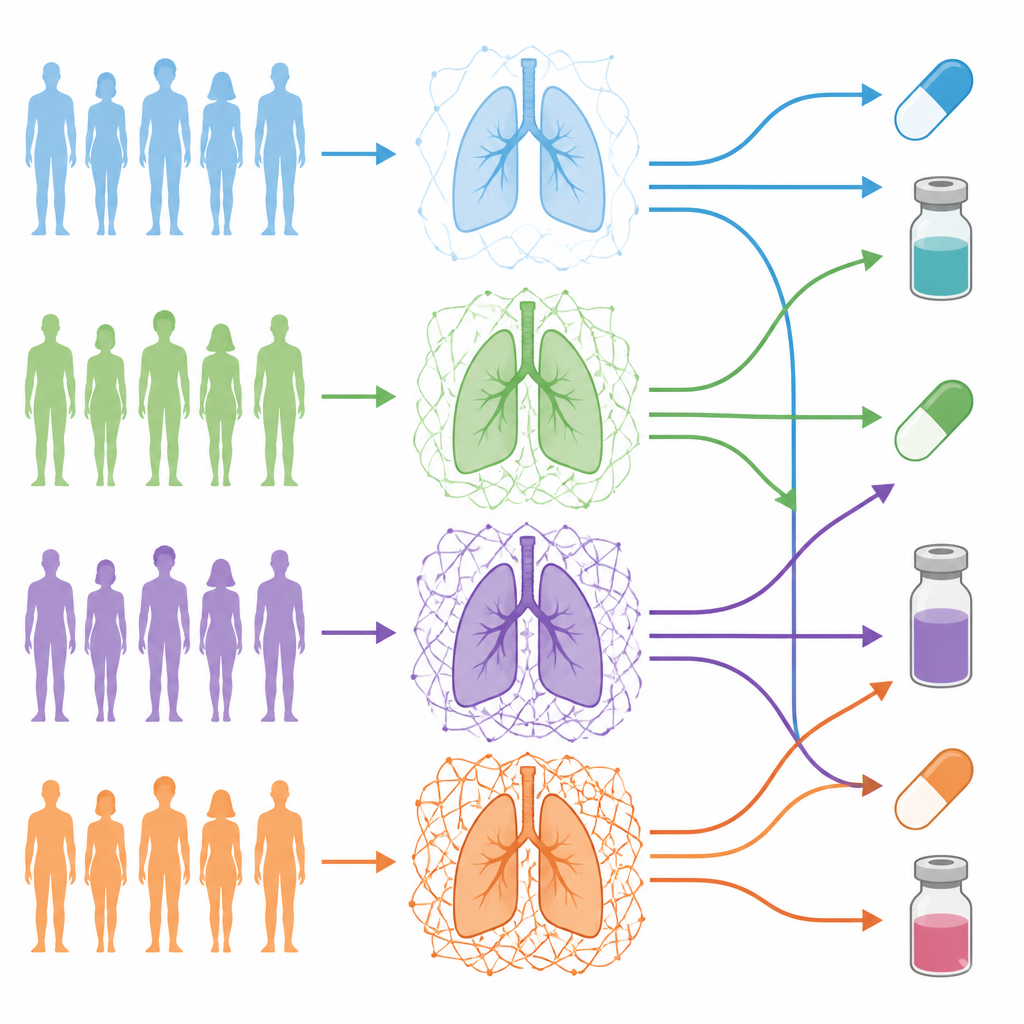
Yüksek ve düşük dereceler tümör hakkında ne söylüyor
En yüksek ECM derecesine sahip tümörler, kanserle ilişkili fibroblastlar gibi stromal hücrelerle doluydu ve kendi içlerindeki kanser hücresi oranları daha düşüktü; bu desen daha gelişmiş tümör mikroçevreleriyle ilişkilidir. Bu ECM zengini tümörler, epitelyalden mezenkimal geçiş, invazivlik, kanser kök hücre benzeri özellikler ve damar büyümesi ile ilişkili daha güçlü sinyaller gösterdi. En yüksek ECM derecesindeki hastalar, seyrek matrise sahip tümörlü hastalarla karşılaştırıldığında daha agresif klinik özelliklere, daha fazla tümör mutasyonuna ve daha yüksek kısa dönem ölüm ya da nüks riskine eğilimliydi.
Matriks ile hücre davranışı arasındaki gizli bağlantılar
Dış matriksin hücre içi davranışla nasıl bağlantılı olduğunu açığa çıkarmak için araştırmacılar, her hasta için değişmiş matriks proteinlerini etkilediği sinyal proteinleri ve transkripsiyon faktörlerine bağlayan ağ modelleri kurdu. Bu ağları birleştirmek, daha yüksek ECM derecelerinin hücre hareketi, hayatta kalma ve mekanik strese uyum sağlayan yolların daha güçlü aktivitesiyle ilişkili olduğunu gösterdi. Hücrelerin bağlantılarını gevşetmelerini, göç etmelerini ve invaze olmalarını teşvik eden sinyaller daha aktifken, normalde invazyonu baskılayan koruyucu faktörler ECM zengini tümörlerde zayıftı. Çalışma ayrıca KRAS ve EGFR gibi bilinen bazı kanser mutasyonlarının farklı ECM derecelerinde eğilim gösterdiğini buldu; bu da matris ortamı ile genetik değişikliklerin birbirini güçlendirebileceğini düşündürüyor.
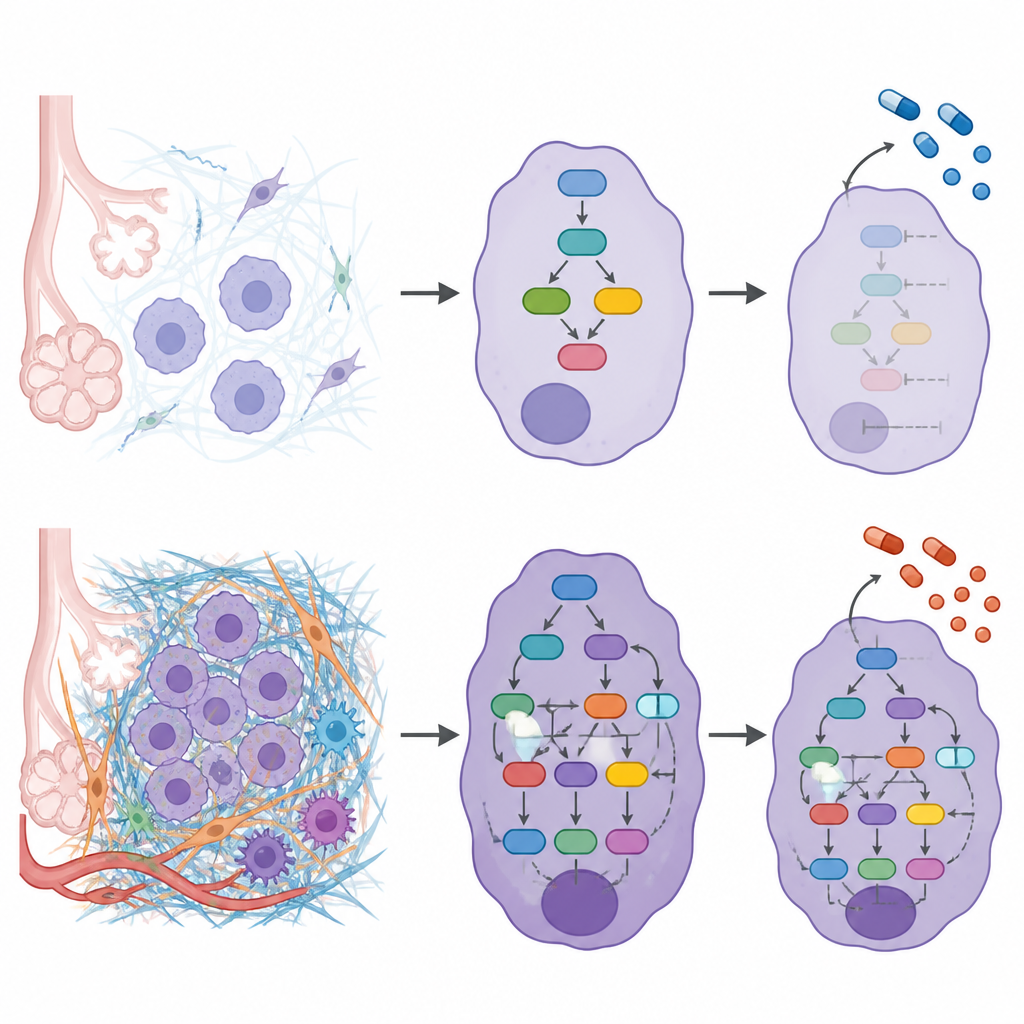
Matriksi tedavi seçimleriyle ilişkilendirmek
Matriksin ilaçların tümör hücrelerine ulaşma ve etki biçimini şekillendirebileceği düşünüldüğünde, ekip bir sonraki adım olarak farklı ECM derecelerinin mevcut kanser ilaçlarına farklı yanıt verip vermeyeceğini sordu. Ağ haritalarını kullanarak, her ilacın hedeflerinin her derecedeki matris kaynaklı sinyal merkezlerine ne kadar “yakın” olduğunu ölçtüler. Bu, belirli ECM ortamlarında en iyi çalışması öngörülen ilaçları ve dereceler arasında benzer etki göstermesi muhtemel ilaçları ortaya koydu. DNA onarım enzimlerini bloke eden olaparib adlı ilaç, özellikle düşük ECM dereceleriyle güçlü bir bağlantı gösterirken; EGFR hedefleyen erlotinib, ECM derecesinden bağımsız olarak geniş ölçüde etkili görünüyordu.
Tahminleri laboratuvarda test etmek
Araştırmacılar ardından, KRAS veya EGFR mutasyonları taşıyan akciğer kanseri hücre hatlarını kullanarak laboratuvarda düşük ve yüksek ECM ortamlarının basitleştirilmiş versiyonlarını yeniden oluşturdular. Hücreleri düşük dereceli bir ortamı taklit etmek için sağlıklı akciğer kaynaklı matriks üzerinde, daha zengin bir matriksi taklit etmek içinse tümör benzeri bir bazal membran üzerinde yetiştirdiler. Ağ tahminleriyle uyumlu olarak, olaparib EGFR-mutant hücrelere sağlıklı-benzeri matriks üzerinde tümör-benzeri matrikse göre daha güçlü etki gösterirken; KRAS-mutant hücreler üzerindeki etkisi matrikse çok bağlı değildi. Buna karşılık erlotinib, ağ analizinden çıkan ECM-bağımsız profiline uygun olarak her iki matris koşulunda da benzer derece hücre canlılığını azalttı.
Bu hastalar için ne anlama geliyor
Bu çalışma, tümörün destekleyici iskelesinin yalnızca bir arka plan olmadığını, ölçülebilir, sınıflandırılabilir ve tümörlerin büyüme ve ilaç yanıtlarıyla ilişkilendirilebilecek önemli bir özellik olduğunu öne sürüyor. Akciğer kanserlerini ECM derecelerine sınıflandırıp matriksi hücre davranışına bağlayan sinyal ağlarını haritalayarak, klinisyenler eninde sonunda kanserin genetik yapısına ve fiziksel çevresine uygun tedavileri seçebilecek hale gelebilir. Bu yaklaşımın rutin bakıma rehberlik etmeden önce daha fazla doğrulamaya ihtiyacı olsa da, tümör çevresinin hangi tedavilerin en olası şekilde işe yarayacağını belirlemede rol oynayacağı bir geleceğe işaret ediyor.
Atıf: Dansık, A., Sarıca, S., Öztürk, E. et al. Extracellular matrix-driven patient stratification and network modeling reveal distinct molecular grades with potential clinical implications. npj Syst Biol Appl 12, 66 (2026). https://doi.org/10.1038/s41540-026-00697-0
Anahtar kelimeler: hücre dışı matris, akciğer adenokarsinomu, tümör mikroçevresi, kanser ağları, ilaç yanıtı