Clear Sky Science · fr
La stratification des patients basée sur la matrice extracellulaire et la modélisation en réseau révèlent des degrés moléculaires distincts avec des implications cliniques potentielles
Pourquoi l’environnement autour de la tumeur compte
Quand on pense au cancer, on imagine souvent des cellules rebelles qui prolifèrent hors de contrôle. Mais ces cellules vivent dans un voisinage complexe composé de protéines et de sucres qui forment une trame de soutien appelée matrice extracellulaire. Cette trame est loin d’être passive. Elle peut se durcir, s’épaissir et émettre des signaux qui favorisent la croissance tumorale ou la résistance au traitement. Dans cette étude, les chercheurs se sont demandé si la composition de cette trame dans les tumeurs pulmonaires pouvait servir à regrouper les patients de façon significative et à orienter le choix des thérapies.
Classer les tumeurs selon leur « échafaudage » structurel
L’équipe s’est concentrée sur l’adénocarcinome pulmonaire, un type fréquent de cancer du poumon, et a analysé 101 patients dont les tumeurs avaient été profilées en profondeur aux niveaux de l’ADN, de l’ARN et des protéines. Ils ont utilisé une liste sélectionnée de gènes impliqués dans la construction et la régulation de la matrice pour créer un « code-barres ECM » pour chaque patient. Ce code-barres capturait dans quelle mesure la matrice de chaque tumeur différait du tissu pulmonaire normal adjacent du patient. En regroupant les patients à partir de ces codes-barres, quatre « degrés ECM » distincts sont apparus, allant d’une matrice quasi normale à des tumeurs enveloppées dans une trame dense et complexe.
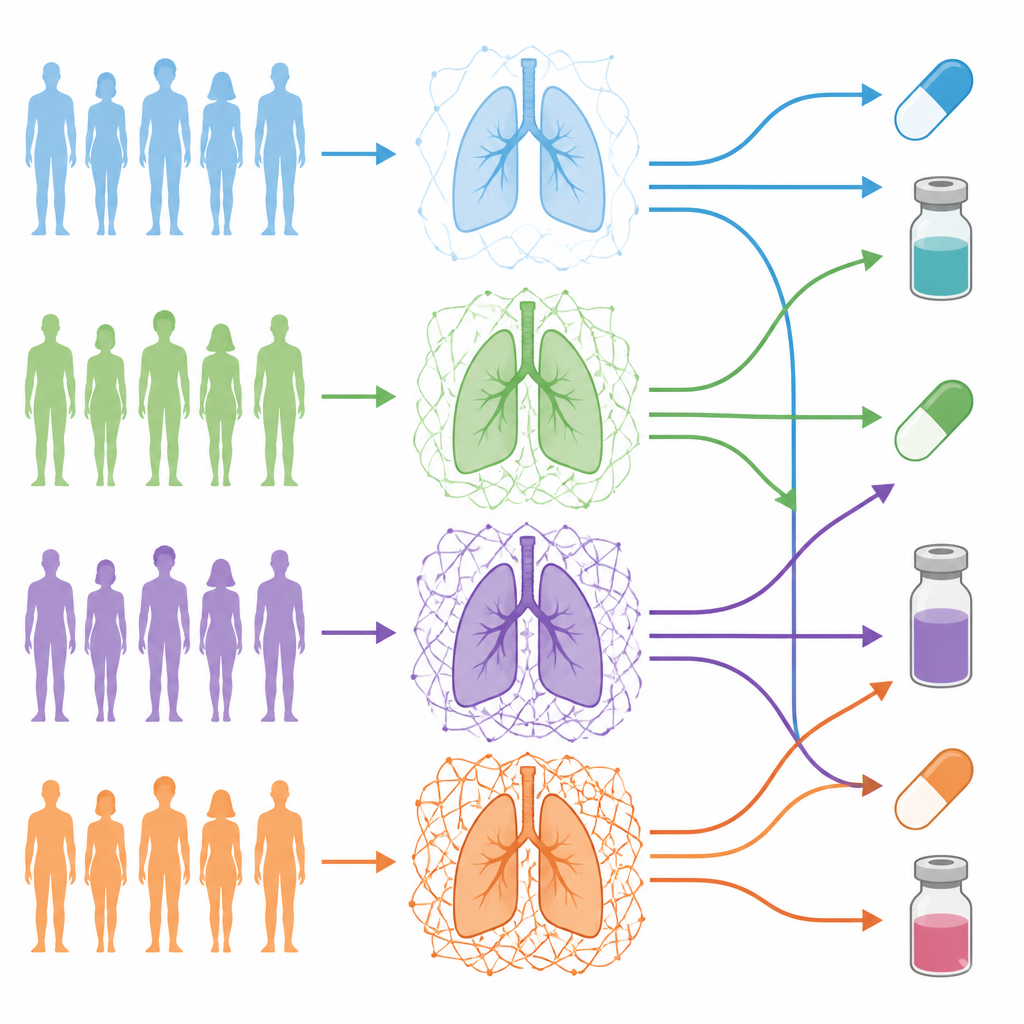
Ce que révèlent les degrés élevés et faibles
Les tumeurs présentant les degrés ECM les plus élevés étaient fortement peuplées de cellules stromales telles que des fibroblastes associés au cancer, et comportaient une fraction moindre de cellules cancéreuses elles-mêmes, un profil associé à des microenvironnements tumoraux plus avancés. Ces tumeurs riches en ECM montraient des signaux plus puissants liés à la transition épithélio-mésenchymateuse, à l’invasivité, aux cellules de type « stem-like » et à l’angiogenèse. Les patients présentant le degré ECM le plus élevé avaient tendance à manifester des caractéristiques cliniques plus agressives, davantage de mutations tumorales et un risque à court terme plus élevé de décès ou de récidive, comparés aux patients dont les tumeurs avaient une matrice éparse.
Des connexions cachées entre la matrice et le comportement cellulaire
Pour mettre au jour comment la matrice externe se relie au comportement interne des cellules, les chercheurs ont construit des modèles en réseau pour chaque patient reliant les protéines de matrice altérées aux protéines de signalisation et facteurs de transcription qu’elles influencent. La combinaison de ces réseaux a montré que des degrés ECM plus élevés s’associaient à une activité renforcée dans des voies régulant le mouvement cellulaire, la survie et l’adaptation au stress mécanique. Les signaux favorisant le détachement des cellules, la migration et l’invasion étaient plus actifs, tandis que des facteurs protecteurs qui suppriment normalement l’invasion étaient affaiblis dans les tumeurs riches en ECM. L’étude a également constaté que certaines mutations cancéreuses bien connues, comme celles de KRAS et EGFR, avaient tendance à apparaître dans des degrés ECM différents, ce qui suggère que l’environnement matriciel et les altérations génétiques peuvent se renforcer mutuellement.
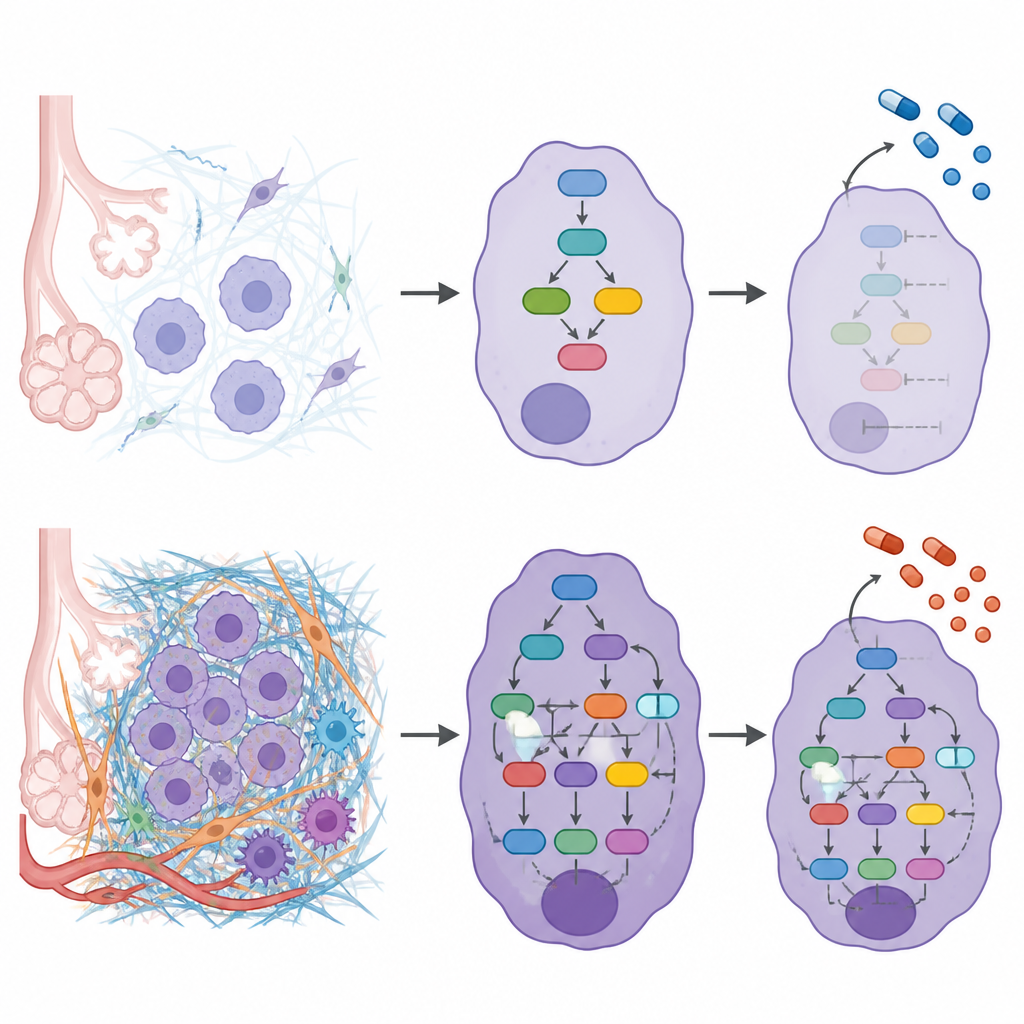
Relier la matrice aux choix thérapeutiques
Comme la matrice peut influencer la façon dont les médicaments atteignent et affectent les cellules tumorales, l’équipe s’est ensuite demandée si les différents degrés ECM pourraient répondre différemment aux traitements anticancéreux existants. À l’aide de leurs cartes en réseau, ils ont mesuré la « proximité » des cibles de chaque médicament par rapport aux nœuds de signalisation pilotés par la matrice dans chaque degré. Cela a révélé des médicaments prédits comme étant plus efficaces dans des contextes ECM spécifiques et d’autres susceptibles d’agir de manière similaire à travers les degrés. Un médicament qui bloque des enzymes de réparation de l’ADN, l’olaparib, s’est avéré particulièrement lié aux degrés ECM faibles, tandis qu’un inhibiteur ciblant EGFR, l’erlotinib, semblait efficace de manière large, quel que soit le degré ECM.
Mettre les prédictions à l’épreuve en laboratoire
Les chercheurs ont ensuite recréé des versions simplifiées d’environnements ECM faibles et élevés en laboratoire en utilisant des lignées cellulaires de cancer du poumon porteuses de mutations KRAS ou EGFR. Ils ont cultivé les cellules sur une matrice d’origine pulmonaire saine pour mimer un environnement de bas degré et sur une membrane basale de type tumoral pour mimer une matrice plus riche. Conforme aux prédictions des réseaux, l’olaparib était plus efficace contre les cellules mutées pour EGFR sur la matrice de type saine que sur la matrice de type tumoral, tandis que son effet sur les cellules mutées pour KRAS dépendait peu de la matrice. En revanche, l’erlotinib réduisait la viabilité cellulaire de manière similaire dans les deux conditions matricielles, correspondant à son profil peu sensible à l’ECM issu de l’analyse en réseau.
Ce que cela signifie pour les patients
Ce travail suggère que l’échafaudage de soutien tumoral n’est pas qu’un décor, mais une caractéristique clé qui peut être mesurée, classée et reliée à la façon dont les tumeurs croissent et répondent aux médicaments. En classant les cancers du poumon selon des degrés ECM et en cartographiant les réseaux de signalisation qui connectent la matrice au comportement cellulaire, les cliniciens pourraient à terme sélectionner des thérapies adaptées à la fois au profil génétique de la tumeur et à son environnement physique. Bien que des validations supplémentaires soient nécessaires avant que cette approche puisse guider les soins de routine, elle ouvre la voie à un futur où la structure entourant la tumeur participe au choix des traitements les plus susceptibles d’être efficaces.
Citation: Dansık, A., Sarıca, S., Öztürk, E. et al. Extracellular matrix-driven patient stratification and network modeling reveal distinct molecular grades with potential clinical implications. npj Syst Biol Appl 12, 66 (2026). https://doi.org/10.1038/s41540-026-00697-0
Mots-clés: matrice extracellulaire, adénocarcinome pulmonaire, microenvironnement tumoral, réseaux du cancer, réponse aux médicaments