Clear Sky Science · pl
Stratyfikacja pacjentów i modelowanie sieci napędzane przez macierz zewnątrzkomórkową ujawniają odrębne stopnie molekularne o potencjalnych implikacjach klinicznych
Dlaczego otoczenie guza ma znaczenie
Kiedy myślimy o raku, często wyobrażamy sobie zbuntowane komórki, które rosną bez kontroli. Jednak te komórki żyją w złożonym sąsiedztwie zbudowanym z białek i cukrów tworzących podporową siatkę zwaną macierzą zewnątrzkomórkową. Ta siatka jest daleka od bierności. Może się usztywniać, zgrubieć i przekazywać sygnały, które pomagają guzom rosnąć lub opierać się leczeniu. W tym badaniu naukowcy zastanawiali się, czy skład tej siatki w guzach płuca można wykorzystać do podziału pacjentów na sensowne grupy i do ukierunkowania wyboru terapii.
Sortowanie guzów według ich strukturalnego „rusztowania”
Zespół skupił się na gruczolakoraku płuca, powszechnym typie raka płuca, i przeanalizował próbki od 101 pacjentów, których guzy zostały dogłębnie zprofilowane na poziomie DNA, RNA i białek. Wykorzystali skuratorowy wykaz genów budujących i regulujących macierz, aby stworzyć dla każdego pacjenta „kod kreskowy ECM”. Ten kod odzwierciedlał, jak bardzo macierz każdego guza różniła się od przylegającej, pozornie zdrowej tkanki płucnej danego pacjenta. Grupując pacjentów według tych kodów, wyłoniły się cztery odrębne „stopnie ECM”, od macierzy niemal przypominającej normalną po guzy owinięte gęstą, złożoną siecią.
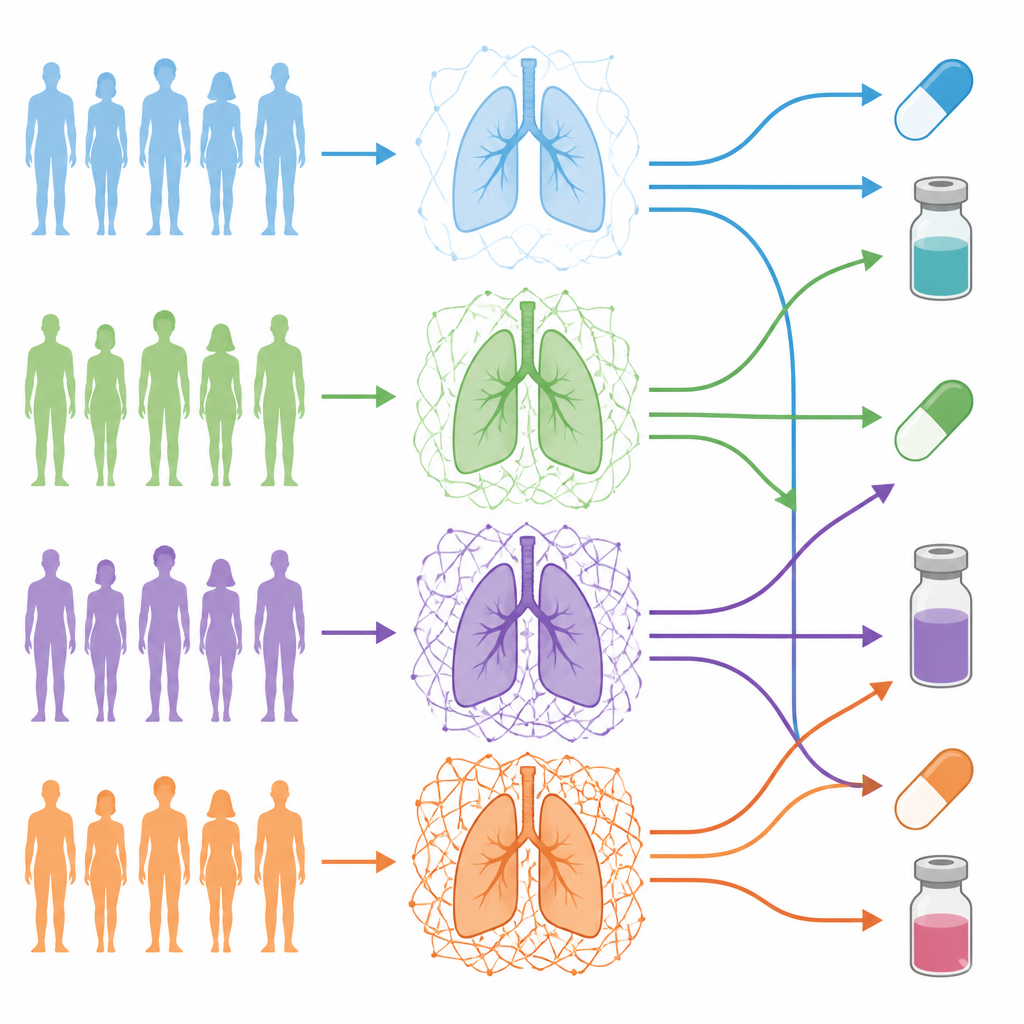
Co ujawniają wysokie i niskie stopnie
Guzy o najwyższych stopniach ECM były wypełnione komórkami zrębu, takimi jak fibroblasty związane z nowotworem, i miały niższy udział samych komórek nowotworowych — wzorzec związany z bardziej zaawansowanym mikrośrodowiskiem guza. Te bogate w ECM guzy wykazywały silniejsze sygnały związane z przejściem nabłonkowo-mezenchymalnym, inwazyjnością, komórkami o cechach przypominających komórki macierzyste raka oraz wzrostem naczyń krwionośnych. Pacjenci z guzami w najwyższym stopniu ECM mieli tendencję do wykazywania bardziej agresywnych cech klinicznych, większej liczby mutacji w guzie oraz wyższego krótkoterminowego ryzyka zgonu lub nawrotu choroby w porównaniu z pacjentami, których guzy miały rzadką macierz.
Ukryte połączenia między macierzą a zachowaniem komórek
Aby odkryć, jak zewnętrzna macierz łączy się z wewnętrznym zachowaniem komórek, badacze zbudowali modele sieciowe dla każdego pacjenta, łącząc zmienione białka macierzy z białkami sygnalizacyjnymi i czynnikami transkrypcyjnymi, które one wpływają. Połączenie tych sieci wykazało, że wyższe stopnie ECM wiązały się z silniejszą aktywnością w szlakach regulujących ruch komórek, przeżycie i adaptację do naprężeń mechanicznych. Sygnały zachęcające komórki do rozluźniania przyczepów, migracji i inwazji były bardziej aktywne, podczas gdy czynniki ochronne, które normalnie tłumią inwazję, były słabsze w guzach bogatych w ECM. Badanie wykazało również, że niektóre dobrze znane mutacje nowotworowe, takie jak w KRAS i EGFR, miały tendencję do występowania w różnych stopniach ECM, co sugeruje, że środowisko macierzy i zmiany genetyczne mogą wzajemnie się wzmacniać.
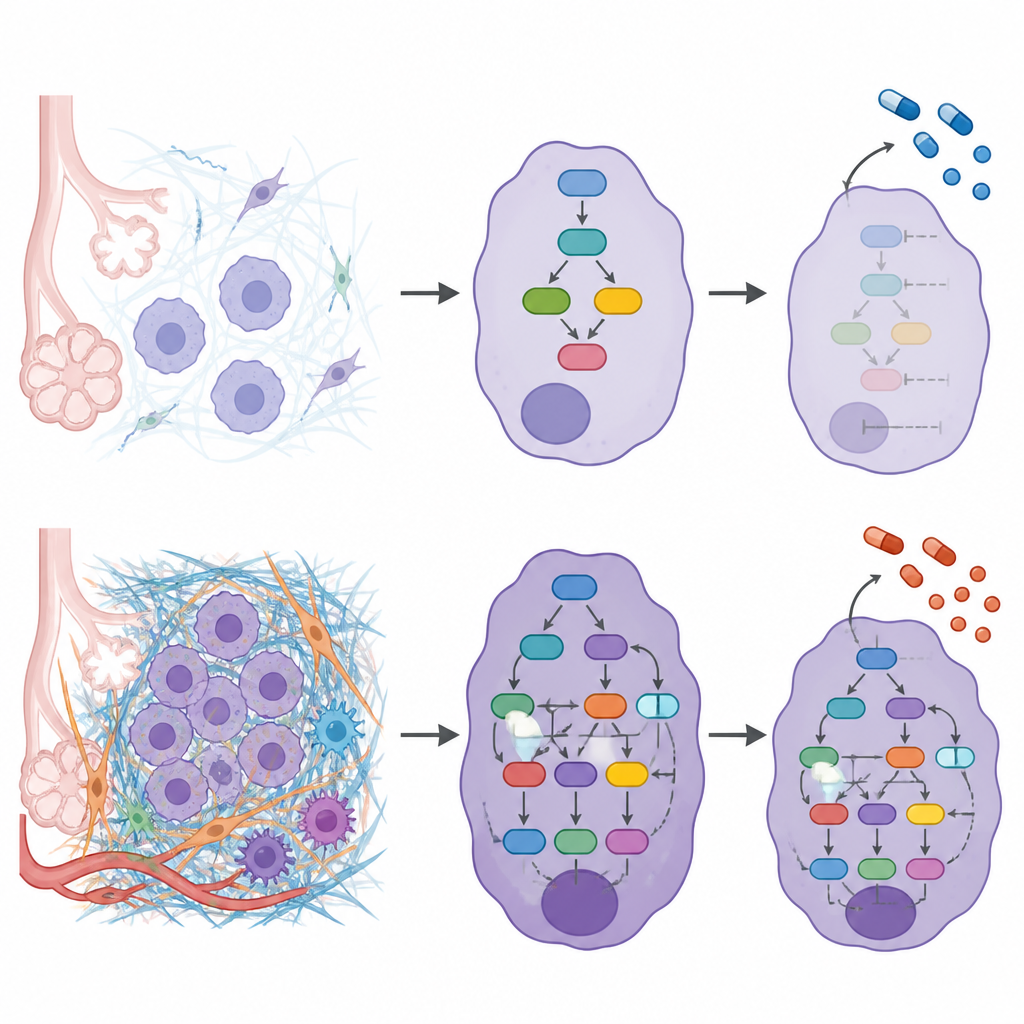
Powiązanie macierzy z wyborem terapii
Ponieważ macierz może kształtować, jak leki docierają do komórek guza i jak na nie wpływają, zespół zapytał następnie, czy różne stopnie ECM mogą inaczej reagować na istniejące leki przeciwnowotworowe. Korzystając z map sieciowych, zmierzyli, jak „bliskie” są cele każdego leku wobec węzłów sygnalizacyjnych napędzanych przez macierz w każdym stopniu. To ujawniło leki przewidywane jako najbardziej skuteczne w określonych ustawieniach ECM oraz inne prawdopodobnie działające podobnie we wszystkich stopniach. Lek blokujący enzymy naprawy DNA, olaparib, okazał się szczególnie powiązany z niskimi stopniami ECM, podczas gdy lek celujący EGFR, erlotynib, wyglądał na skuteczny szeroko, niezależnie od stopnia ECM.
Próba przewidywań w laboratorium
Naukowcy następnie odtworzyli uproszczone wersje środowisk o niskim i wysokim ECM w laboratorium, używając linii komórkowych raka płuca niosących mutacje KRAS lub EGFR. Hodowali komórki na macierzy pochodzącej z zdrowego płuca, by naśladować środowisko niskiego stopnia, oraz na podobnej do guza błonie podstawnej, by naśladować bogatszą macierz. Zgodnie z przewidywaniami z modelowania sieciowego, olaparib był bardziej efektywny przeciwko komórkom z mutacją EGFR na macierzy przypominającej zdrową niż na macierzy przypominającej guz, podczas gdy jego efekt na komórkach z mutacją KRAS nie zależał znacząco od typu macierzy. W przeciwieństwie do tego erlotynib zmniejszał żywotność komórek w podobnym stopniu w obu warunkach macierzy, co odpowiada jego profilowi niewrażliwemu na ECM z analizy sieciowej.
Co to oznacza dla pacjentów
Ta praca sugeruje, że wspierające rusztowanie guza nie jest tylko tłem, lecz kluczową cechą, którą można zmierzyć, sklasyfikować i powiązać z tym, jak guzy rosną i reagują na leki. Poprzez klasyfikację raków płuca na stopnie ECM i mapowanie sieci sygnalizacyjnych łączących macierz z zachowaniem komórek, klinicyści mogą w przyszłości dobierać terapie odpowiadające zarówno genetycznemu profilowi nowotworu, jak i jego fizycznemu otoczeniu. Choć potrzeba dodatkowej walidacji, zanim podejście to będzie mogło kierować rutynową opieką, wskazuje ono na przyszłość, w której struktura otaczająca guz pomaga decydować, które leczenia mają największe szanse powodzenia.
Cytowanie: Dansık, A., Sarıca, S., Öztürk, E. et al. Extracellular matrix-driven patient stratification and network modeling reveal distinct molecular grades with potential clinical implications. npj Syst Biol Appl 12, 66 (2026). https://doi.org/10.1038/s41540-026-00697-0
Słowa kluczowe: macierz zewnątrzkomórkowa, gruczolakorak płuca, mikrośrodowisko guza, sieci nowotworowe, odpowiedź na leki