Clear Sky Science · de
Extrazelluläre Matrix‑basierte Patientensegmentierung und Netzwerkmodellierung zeigen unterschiedliche molekulare Grade mit potenziellen klinischen Implikationen
Warum die Umgebung des Tumors wichtig ist
Wenn wir an Krebs denken, stellen wir uns oft entgleiste Zellen vor, die unkontrolliert wachsen. Diese Zellen leben jedoch in einer komplexen Nachbarschaft aus Proteinen und Zuckern, die ein Stützgeflecht bilden, die sogenannte extrazelluläre Matrix. Dieses Geflecht ist keineswegs passiv. Es kann sich versteifen, verdicken und Signale senden, die Tumoren Wachstum oder Therapie‑Resistenz ermöglichen. In dieser Studie untersuchten die Forscher, ob die Zusammensetzung dieses Geflechts in Lungentumoren genutzt werden kann, um Patienten in aussagekräftige Gruppen zu sortieren und therapeutische Entscheidungen zu unterstützen.
Einordnung von Tumoren nach ihrem strukturellen „Gerüst“
Das Team konzentrierte sich auf Lungenadenokarzinome, eine häufige Form von Lungenkrebs, und analysierte 101 Patienten, deren Tumoren auf DNA‑, RNA‑ und Proteinebene umfassend charakterisiert worden waren. Mit einer kuratierten Liste von Genen, die die Matrix aufbauen und regulieren, erstellten sie für jeden Patienten einen „ECM‑Barcode“. Dieser Barcode erfasste, wie stark sich die Matrix jedes Tumors von dem benachbarten normalen Lungengewebe desselben Patienten unterschied. Beim Gruppieren der Patienten anhand dieser Barcodes ergaben sich vier unterschiedliche „ECM‑Grade“, die von nahezu normaler Matrix bis zu Tumoren reichten, die von einem dichten, komplexen Geflecht umgeben waren.
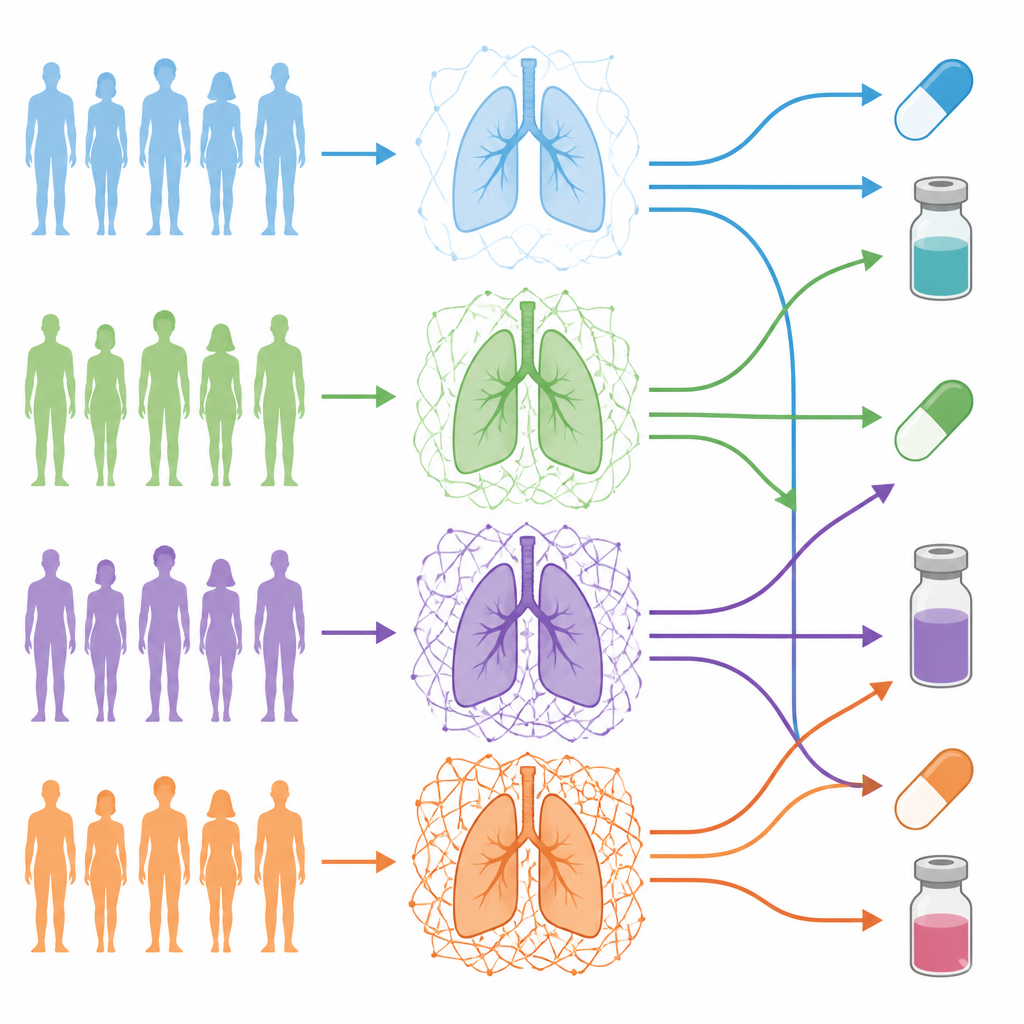
Was hohe und niedrige Grade über den Tumor verraten
Tumoren mit den höchsten ECM‑Graden waren dicht mit stromalen Zellen wie krebsassoziierten Fibroblasten besiedelt und enthielten einen geringeren Anteil an Krebszellen selbst — ein Muster, das mit fortgeschritteneren Mikroumgebungen des Tumors verbunden ist. Diese ECM‑reichen Tumoren zeigten stärkere Signale, die mit epithelial‑mesenchymaler Transition, Invasivität, cancer‑stem‑like Zellen und Gefäßneubildung assoziiert sind. Patienten in den höchsten ECM‑Graden hatten tendenziell aggressivere klinische Merkmale, mehr Tumormutationen und ein erhöhtes kurzfristiges Risiko für Tod oder Rückfall im Vergleich zu Patienten mit spärlicher Matrix.
Verborgene Verdrahtung zwischen Matrix und Zellverhalten
Um aufzudecken, wie die äußere Matrix mit dem inneren Zellverhalten verbunden ist, bauten die Forscher für jeden Patienten Netzwerkmodelle, die veränderte Matrixproteine mit den Signalproteinen und Transkriptionsfaktoren verknüpften, die sie beeinflussen. Die Kombination dieser Netzwerke zeigte, dass höhere ECM‑Grade mit stärkerer Aktivität in Wegen einhergingen, die Zellbewegung, Überleben und Anpassung an mechanische Belastung steuern. Signale, die Zellen dazu anregen, ihre Verankerungen zu lockern, zu migrieren und zu invadieren, waren aktiver, während Schutzfaktoren, die normalerweise Invasion unterdrücken, in ECM‑reichen Tumoren geschwächt waren. Die Studie fand außerdem, dass bestimmte bekannte Krebs‑Mutationen, etwa in KRAS und EGFR, dazu neigten, in verschiedenen ECM‑Graden aufzutreten, was darauf hindeutet, dass die Matrixumgebung und genetische Veränderungen sich gegenseitig verstärken können.
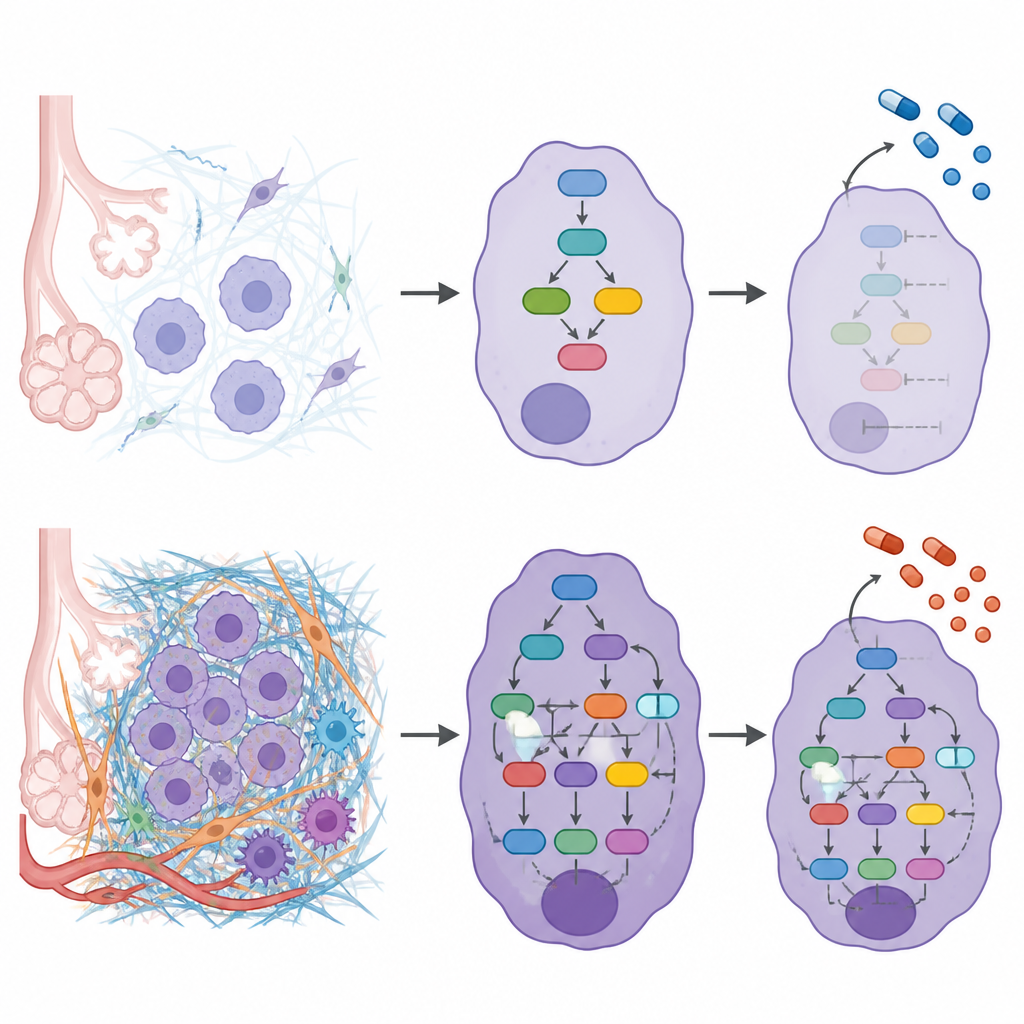
Die Matrix mit Behandlungsentscheidungen verknüpfen
Da die Matrix beeinflussen kann, wie Medikamente Tumorzellen erreichen und wirken, fragten die Forschenden als Nächstes, ob verschiedene ECM‑Grade unterschiedlich auf bestehende Krebsmedikamente reagieren könnten. Mithilfe ihrer Netzwerkkarten maßen sie, wie „nah“ die Wirkziele jedes Arzneimittels an den matrixgetriebenen Signalzentren in jedem Grad lagen. Das offenbarte Medikamente, die in bestimmten ECM‑Konstellationen voraussichtlich am besten wirken, und andere, die gradeübergreifend ähnlich aktiv sein dürften. Ein Wirkstoff, der DNA‑Reparaturenzyme hemmt, Olaparib, schien besonders mit niedrigen ECM‑Graden verbunden zu sein, während ein EGFR‑gerichtetes Medikament, Erlotinib, unabhängig vom ECM‑Grad breit wirksam wirkte.
Vorhersagen im Labor prüfen
Die Forscher rekonstruierten daraufhin vereinfachte Versionen von niedrigen und hohen ECM‑Umgebungen im Labor, indem sie Lungenkrebs‑Zelllinien mit entweder KRAS‑ oder EGFR‑Mutationen verwendeten. Sie kultivierten die Zellen auf gesunder, aus Lunge gewonnener Matrix, um eine niedriggradige Umgebung zu simulieren, und auf einer tumorähnlichen Basalmembran, um eine reichere Matrix nachzubilden. Entsprechend den Netzwerkvorhersagen war Olaparib bei EGFR‑mutierten Zellen auf der gesund‑ähnlichen Matrix wirksamer als auf der tumorähnlichen Matrix, während seine Wirkung auf KRAS‑mutierte Zellen wenig vom Matrixtyp abhing. Im Gegensatz dazu verringerte Erlotinib die Zellvitalität in beiden Matrixbedingungen in ähnlichem Maße, was seinem ECM‑unempfindlichen Profil aus der Netzwerkanalyse entsprach.
Was das für Patienten bedeutet
Diese Arbeit legt nahe, dass das Stützgerüst des Tumors nicht nur Kulisse, sondern ein messbares Merkmal ist, das gruppiert und mit dem Wachstum der Tumoren sowie ihrer Reaktion auf Medikamente verknüpft werden kann. Durch die Einteilung von Lungenkrebs in ECM‑Grade und die Kartierung der Signalnetzwerke, die die Matrix mit dem Zellverhalten verbinden, könnten Kliniker künftig Therapien auswählen, die sowohl zur genetischen Ausstattung des Krebses als auch zu seiner physischen Umgebung passen. Obwohl vor einer routinemäßigen Anwendung noch weitere Validierungen nötig sind, weist der Ansatz in eine Zukunft, in der die Struktur um den Tumor mitentscheidet, welche Behandlungen am wahrscheinlichsten wirken.
Zitation: Dansık, A., Sarıca, S., Öztürk, E. et al. Extracellular matrix-driven patient stratification and network modeling reveal distinct molecular grades with potential clinical implications. npj Syst Biol Appl 12, 66 (2026). https://doi.org/10.1038/s41540-026-00697-0
Schlüsselwörter: extrazelluläre Matrix, Lungenadenokarzinom, Tumormikroumgebung, Krebsnetzwerke, Arzneimittelantwort