Clear Sky Science · es
La estratificación de pacientes impulsada por la matriz extracelular y el modelado de redes revela grados moleculares distintos con posibles implicaciones clínicas
Por qué importa el entorno del tumor
Cuando pensamos en el cáncer, a menudo imaginamos células rebeldes que crecen fuera de control. Pero esas células viven en un vecindario complejo formado por proteínas y azúcares que constituyen una malla de soporte llamada matriz extracelular. Esa malla está lejos de ser pasiva: puede endurecerse, espesarse y enviar señales que ayudan a los tumores a crecer o a resistir tratamientos. En este estudio, los investigadores preguntaron si la composición de esa malla en tumores pulmonares podría usarse para clasificar a los pacientes en grupos con significado clínico y orientar la elección de terapias.
Clasificar tumores según su “andamiaje” estructural
El equipo se centró en el adenocarcinoma de pulmón, un tipo común de cáncer de pulmón, y analizó 101 pacientes cuyos tumores habían sido perfilados en profundidad a nivel de ADN, ARNm y proteínas. Utilizaron una lista curada de genes que construyen y regulan la matriz para crear un “código de barras ECM” para cada paciente. Este código reflejaba cuánto difería la matriz de cada tumor respecto al tejido pulmonar normal cercano del mismo paciente. Al agrupar a los pacientes usando estos códigos, emergieron cuatro “grados de ECM” distintos, que iban desde una matriz casi similar a la normal hasta tumores envueltos en una malla densa y compleja.
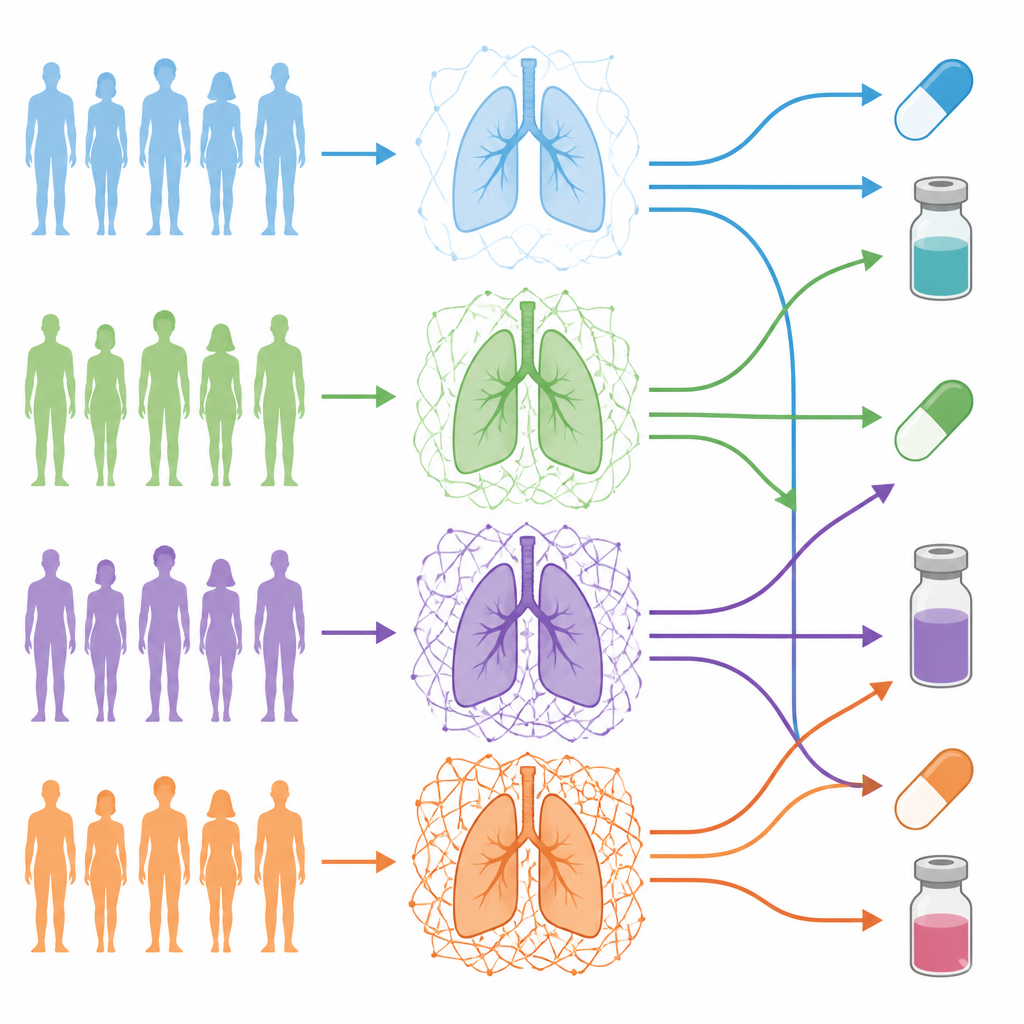
Qué revelan los grados altos y bajos sobre el tumor
Los tumores con los grados de ECM más altos estaban llenos de células del estroma como fibroblastos asociados al cáncer y tenían fracciones más bajas de células cancerosas propias, un patrón vinculado a microambientes tumorales más avanzados. Estos tumores ricos en ECM mostraron señales más intensas asociadas a la transición epitelio-mesénquima, invasividad, células con características de células madre cancerosas y angiogénesis. Los pacientes en el grado de ECM más alto tendieron a presentar características clínicas más agresivas, más mutaciones tumorales y un mayor riesgo a corto plazo de muerte o recidiva, en comparación con pacientes cuyos tumores tenían una matriz escasa.
Conexiones ocultas entre la matriz y el comportamiento celular
Para descubrir cómo la matriz externa se conecta con el comportamiento interno de las células, los investigadores construyeron modelos de redes para cada paciente que vinculaban proteínas de la matriz alteradas con las proteínas de señalización y los factores de transcripción que influyen. Al combinar estas redes, observaron que los grados de ECM más altos se asociaban con una mayor actividad en vías que regulan el movimiento celular, la supervivencia y la adaptación al estrés mecánico. Las señales que favorecen que las células aflojen sus adhesiones, migren e invadan estaban más activas, mientras que los factores protectores que normalmente suprimen la invasión eran más débiles en tumores ricos en ECM. El estudio también encontró que ciertas mutaciones tumorales bien conocidas, como las de KRAS y EGFR, tendían a aparecer en distintos grados de ECM, lo que sugiere que el entorno de la matriz y los cambios genéticos pueden reforzarse mutuamente.
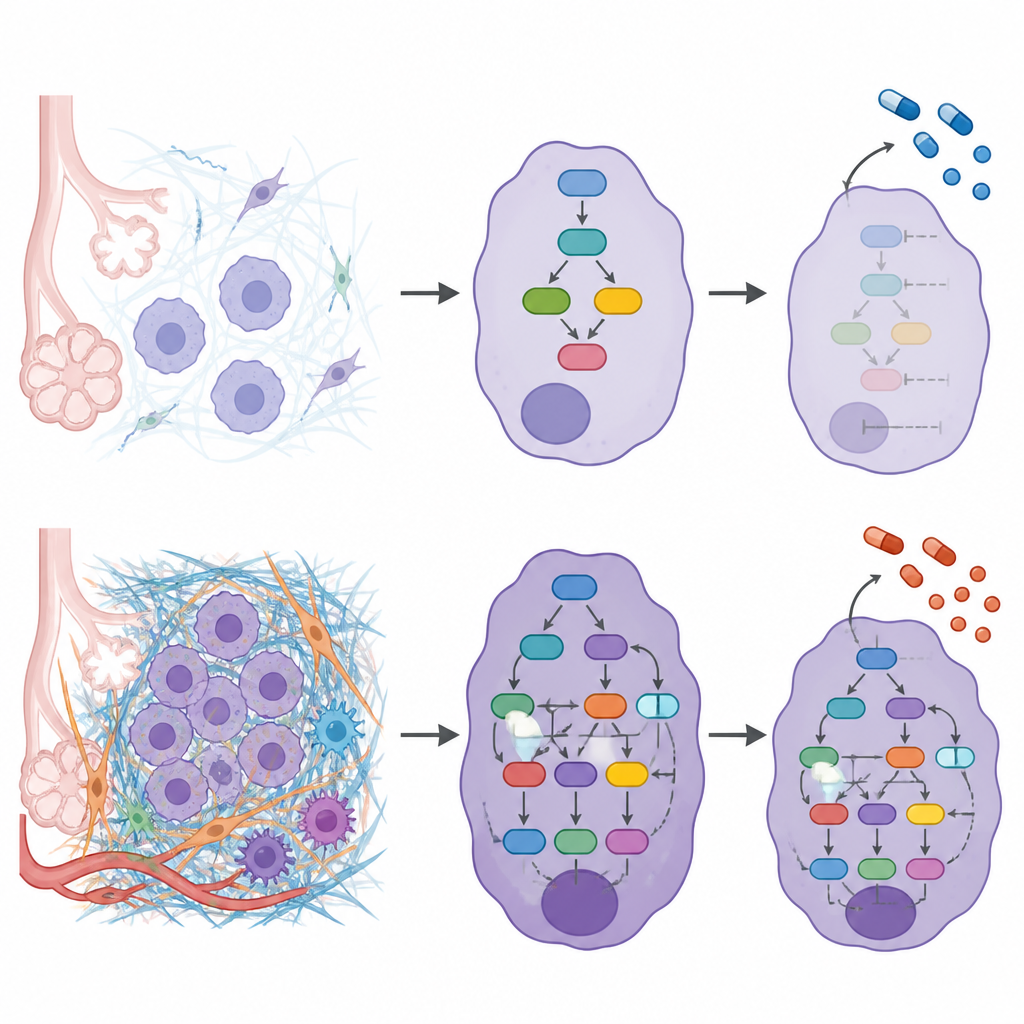
Vincular la matriz con las decisiones terapéuticas
Dado que la matriz puede influir en cómo los fármacos alcanzan y afectan a las células tumorales, el equipo se preguntó si los diferentes grados de ECM podrían responder de forma distinta a medicamentos oncológicos existentes. Usando sus mapas de redes, midieron cuán “cerca” estaban las dianas de cada fármaco de los nodos de señalización impulsados por la matriz en cada grado. Esto reveló medicamentos previstos para funcionar mejor en escenarios ECM específicos y otros que probablemente actúen de forma similar entre grados. Un fármaco que inhibe enzimas de reparación del ADN, olaparib, apareció especialmente conectado a los grados bajos de ECM, mientras que un inhibidor de EGFR, erlotinib, parecía eficaz de forma amplia sin depender del grado de ECM.
Poner las predicciones a prueba en el laboratorio
Los investigadores recrearon luego versiones simplificadas de entornos ECM bajos y altos en el laboratorio usando líneas celulares de cáncer de pulmón portadoras de mutaciones en KRAS o EGFR. Cultivaron las células sobre matriz derivada de pulmón sano para imitar un entorno de grado bajo y sobre una membrana basal similar a tumoral para simular una matriz más rica. En consonancia con las predicciones de las redes, olaparib fue más potente contra células con mutación en EGFR sobre la matriz de aspecto sano que sobre la similar a tumor, mientras que su efecto sobre células con mutación en KRAS no dependió mucho de la matriz. En contraste, erlotinib redujo la viabilidad celular en grado similar en ambas condiciones de matriz, coincidiendo con su perfil insensible al ECM observado en el análisis de redes.
Qué significa esto para los pacientes
Este trabajo sugiere que el andamiaje que sostiene al tumor no es solo un telón de fondo, sino una característica clave que puede medirse, agruparse y vincularse con cómo los tumores crecen y responden a fármacos. Al clasificar los cánceres de pulmón en grados de ECM y mapear las redes de señalización que conectan la matriz con el comportamiento celular, los clínicos podrían, en el futuro, seleccionar terapias que se ajusten tanto al perfil genético del cáncer como a su entorno físico. Aunque se necesita más validación antes de que este enfoque pueda guiar la práctica clínica rutinaria, apunta hacia un futuro en el que la estructura alrededor del tumor ayude a decidir qué tratamientos tienen más probabilidades de funcionar.
Cita: Dansık, A., Sarıca, S., Öztürk, E. et al. Extracellular matrix-driven patient stratification and network modeling reveal distinct molecular grades with potential clinical implications. npj Syst Biol Appl 12, 66 (2026). https://doi.org/10.1038/s41540-026-00697-0
Palabras clave: matriz extracelular, adenocarcinoma de pulmón, microambiente tumoral, redes del cáncer, respuesta a fármacos