Clear Sky Science · ru
Стратификация пациентов по внеклеточному матриксу и моделирование сетей выявляют различные молекулярные градации с потенциальными клиническими последствиями
Почему окружение опухоли имеет значение
Когда мы думаем о раке, часто представляем себе бунтующие клетки, которые бесконтрольно растут. Но эти клетки живут в сложном окружении из белков и сахаров, формирующих опорную «сеть» — внеклеточный матрикс. Эта сеть далека от пассивности. Она может уплотняться, утолщаться и передавать сигналы, которые помогают опухолям расти или сопротивляться терапии. В этом исследовании учёные задали вопрос: можно ли использовать состав этой сети в опухолях легких для разделения пациентов на информативные группы и для выбора терапии.
Сортировка опухолей по их структурному «каркасу»
Команда сосредоточилась на аденокарциноме легкого, распространённом типе рака легкого, и проанализировала 101 пациента, чьи опухоли были глубоко охарактеризованы на уровнях ДНК, РНК и белков. Они использовали курированный список генов, отвечающих за формирование и регуляцию матрикса, чтобы создать «ECM-штрихкод» для каждого пациента. Этот штрихкод отражал, насколько матрикс каждой опухоли отличался от близкой нормальной ткани легкого у того же пациента. При группировке пациентов по этим штрихкодам выявились четыре различных «градации ECM», от почти нормального матрикса до опухолей, окружённых плотной и сложной сетью.
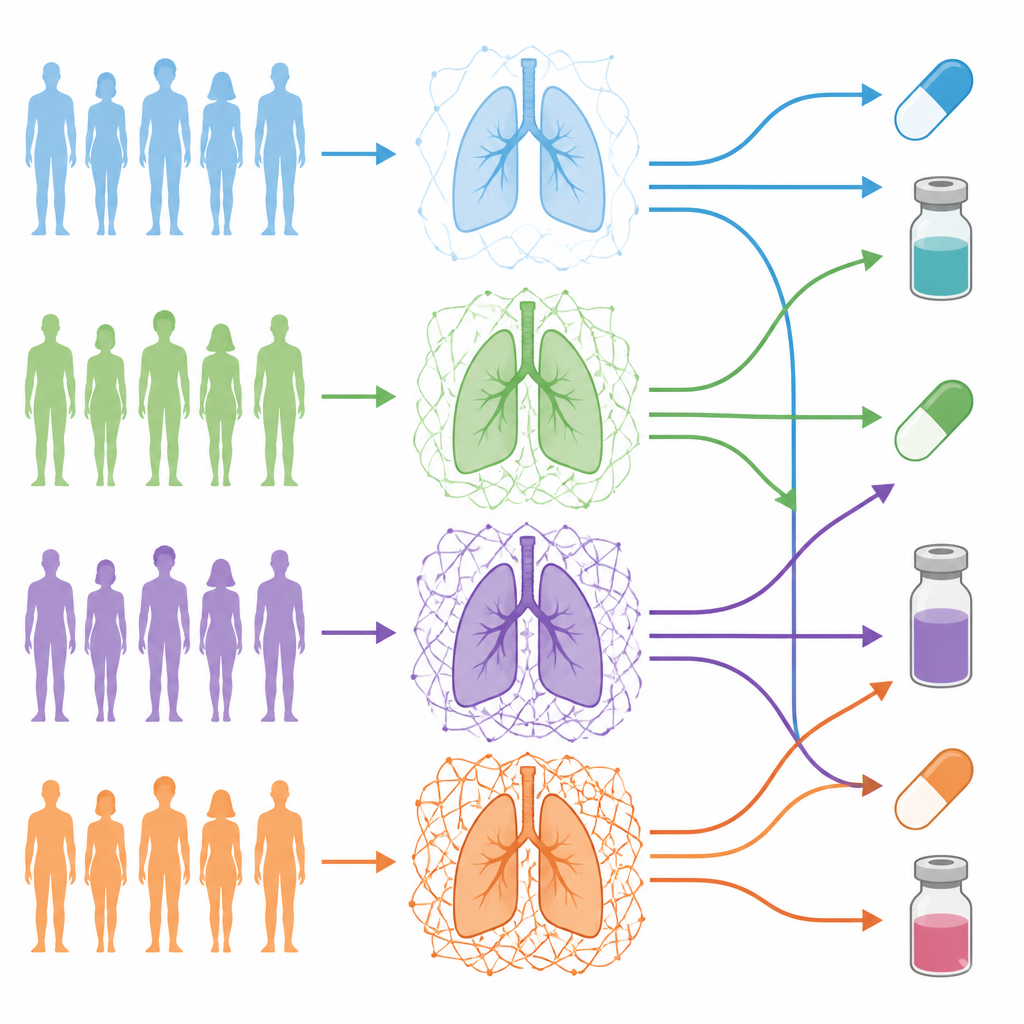
Что показывают высокие и низкие градации
Опухоли с наивысшими градациями ECM были насыщены стромальными клетками, такими как фибробласты, ассоциированные с раком, и имели более низкую долю собственно раковых клеток — паттерн, связанный с более продвинутым микросредой опухоли. Эти обогащённые матриксом опухоли демонстрировали усиленные сигналы, связанные с эпителиально-мезенхимальным переходом, инвазивностью, клетками с признаками стволовых свойств и ангиогенезом. Пациенты с опухолями высокого ECM-грейда, как правило, имели более агрессивные клинические признаки, большее число мутаций в опухоли и более высокий краткосрочный риск смерти или рецидива по сравнению с пациентами с разреженным матриксом.
Скрытая проводка между матриксом и поведением клеток
Чтобы выяснить, как внешний матрикс связан с внутренним поведением клеток, исследователи построили сетевые модели для каждого пациента, которые связывали изменённые матричные белки с сигнальными белками и транскрипционными факторами, на которые они влияют. Объединение этих сетей показало, что более высокие градации ECM связаны с усиленной активностью путей, регулирующих движение клеток, выживание и адаптацию к механическим нагрузкам. Сигналы, поощряющие ослабление клеточных прикреплений, миграцию и инвазию, были более активны, тогда как защитные факторы, которые обычно подавляют инвазию, были ослаблены в опухолях, богатых матриксом. Исследование также обнаружило, что некоторые известные онкогенные мутации, например в KRAS и EGFR, имеют склонность возникать в разных градациях ECM, что говорит о том, что окружение матрикса и генетические изменения могут взаимно усиливать друг друга.
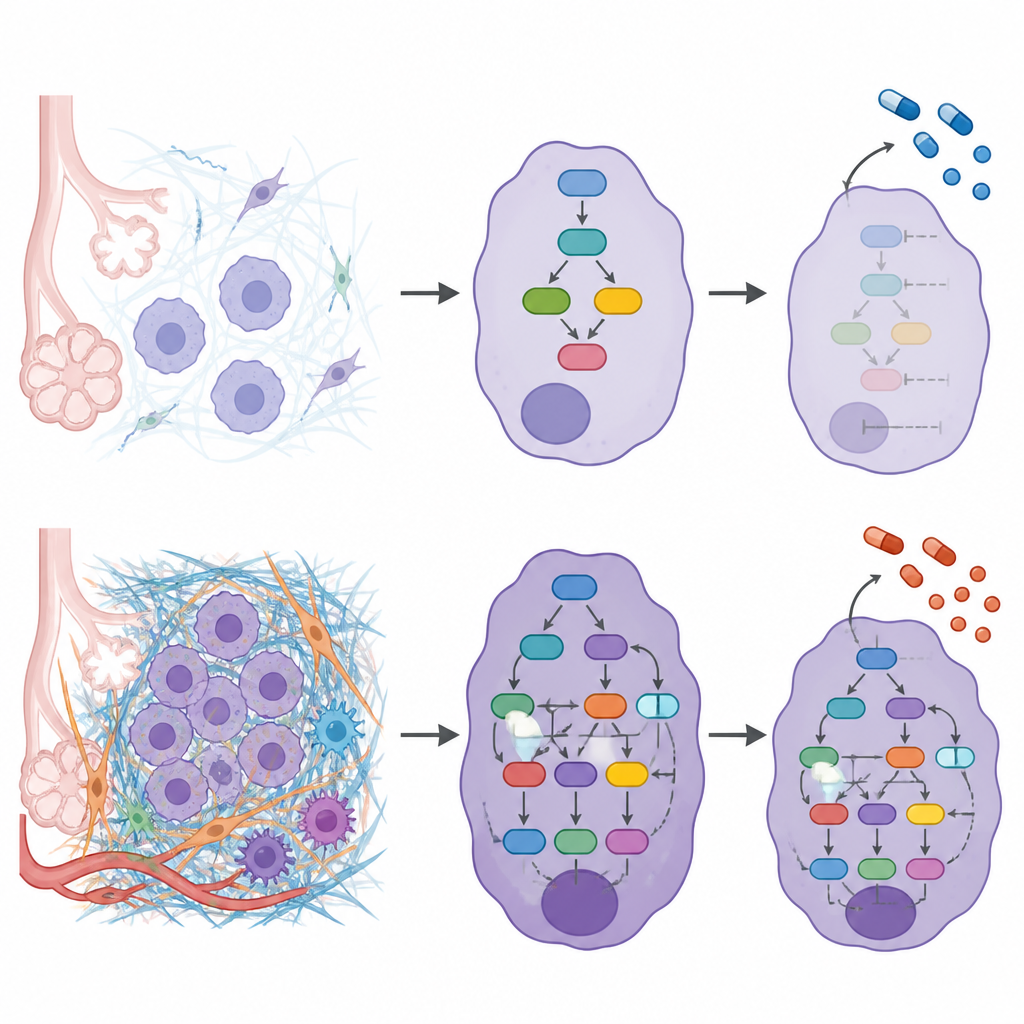
Связь матрикса с выбором лечения
Поскольку матрикс может определять, как препараты достигают и влияют на опухолевые клетки, команда далее изучила, могут ли разные градации ECM по‑разному реагировать на существующие противораковые средства. Используя свои сетевые карты, они оценили, насколько «близки» мишени каждого препарата к сигнальным узлам, управляемым матриксом, в каждой градации. Это выявило лекарства, прогнозируемые как оптимальные для конкретных ECM‑условий, и другие, которые, вероятно, действуют схожим образом во всех градациях. Один препарат, блокирующий ферменты репарации ДНК — олапариб, оказался особенно связан с низкими градациями ECM, в то время как препарат, нацеленный на EGFR — эрлотиниб, выглядел эффективным независимо от градации ECM.
Проверка предсказаний в лаборатории
Затем исследователи воссоздали упрощённые версии низкого и высокого ECM‑окружения в лаборатории, используя линии клеток рака легкого с мутациями KRAS или EGFR. Они выращивали клетки на матриксе, полученном из здоровой ткани легкого, чтобы имитировать среду низкого грейда, и на опухолеподобной базальной мембране, чтобы имитировать более богатый матрикс. В соответствии с сетевыми предсказаниями олапариб оказывал большее действие на клетки с мутацией EGFR на матриксе, похожем на здоровый, чем на опухолеподобном, тогда как его эффект на клетки с мутацией KRAS мало зависел от матрикса. Напротив, эрлотиниб снижал жизнеспособность клеток в обоих условиях матрикса в схожей степени, что соответствует его ECM‑независимому профилю из сетевого анализа.
Что это значит для пациентов
Эта работа предлагает, что опорный каркас опухоли — не просто фон, а ключевая характеристика, которую можно измерить, классифицировать и связать с тем, как опухоли растут и реагируют на лекарства. Классифицируя рак легкого по градациям ECM и картируя сигнальные сети, связывающие матрикс с поведением клеток, клиницисты в будущем, возможно, смогут подбирать терапии с учётом и генетики опухоли, и её физического окружения. Хотя для внедрения этого подхода в рутинную практику требуется дополнительная валидация, исследование указывает на будущее, в котором структура вокруг опухоли будет помогать решать, какие лечения наиболее вероятно окажутся эффективными.
Цитирование: Dansık, A., Sarıca, S., Öztürk, E. et al. Extracellular matrix-driven patient stratification and network modeling reveal distinct molecular grades with potential clinical implications. npj Syst Biol Appl 12, 66 (2026). https://doi.org/10.1038/s41540-026-00697-0
Ключевые слова: внеклеточный матрикс, аденокарцинома легкого, микроокружение опухоли, раковые сети, ответ на препараты