Clear Sky Science · he
מיון מטופלים מונע מטריקס חוץ-תאי ומידול רשתות חושפים דרגות מולקולריות מובחנות עם השלכות קליניות פוטנציאליות
למה הסביבה של הגידול חשובה
כשאנחנו חושבים על סרטן, לעתים קרובות מדמיינים תאים שמרשעתם יוצאת משליטה. אבל אותם תאים חיים בשכונה מורכבת המורכבת מחלבונים וסוכרים היוצרים מסגרת תמיכה הקרויה המטריקס החוץ-תאי. המסגרת הזו רחוקה מלהיות פסיבית. היא עלולה להתקשח, לעבות ולשדר אותות המסייעים לגידולים לצמוח או לעמוד בעמידות לטיפול. במחקר זה בדקו האם הרכב המסגרת הזו בגידולי ריאה ניתן לשמש למיון מטופלים לקבוצות בעלות משמעות קלינית ולהנחיית בחירות טיפוליות.
מיון הגידולים לפי "שלד" מבני
הצוות התמקד במדיאפאדנוקרצינומה של הריאה, סוג שכיח של סרטן ריאה, וניתח 101 מטופלים שלגידוליהם ניתחה פרופיל עמוק ברמות ה-DNA, RNA וחלבונים. הם השתמשו ברשימה קשובה של גנים שבונים ומארגנים את המטריקס כדי ליצור "ברקוד ECM" לכל מטופל. הברקוד הזה תיעד עד כמה המטריקס של כל גידול שונה מרקמת הריאה הנורמלית הסמוכה של אותו מטופל. כאשר קיבצו את המטופלים לפי הברקודים הללו, צפו ארבע דרגות ECM מובחנות, הנעות מדרגה כמעט נורמלית עד גידולים עטופים ברשת צפופה ומורכבת.
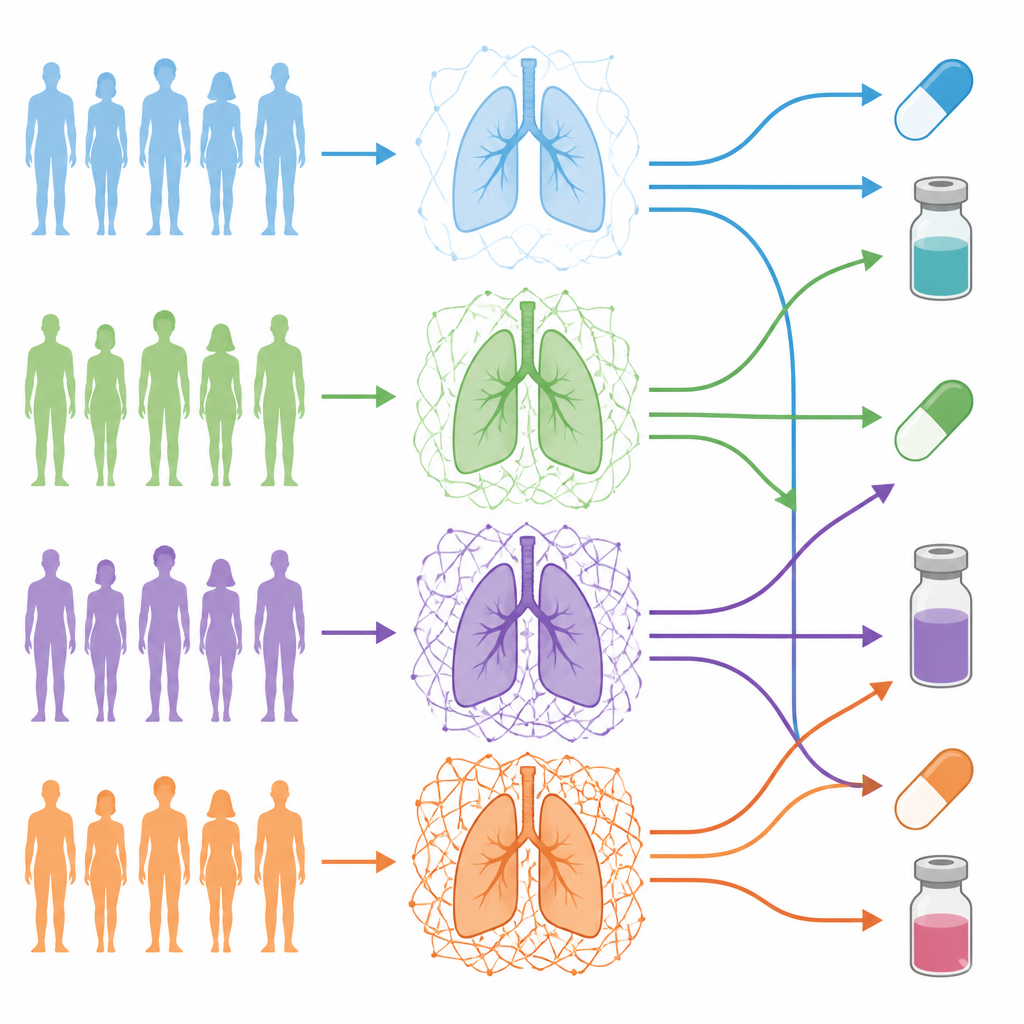
מה חושפות דרגות גבוהות ונמוכות על הגידול
גידולים בדרגות ECM הגבוהות ביותר היו רוויים בתאים סטרומליים כגון פיברובלסטים קשורים לסרטן, והיו בהם אחוזים נמוכים יותר של תאי סרטן עצמם — דפוס המקושר למיקרו-סביבות גידול מתקדמות יותר. גידולים עשירים במטריקס הראו אותות חזקים הקשורים למעבר אפיתליאלי-מזנכימלי, לחדירה, לתאי דמויי גזע סרטן ולצמיחת כלי דם. מטופלים בדרגת ECM הגבוהה נטו להציג מאפיינים קליניים אגרסיביים יותר, יותר מוטציות בגידול וסיכון קצר-טווח גבוה יותר לתמותה או לחזרת הסרטן, בהשוואה למטופלים שגידולם חופף במטריקס דליל.
חיבורים נסתרים בין המטריקס להתנהגות התא
כדי לחשוף כיצד המטריקס החיצוני מתחבר להתנהגות פנימית של תאים, בנו החוקרים מודלים של רשת לכל מטופל שקישרו חלבוני מטריקס משנים לחלבוני איתות ופקטורי שעתוק שהם משפיעים עליהם. שילוב הרשתות הללו הראה שדרגות ECM גבוהות יותר מקושרות לפעילות מוגברת במסלולים שמווסתים תנועת התא, הישרדות והתאמה ללחץ מכאני. אותות שמעודדים תאים לשחרר את עיגונם, לנוע ולחדור היו פעילים יותר, בעוד שגורמים מגינים שבדרך כלל מדכאים חדירה היו חלשים יותר בגידולים עשירים במטריקס. המחקר גם מצא שמוטציות סרטניות ידועות, כגון ב-KRAS וב-EGFR, נטו להופיע בדרגות ECM שונות, מה שמרמז כי סביבת המטריקס והשינויים הגנטיים עשויים לחזק זה את זה.
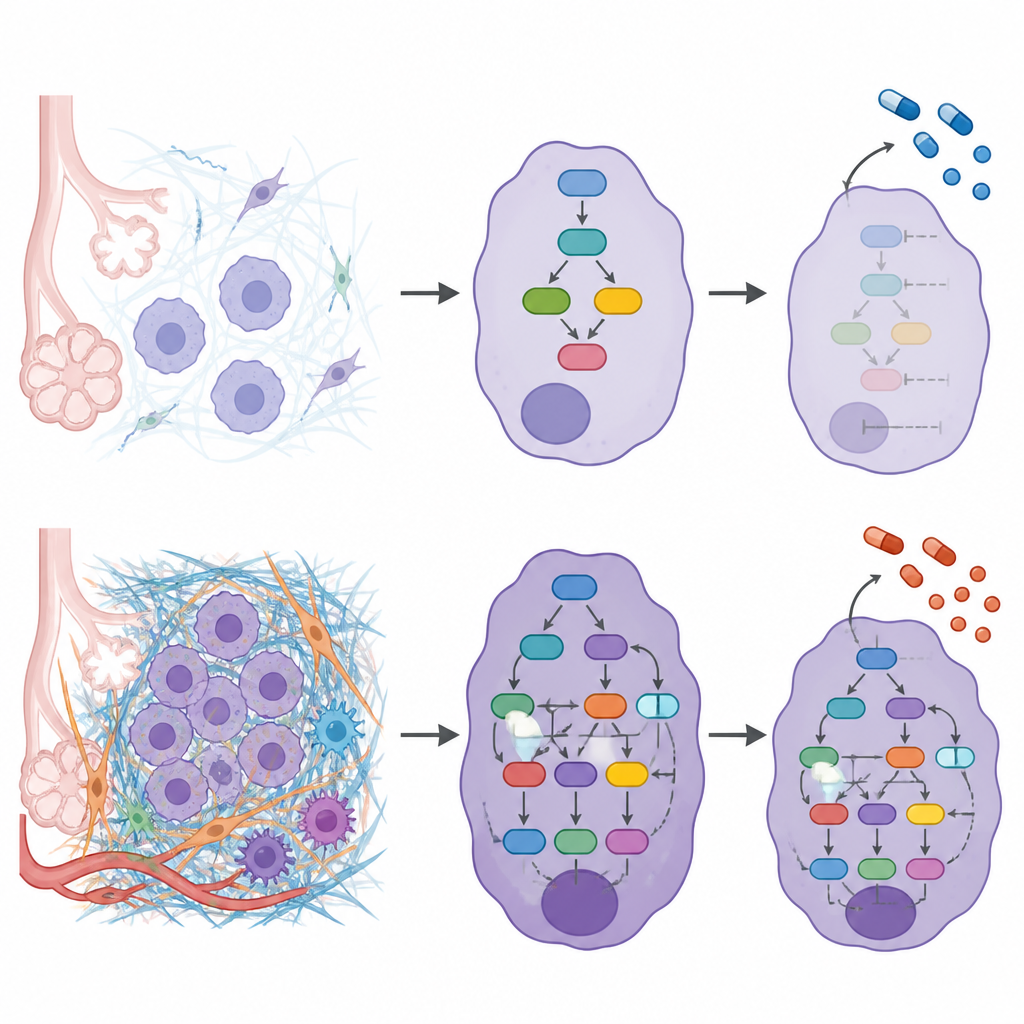
קישור המטריקס לבחירות טיפוליות
מכיוון שהמטריקס יכול לעצב את אופן הגעת התרופות והשפעתן על תאי הגידול, בחן הצוות האם דרגות ECM שונות עשויות להגיב אחרת לתרופות קיימות. באמצעות מיפוי הרשת שלהם, מדדו עד כמה המטרות של כל תרופה קרובות לצירי האיתות המונחים על ידי המטריקס בכל דרגה. זה חשף תרופות שחזויות לעבוד טוב ביותר בסביבות ECM מסוימות ואחרות שסביר שיפעלו באופן דומה על פני הדרגות. תרופה שחוסמת אנזימי תיקון DNA, אולפאריב, הופיעה כקשורה במיוחד לדרגות ECM נמוכות, בעוד שתרופה המכוונת ל-EGFR, ארלוטיניב, נראתה יעילה בהיקף רחב ללא תלות בדרגת ECM.
בדיקת התחזיות במעבדה
החוקרים שיחזרו אז גרסאות מפושטות של סביבות ECM נמוכות וגבוהות במעבדה באמצעות קווי תאי סרטן ריאה נשאים של מוטציות ב-KRAS או ב-EGFR. הם גידלו את התאים על מטריקס שמקורו בריאה בריאה כדי לדמות סביבה מדורגת-נמוכה ועל ממברנת בסיס דמוית-גידול כדי לדמות מטריקס עשיר יותר. בהתאם לתחזיות מהרשת, אולפאריב היה פעיל יותר נגד תאים עם מוטציית EGFR על מטריקס בדומה לבריא מאשר על מטריקס בדומה לגידול, בעוד שהשפעתו על תאי KRAS-מוטנטיים לא הושפעה במידה רבה מהמטריקס. לעומת זאת, ארלוטיניב הוריד את כושר ההישרדות התאית במידה דומה בשתי תנאי המטריקס, בהתאמה לפרופיל שאינו-תלוי ECM שנגזר מניתוח הרשת.
מה זה אומר למטופלים
העבודה הזו מצביעה על כך שהשלד התומך של הגידול אינו רק רקע אלא תכונה מרכזית שניתן למדוד, למיין ולשים בקשר לאופן שבו גידולים גדלים ומגיבים לתרופות. על ידי סיווג סרטןי ריאה לדרגות ECM ומיפוי רשתות האיתות שקושרות את המטריקס להתנהגות התא, קלינאים עשויים יום אחד לבחור טיפולים המתאימים גם למארג הגנטי של הסרטן וגם לסביבתו הפיזית. בעוד שצריך עוד אימות לפני ששיטה זו תוכל להנחות טיפול שגרתי, היא מצביעה לעתיד שבו המבנה סביב הגידול מסייע להחליט אילו טיפולים צפויים להיות היעילים ביותר.
ציטוט: Dansık, A., Sarıca, S., Öztürk, E. et al. Extracellular matrix-driven patient stratification and network modeling reveal distinct molecular grades with potential clinical implications. npj Syst Biol Appl 12, 66 (2026). https://doi.org/10.1038/s41540-026-00697-0
מילות מפתח: מטריקס חוץ-תאי, מדיאפאדנוקרצינומה של הריאה, מיקרו-סביבת הגידול, רשתות סרטניות, תגובת תרופות