Clear Sky Science · nl
Door de extracellulaire matrix aangedreven patiëntstratificatie en netwerkmodellering onthullen onderscheidende moleculaire gradaties met potentiële klinische implicaties
Waarom de omgeving van de tumor ertoe doet
Als we aan kanker denken, zien we vaak losse cellen die ongecontroleerd groeien. Die cellen leven echter in een complex buurtje van eiwitten en suikers dat een steunraamwerk vormt: de extracellulaire matrix. Dat raamwerk is allesbehalve passief. Het kan verharden, verdikken en signalen afgeven die tumorgroei of behandelresistentie bevorderen. In deze studie vroegen de onderzoekers of de samenstelling van dat raamwerk in longtumoren gebruikt kon worden om patiënten in zinvolle groepen in te delen en therapiekeuzes te sturen.
Tumoren sorteren op hun structurele “steigers”
Het team richtte zich op longadenocarcinoom, een veelvoorkomend type longkanker, en analyseerde 101 patiënten van wie de tumoren diepgaand waren geprofileerd op DNA-, RNA- en proteïneniveau. Ze gebruikten een samengestelde lijst van genen die de matrix opbouwen en reguleren om voor elke patiënt een “ECM‑barcode” te maken. Deze barcode legde vast hoe sterk de matrix van elke tumor afweek van het nabijgelegen normale longweefsel van die patiënt. Bij het groeperen van patiënten op basis van deze barcodes kwamen vier onderscheiden “ECM‑gradaties” naar voren, variërend van vrijwel normaal-achtig matrix tot tumoren omhuld door een dicht, complex netwerk.
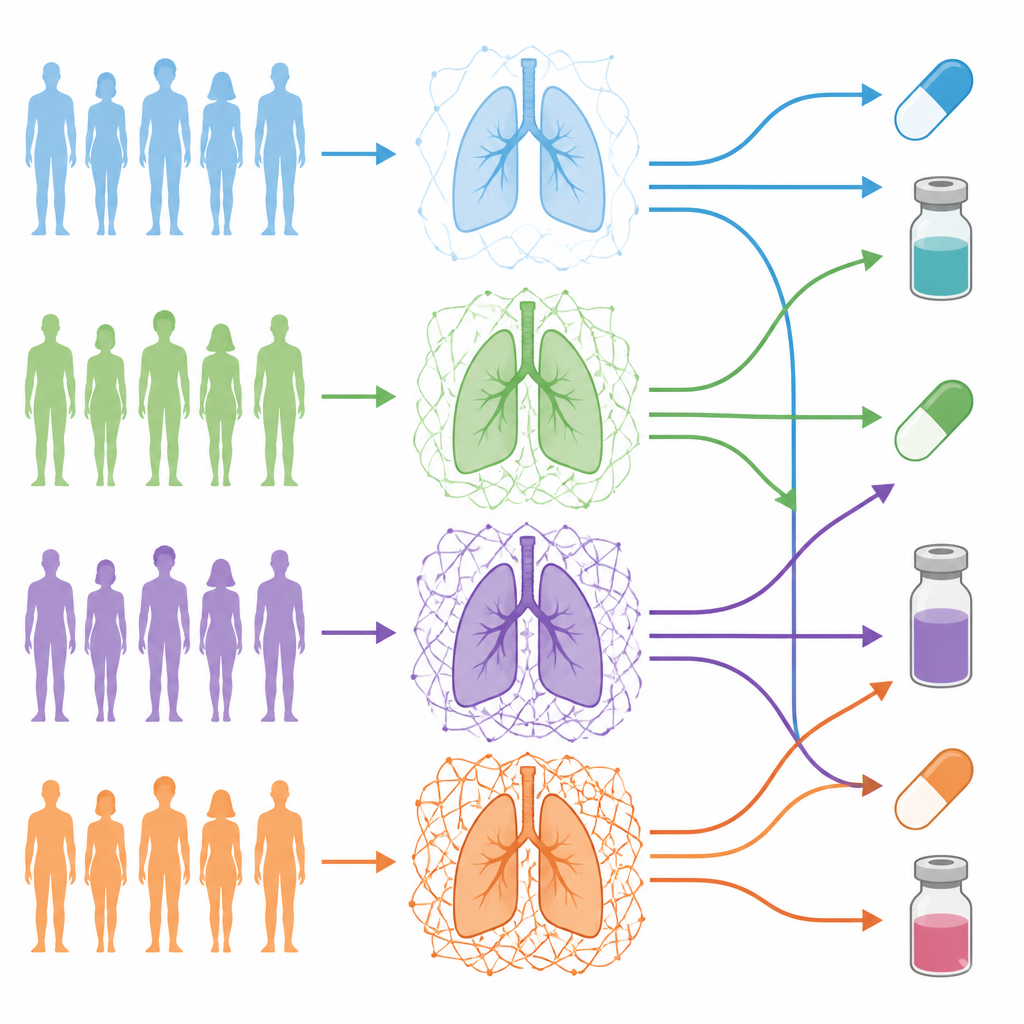
Wat hoge en lage gradaties over de tumor onthullen
Tumoren met de hoogste ECM‑gradaties zaten vol met stroma‑cellen zoals kanker‑geassocieerde fibroblasten en hadden een lager aandeel kankercellen zelf, een patroon dat gekoppeld is aan meer geavanceerde tumormicro‑omgevingen. Deze ECM‑rijke tumoren toonden sterkere signalen geassocieerd met epitheliale‑naar‑mesenchymale transitie, invasiviteit, kankerstam‑achtige eigenschappen en bloedvatvorming. Patiënten met tumoren in de hoogste ECM‑gradatie hadden vaker agressievere klinische kenmerken, meer tumor‑mutaties en een hoger kortetermijnrisico op overlijden of terugkeer van kanker vergeleken met patiënten met een schaars matrix.
Verborgen koppelingen tussen de matrix en celgedrag
Om te achterhalen hoe de buitenste matrix verbonden is met het binnenste celgedrag bouwden de onderzoekers voor elke patiënt netwerkmodellen die gewijzigde matrixeiwitten koppelden aan de signaalproteïnen en transcriptiefactoren die zij beïnvloeden. Door deze netwerken te combineren bleek dat hogere ECM‑gradaties samenhingen met sterkere activiteit in paden die celbeweging, overleving en aanpassing aan mechanische stress reguleren. Signaleringen die cellen aanzetten losser te hechten, te migreren en te infiltreren waren actiever, terwijl beschermende factoren die normaal invasie onderdrukken zwakker waren in ECM‑rijke tumoren. De studie vond ook dat sommige goed bekende kankermutaties, zoals in KRAS en EGFR, vaker voorkwamen in verschillende ECM‑gradaties, wat suggereert dat de matrixomgeving en genetische veranderingen elkaar kunnen versterken.
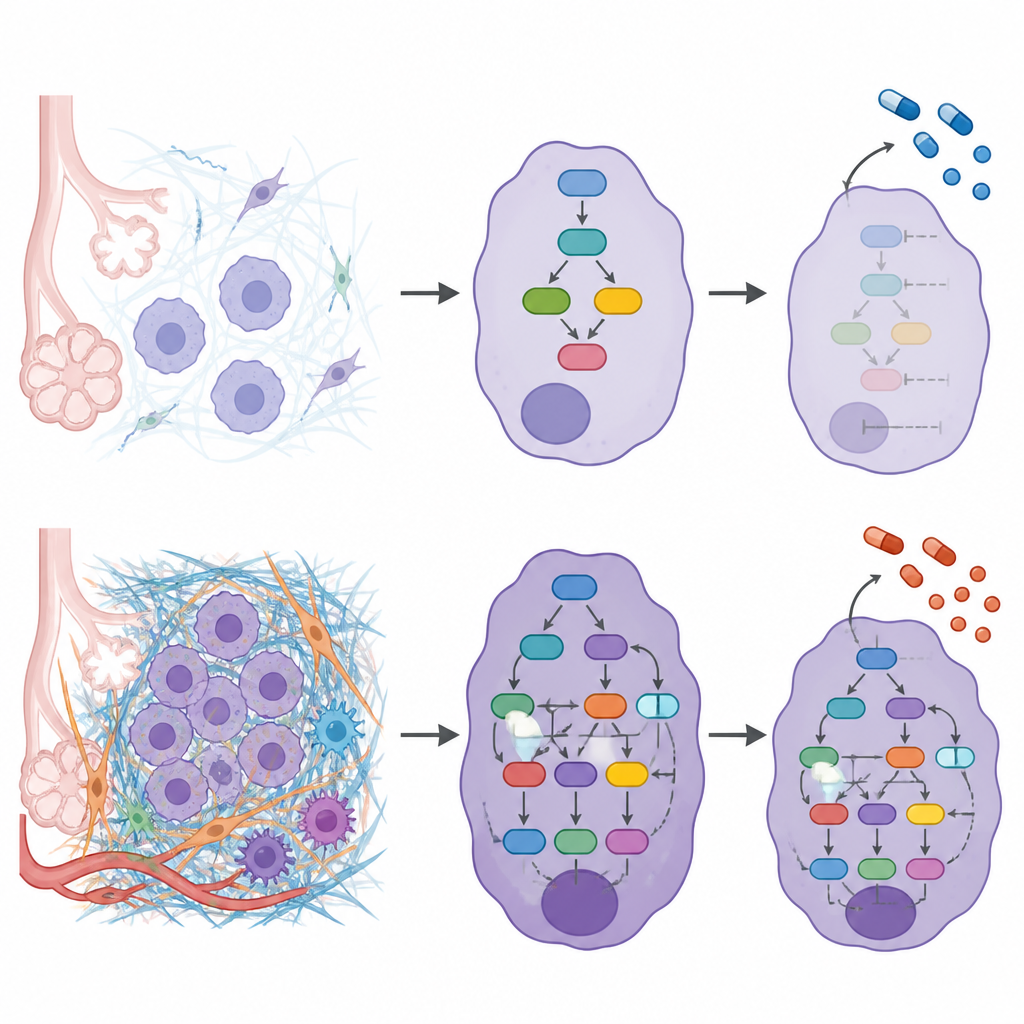
De matrix koppelen aan behandelkeuzes
Aangezien de matrix kan beïnvloeden hoe geneesmiddelen de tumorcellen bereiken en beïnvloeden, vroegen de onderzoekers vervolgens of verschillende ECM‑gradaties verschillend zouden reageren op bestaande kankertherapieën. Met hun netwerkmappen maten ze hoe “dicht” de doelmoleculen van elk geneesmiddel stonden bij de matrix‑gedreven signaalhubs in elke gradatie. Dit onthulde middelen die voorspeld werden het beste te werken in specifieke ECM‑omgevingen en andere die naar verwachting vergelijkbaar zouden werken over gradaties heen. Een middel dat DNA‑herstelenzymen remt, olaparib, leek vooral verbonden met lage ECM‑gradaties, terwijl een EGFR‑gericht middel, erlotinib, breed effectief leek ongeacht de ECM‑gradatie.
Voorspellingen in het laboratorium testen
De onderzoekers maakten vervolgens vereenvoudigde versies van lage en hoge ECM‑omgevingen na in het laboratorium met behulp van longkankercellijnen die óf KRAS‑ óf EGFR‑mutaties droegen. Ze groeiden de cellen op gezond longafgeleid matrix om een lage‑gradatie omgeving te simuleren en op een tumorachtig basaalmembraan om een rijkere matrix na te bootsen. In overeenstemming met de netwerkvoorspellingen was olaparib krachtiger tegen EGFR‑gemuteerde cellen op het gezond‑achtige matrix dan op het tumorachtige matrix, terwijl het effect op KRAS‑gemuteerde cellen weinig afhankelijkt van de matrix was. Daarentegen verminderde erlotinib de cellulaire levensvatbaarheid in vergelijkbare mate in beide matrixcondities, wat overeenkomt met het ECM‑ongevoelige profiel uit de netwerkanalyse.
Wat dit betekent voor patiënten
Dit werk suggereert dat het steunraamwerk van de tumor niet slechts achtergrond is, maar een belangrijke eigenschap die gemeten, geclassificeerd en gekoppeld kan worden aan hoe tumoren groeien en reageren op geneesmiddelen. Door longkankers in ECM‑gradaties in te delen en de signaalnetwerken in kaart te brengen die de matrix met celgedrag verbinden, zouden clinici uiteindelijk therapieën kunnen kiezen die passen bij zowel het genetische profiel van de kanker als haar fysieke omgeving. Hoewel meer validatie nodig is voordat deze benadering routinematig klinische beslissingen kan sturen, wijst het op een toekomst waarin de structuur rond de tumor meehelpt bepalen welke behandelingen het meest kansrijk zijn.
Bronvermelding: Dansık, A., Sarıca, S., Öztürk, E. et al. Extracellular matrix-driven patient stratification and network modeling reveal distinct molecular grades with potential clinical implications. npj Syst Biol Appl 12, 66 (2026). https://doi.org/10.1038/s41540-026-00697-0
Trefwoorden: extracellulaire matrix, longadenocarcinoom, tumormicro‑omgeving, kankernetwerken, geneesmiddelrespons