Clear Sky Science · pt
Estratificação de pacientes guiada pela matriz extracelular e modelagem de redes revelam graus moleculares distintos com possíveis implicações clínicas
Por que o entorno do tumor importa
Quando pensamos em câncer, frequentemente imaginamos células descontroladas crescendo sem freio. Mas essas células vivem em um bairro complexo feito de proteínas e açúcares que formam uma malha de suporte chamada matriz extracelular. Essa malha está longe de ser passiva. Ela pode enrijecer, engrossar e enviar sinais que ajudam os tumores a crescer ou a resistir ao tratamento. Neste estudo, os pesquisadores perguntaram se a composição dessa malha em tumores pulmonares poderia ser usada para classificar pacientes em grupos relevantes e orientar escolhas terapêuticas.
Classificando tumores pelo “andaime” estrutural
A equipe focou no adenocarcinoma de pulmão, um tipo comum de câncer pulmonar, e analisou 101 pacientes cujos tumores foram profundamente perfilados em níveis de DNA, RNA e proteína. Eles usaram uma lista curada de genes que constroem e regulam a matriz para criar um “código de barras ECM” para cada paciente. Esse código capturou o quanto a matriz de cada tumor diferia do tecido pulmonar normal próximo daquele paciente. Ao agrupar os pacientes usando esses códigos, surgiram quatro “graus ECM” distintos, variando de matriz quase semelhante à normal até tumores envolvidos por uma malha densa e complexa.
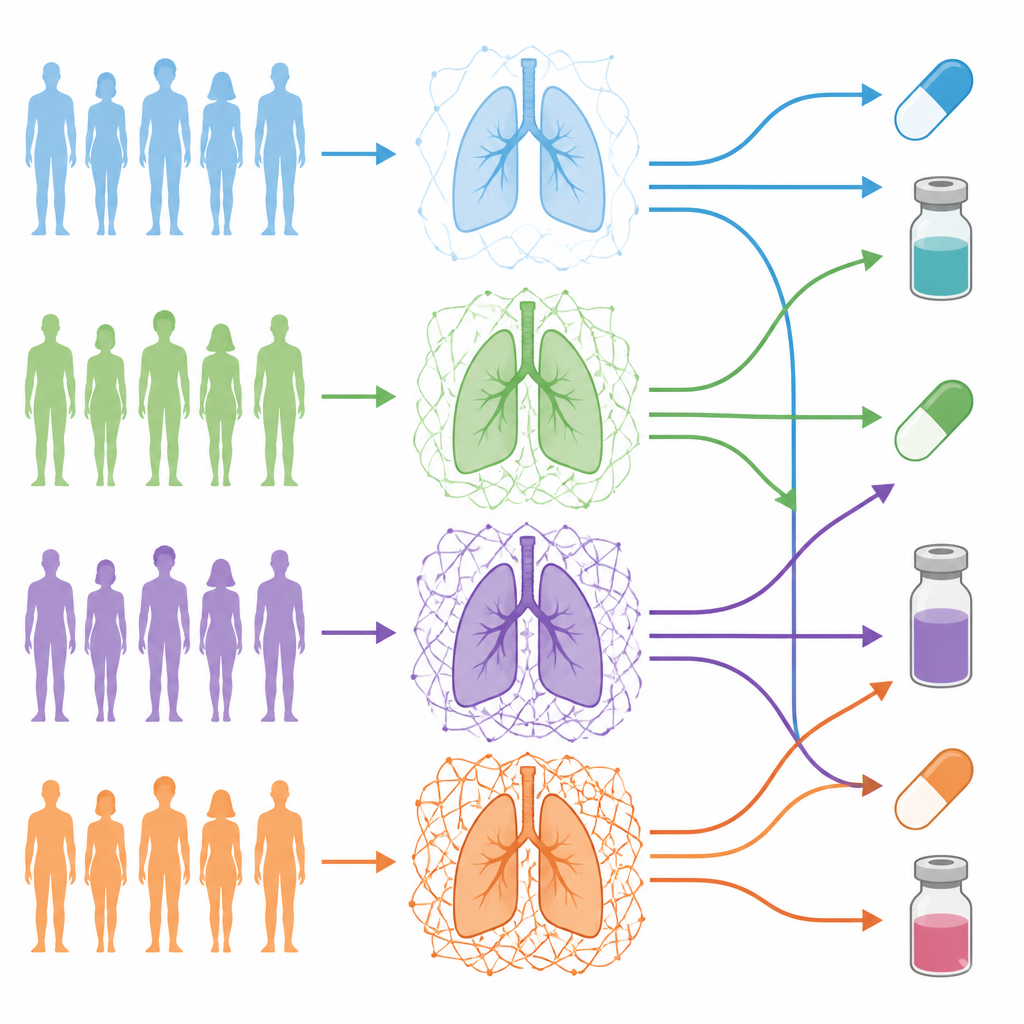
O que os graus altos e baixos revelam sobre o tumor
Os tumores com os graus ECM mais altos estavam repletos de células do estroma, como fibroblastos associados ao câncer, e tinham frações menores de células cancerígenas propriamente ditas — um padrão associado a microambientes tumorais mais avançados. Esses tumores ricos em ECM mostraram sinais mais fortes ligados à transição epitélio-mesenquimal, invasividade, células com características de células-tronco cancerosas e crescimento de vasos sanguíneos. Pacientes no grau ECM mais alto tendiam a ter características clínicas mais agressivas, mais mutações tumorais e maior risco de curto prazo de morte ou recidiva, em comparação com pacientes cujos tumores apresentavam matriz esparsa.
Fiação oculta entre a matriz e o comportamento celular
Para descobrir como a matriz externa se conecta ao comportamento interno das células, os pesquisadores construíram modelos de rede para cada paciente que ligavam proteínas de matriz alteradas às proteínas de sinalização e fatores de transcrição que elas influenciam. A combinação dessas redes mostrou que graus ECM mais elevados estavam associados a maior atividade em vias que regulam movimento celular, sobrevivência e adaptação ao estresse mecânico. Sinais que incentivam as células a afrouxarem suas adesões, migrar e invadir estavam mais ativos, enquanto fatores protetores que normalmente suprimem a invasão eram mais fracos em tumores ricos em ECM. O estudo também encontrou que certas mutações bem conhecidas do câncer, como em KRAS e EGFR, tendiam a aparecer em graus ECM diferentes, sugerindo que o ambiente da matriz e as alterações genéticas podem se reforçar mutuamente.
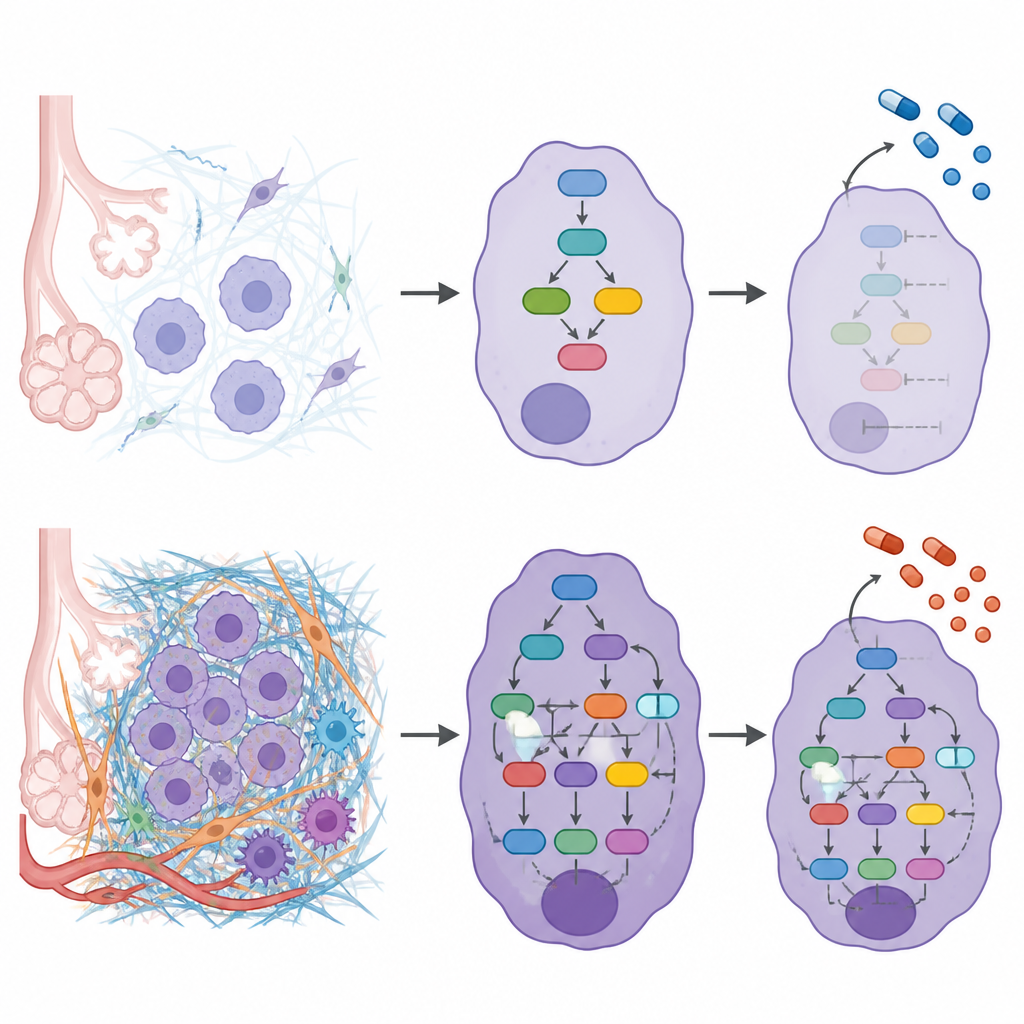
Ligando a matriz às escolhas de tratamento
Como a matriz pode moldar como os fármacos alcançam e afetam as células tumorais, a equipe em seguida investigou se diferentes graus ECM poderiam responder de forma distinta a medicamentos anticâncer existentes. Usando seus mapas de rede, eles mediram quão “próximos” os alvos de cada droga estavam dos hubs de sinalização dirigidos pela matriz em cada grau. Isso revelou medicamentos previstos como mais eficazes em cenários ECM específicos e outros provavelmente com ação semelhante entre os graus. Um fármaco que bloqueia enzimas de reparo de DNA, olaparibe, aparentou estar especialmente conectado aos graus ECM baixos, enquanto um medicamento direcionado ao EGFR, erlotinibe, mostrou-se amplamente eficaz independentemente do grau ECM.
Testando as previsões em laboratório
Os pesquisadores então recriaram versões simplificadas de ambientes ECM baixos e altos no laboratório usando linhas celulares de câncer de pulmão com mutações em KRAS ou EGFR. Eles cultivaram as células em matriz derivada de pulmão saudável para mimetizar um ambiente de baixo grau e em uma membrana basal parecida com a tumoral para mimetizar uma matriz mais rica. Em concordância com as previsões das redes, o olaparibe foi mais potente contra células com mutação em EGFR sobre a matriz de tipo saudável do que sobre a matriz tipo tumoral, enquanto seu efeito em células com mutação em KRAS não dependia muito da matriz. Em contraste, o erlotinibe reduziu a viabilidade celular em grau semelhante nas duas condições de matriz, correspondendo ao seu perfil ECM-insensível da análise em rede.
O que isso significa para os pacientes
Este trabalho sugere que o arcabouço de suporte do tumor não é apenas um pano de fundo, mas uma característica chave que pode ser medida, agrupada e ligada a como os tumores crescem e respondem a drogas. Ao classificar os cânceres de pulmão em graus ECM e mapear as redes de sinalização que conectam a matriz ao comportamento celular, os clínicos podem, no futuro, ser capazes de selecionar terapias que se ajustem tanto à composição genética do câncer quanto ao seu entorno físico. Embora sejam necessárias mais validações antes que essa abordagem possa orientar a prática clínica rotineira, ela aponta para um futuro em que a estrutura ao redor do tumor ajuda a decidir quais tratamentos têm maior probabilidade de funcionar.
Citação: Dansık, A., Sarıca, S., Öztürk, E. et al. Extracellular matrix-driven patient stratification and network modeling reveal distinct molecular grades with potential clinical implications. npj Syst Biol Appl 12, 66 (2026). https://doi.org/10.1038/s41540-026-00697-0
Palavras-chave: matriz extracelular, adenocarcinoma de pulmão, microambiente tumoral, redes do câncer, resposta a fármacos