Clear Sky Science · tr
Multimodal görüntüleme, PARP inhibitörlerinin düzensiz dağılımına yol açan lizozomal ilaç deposunu ortaya çıkardı
Bu araştırma kanser tedavisi için neden önemli
Birçok modern kanser ilacı son derece hedefe yönelik tasarlanmış olsa da bazı hastalarda başarısız olur. Az incelenmiş bir neden, ilaçların tek bir tümör içinde bile her kanser hücresinde aynı konsantrasyona ulaşmayabilmesidir. Bu makale, PARP inhibitörleri olarak bilinen ve yumurtalık kanserinde yaygın kullanılan üç ilacın tümörler ve bireysel hücreler içinde nasıl yayıldığını inceliyor ve hücre içindeki küçük geri dönüşüm bölmeleri olan lizozomların, tedavinin başarılı olup olmayacağını şekillendiren gizli bir ilaç deposu gibi davranabileceğini gösteriyor.
Aynı tümör içinde düzensiz ilaç düzeyleri
Araştırmacılar, agresif ve yüksek derecede değişken bir yumurtalık kanseri türü olan yüksek dereceli seröz over karsinomuna odaklandı. Cerrahiyle çıkarılan taze tümör örneklerini laboratuvarda ince dilimler halinde canlı tutup üç klinik PARP inhibitörü ile muamele ettiler. Gelişmiş kütle spektrometrisi görüntüleme ile ilaçların her dilim boyunca nerede biriktiğini görebildiler. Her bölge aynı doza maruz kalmış olmasına rağmen ilaç dağılımı çarpıcı biçimde düzensizdi – bazı alanlar ilaç “sıcak noktaları” iken yakındaki bölgelerde çok az ilaç vardı. Bu yamalı görünüm hastalar arasında, aynı hastadaki farklı tümörler arasında ve hatta tek bir tümör örneği içinde bile ortaya çıktı; bu da hücre içi özelliklerin her bölgenin ne kadar ilaç absorbe ettiğini güçlü biçimde etkilediğini düşündürüyor. 
İlaçça zengin bölgeler daha iyi yanıt veriyor ama hücresel bir ipucu açığa çıkıyor
Sıcak noktaları düşük ilaçlı bölgelerden ayıran özellikleri bulmak için ekip, doku düzenini korurken gen aktivitesini okuyan spatial transkriptomik teknolojisini kullandı. İki PARP inhibitörü (rucaparib ve niraparib) için yüksek ve düşük düzeyli bölgeleri karşılaştırdıklarında, ilaçça zengin alanların daha güçlü DNA hasarı, hücre döngüsü durağanlığı ve programlı hücre ölümü imzaları gösterdiğini buldular – bunlar bu ilaçların tetiklemesi beklenen etkilerdi. Aynı zamanda, yüksek-ilaç bölgeleri tutarlı şekilde lizozomlarla ilişkili daha fazla gen ifadesi gösteriyordu; lizozomlar hücresel atıkları parçalayan ve bileşenleri geri dönüştüren asidik bölmelerdir. Birden çok lizozom-ilişkili gen yerel ilaç yoğunluğu ile güçlü bir korelasyon sergiledi; bu da lizozomal içeriğin bir hücrenin ne kadar ilaç tutabileceğini ve ne kadar güçlü yanıt verebileceğini belirlemeye yardımcı olabileceğine işaret ediyor.
Tek tek hücrelerde genetik olmayan ilaç alım farkları
Daha yakından bakmak için bilim insanları kültürde yetiştirilen over kanseri hücre hatlarına yöneldi. İlaçlardan biri olan rucaparib mikroskop altında parıldıyor ve binlerce bireysel hücre içinde seviyesini ölçmelerine olanak verdi. Tüm hücreler aynı konsantrasyona maruz kalmasına rağmen en yüksek ve en düşük biriktiren hücreler arasında hücre içi ilaç sinyalinde beş kata kadar fark görüldü. En parlak ve en sönük hücreleri ayırıp birkaç hafta büyüttüklerinde bu farkların genetik olarak sabit olmadığını; zamanla popülasyonların benzer bir dağılıma geri döndüğünü gösterdiler. Bu, organel içeriği veya metabolik durum gibi genetik olmayan faktörlerin ilaç alımındaki çeşitliliğin temelini oluşturduğunu düşündürüyor.
Lizozomlar nasıl faydalı bir ilaç deposu haline geliyor
Yüksek ve düşük rucaparib düzeyine sahip hücrelerin proteomik analizleri, yüksek-ilaç hücrelerinin lizozomal proteinler bakımından zengin olduğunu gösterdi. Görüntüleme, rucaparib’in hızla hücreye girdiğini ve ardından lizozoma özgü boyalarla örtüşen noktasal yapılarda biriktiğini doğruladı. Daha fazla lizozomal sinyal gösteren hücreler daha fazla hücre içi ilaca sahipti ve lizozomları manipüle etmek ilaç düzeylerini değiştirdi: lizozom oluşumunu veya asitlenmesini artırmak rucaparib birikimini yükseltirken, lizozomal asitliği nötralize etmek onu azalttı. Önemli olarak, ilaç zararsız bir şekilde hapsedilmiş değildi. Lizozomca zengin hücrelerde tedavi sonrası daha fazla DNA hasarı ve daha yavaş büyüme görüldü; lizozomal işlev bozukluğu kısa bir maruziyetten sonra nükleer ilaç seviyelerini düşürdü ve ilacın uzun vadeli öldürücü etkisini zayıflattı. 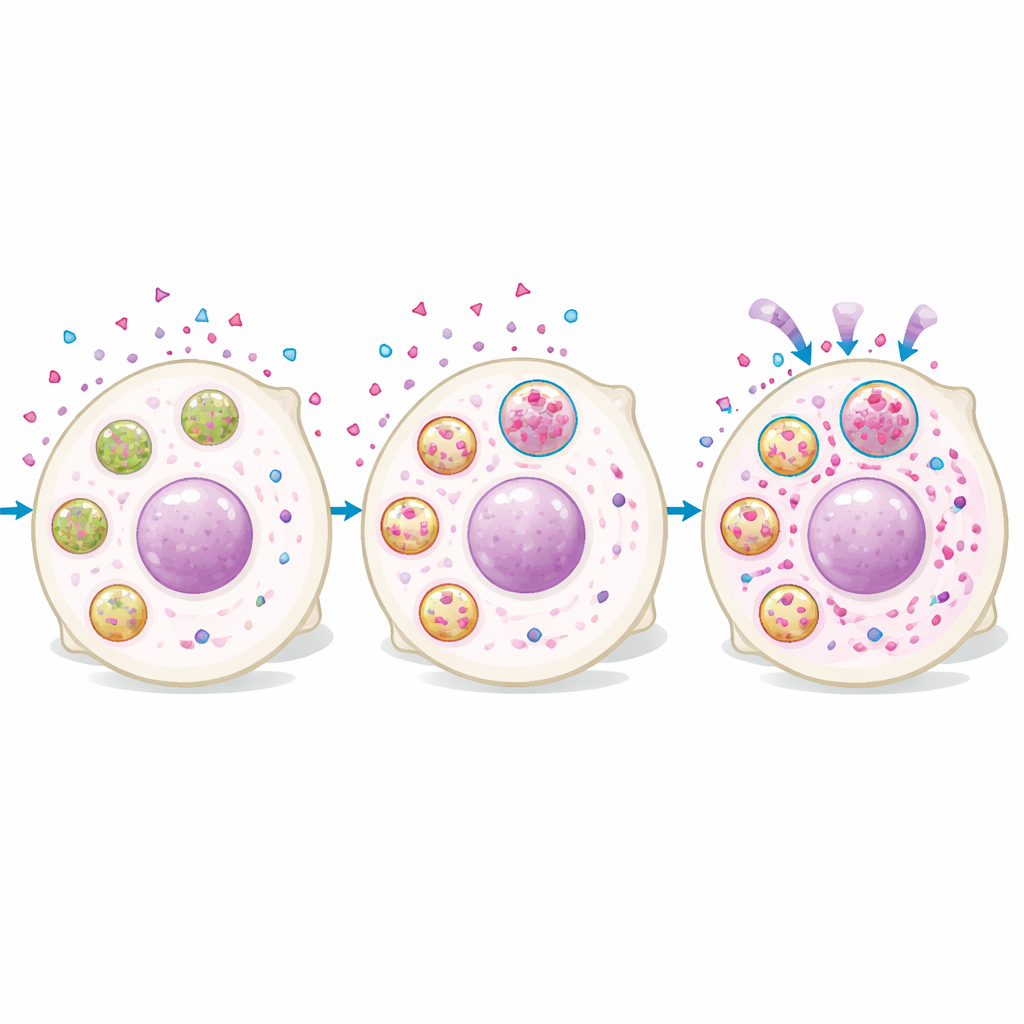
Neden yalnızca bazı PARP ilaçları bu şekilde davranıyor
Tüm PARP inhibitörleri aynı davranmadı. Rucaparib ve niraparib zayıf baziktir; bu, lizozomların asidik ortamında yüklü hale gelip zarları geçme yeteneklerini azaltır ve bu ortamlarda birikmelerini kolaylaştırır. Diğer yaygın kullanılan bir PARP inhibitörü olan olaparib ise çok farklı kimyasal özelliklere sahipti ve bu tür pH-bağımlı lizozomal birikim göstermedi. Ekip ilaç içeriğini kütle spektrometrisi ile ölçtüğünde, lizozomları nötralize etmek rucaparib ve niraparib’in hücre içi düzeylerini azalttı fakat olaparib’i etkilemedi. Benzer şekilde, lizozomal içeriği değiştirmek yalnızca zayıf baz ilaçlara yönelik DNA hasarı yanıtını değiştirdi, olaparib’e değil. Bu, tümörü doğal olarak daha fazla lizozoma sahip olan hastaların bazı PARP inhibitörlerine diğerlerine göre daha iyi yanıt verebileceğini düşündürüyor.
Bu hastalar ve gelecekteki tedaviler için ne anlama geliyor
Bu çalışma, kanser hücrelerindeki lizozomların ölü bir tuzak değil, belirli ilaçları depolayan ve onları etki ettikleri yere —bu durumda çekirdeğe— yavaşça geri veren bir depo işlevi görebileceğini ortaya koyuyor. Tümörler yüksek derecede heterojen olduğundan, çok sayıda lizozoma sahip bölgeler belirli PARP inhibitörlerini daha fazla biriktirerek yerel olarak kanser hücrelerinin daha iyi öldürülmesine yol açabilirken, yakınlardaki daha az lizozoma sahip bölgeler aynı tedaviye rağmen düşük doz alıyor olabilir. Pratik açıdan, bu çalışma bir ilacın kimyasal özelliklerini hastanın tümörünün hücresel yapısı —örneğin lizozomal içeriği— ile eşleştirmenin yanıtları iyileştirip görünen ilaç direncinin bazı vakalarını aşabileceğini öne sürüyor. Ayrıca küçük tümör örneklerinin ex vivo test edilerek hangi ilacın her birey için en iyi dağılımı sağlayıp etkili olacağını belirlemeye yönelik gelecekteki tanı stratejilerine de işaret ediyor.
Atıf: R. Moncayo, C., Restuadi, R., Zhang, G. et al. Multimodal imaging reveals a lysosomal drug reservoir that drives heterogeneous distribution of PARP inhibitors. Nat Commun 17, 4086 (2026). https://doi.org/10.1038/s41467-026-70558-1
Anahtar kelimeler: over kanseri, PARP inhibitörleri, lizozomlar, ilaç direnci, tümör heterojenitesi