Clear Sky Science · pt
Imagem multimodal revela um reservatório lisossomal de fármaco que dirige a distribuição heterogênea de inibidores de PARP
Por que esta pesquisa importa para o tratamento do câncer
Muitos medicamentos modernos para câncer são projetados com precisão, mas ainda falham em alguns pacientes. Uma razão pouco explorada é que os fármacos podem não atingir a mesma concentração dentro de todas as células tumorais, mesmo dentro de um único tumor. Este artigo investiga como três fármacos amplamente usados no câncer de ovário, chamados inibidores de PARP, se distribuem por tumores e células individuais, e revela que pequenos compartimentos de reciclagem dentro das células, conhecidos como lisossomos, podem agir como um reservatório oculto de fármaco que determina se o tratamento terá sucesso ou fracassará.
Níveis desiguais de fármaco dentro do mesmo tumor
Os pesquisadores focalizaram no carcinoma seroso de alto grau do ovário, uma forma agressiva e altamente variável de câncer de ovário. Usando amostras tumorais frescas removidas durante cirurgia, mantiveram fatias finas do tecido do paciente vivas no laboratório e as incubaram com três inibidores de PARP usados clinicamente. Com espectrometria de massa por imagem avançada, puderam visualizar onde os fármacos se acumulavam em cada fatia. Mesmo que todas as regiões tenham sido expostas à mesma dose, a distribuição do fármaco foi marcadamente desigual – algumas áreas eram "pontos quentes" de fármaco enquanto zonas próximas tinham muito pouco. Essa irregularidade apareceu entre diferentes pacientes, entre tumores distintos no mesmo paciente e até dentro de uma única amostra tumoral, sugerindo que propriedades intrínsecas das células influenciam fortemente quanto fármaco cada região absorve. 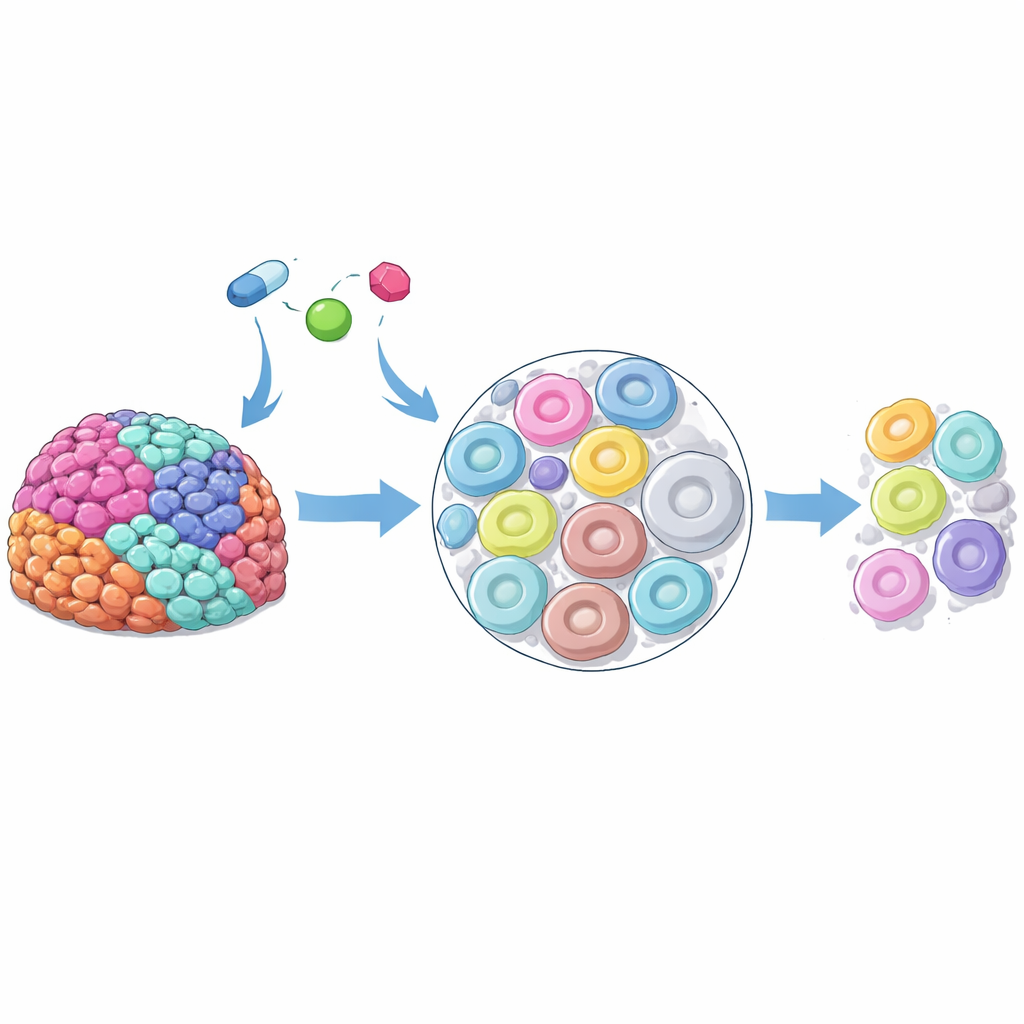
Regiões ricas em fármaco respondem melhor, mas revelam uma pista celular
Para descobrir o que distinguia os pontos quentes das regiões pobres em fármaco, a equipe usou transcriptômica espacial, uma tecnologia que lê a atividade gênica preservando a organização tecidual. Comparando regiões com níveis altos e baixos de dois inibidores de PARP (rucaparibe e niraparibe), encontraram que as áreas ricas em fármaco exibiam assinaturas mais fortes de dano ao DNA, parada do ciclo celular e morte programada – exatamente o que esses fármacos devem induzir. Ao mesmo tempo, essas regiões com alto teor de fármaco expressaram, de forma consistente, mais genes associados a lisossomos, os compartimentos ácidos que digerem resíduos celulares e reciclam componentes. Vários genes ligados aos lisossomos mostraram correlação estreita com a concentração local do fármaco, sugerindo que diferenças no conteúdo lisossomal podem ajudar a determinar quanto fármaco uma célula pode reter e quão fortemente ela responde.
Células individuais mostram diferenças não genéticas na captação de fármaco
Para ampliar a análise, os cientistas recorreram a linhagens de câncer de ovário cultivadas em cultura. Um dos fármacos, rucaparibe, fluoresce ao microscópio, permitindo medir seu nível dentro de milhares de células individuais. Eles observaram até cinco vezes de diferença no sinal intracelular entre as células que mais e as que menos acumulavam o fármaco, mesmo todas expostas à mesma concentração. Separar as células mais brilhantes e as mais fracas e cultivá-las por várias semanas mostrou que essas diferenças não eram fixas por genética: com o tempo, as populações voltaram a uma distribuição semelhante. Isso sugere que fatores não genéticos — como conteúdo variável de organelas ou estado metabólico — explicam a diversidade na captação do fármaco.
Como os lisossomos se tornam um reservatório útil de fármaco
Análises proteômicas de células com níveis altos versus baixos de rucaparibe mostraram que as células com mais fármaco eram enriquecidas em proteínas lisossomais. Imagens confirmaram que o rucaparibe entra rapidamente nas células e então se acumula em estruturas pontuais que se sobrepõem a corantes específicos de lisossomos. Células com maior sinal lisossomal apresentaram mais fármaco intracelular, e manipular os lisossomos alterou os níveis de fármaco: aumentar a biogênese lisossomal ou a acidificação elevou o acúmulo de rucaparibe, enquanto neutralizar a acidez lisossomal o reduziu. Importante, o fármaco não permanecia inofensivamente preso. Células ricas em lisossomos apresentaram mais dano ao DNA e crescimento mais lento após o tratamento, e complicar a função lisossomal diminuiu os níveis nucleares do fármaco e enfraqueceu o efeito letal de longo prazo do fármaco após uma exposição curta. 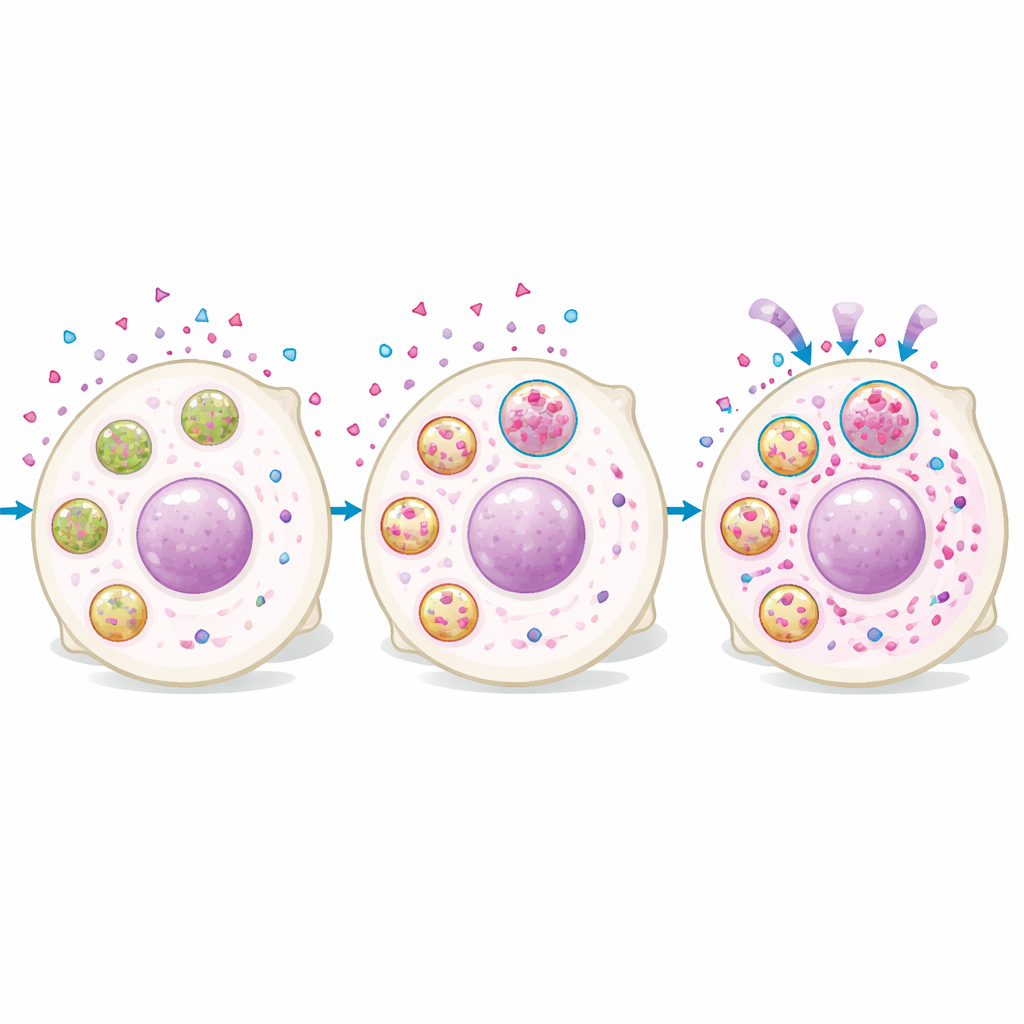
Por que apenas alguns inibidores de PARP se comportam assim
Nem todos os inibidores de PARP se comportaram da mesma forma. Rucaparibe e niraparibe são bases fracas, o que significa que ganham carga e se tornam menos capazes de atravessar membranas no ambiente ácido dos lisossomos, favorecendo seu acúmulo ali. Outro inibidor de PARP amplamente usado, olaparibe, tem propriedades químicas muito diferentes e não mostrou esse tipo de acúmulo lisossomal dependente do pH. Quando a equipe mediu o conteúdo de fármaco por espectrometria de massa, neutralizar os lisossomos reduziu os níveis intracelulares de rucaparibe e niraparibe, mas deixou o olaparibe inalterado. Da mesma forma, alterar o conteúdo lisossomal só modificou a resposta ao dano de DNA dos fármacos base fraca, não a do olaparibe. Isso implica que pacientes cujos tumores naturalmente têm mais lisossomos poderiam responder melhor a alguns inibidores de PARP do que a outros.
O que isso significa para pacientes e terapias futuras
Este estudo revela que lisossomos em células cancerosas podem agir não como uma armadilha sem saída, mas como um reservatório que armazena certos fármacos e os libera lentamente para onde atuam, neste caso o núcleo. Como os tumores são altamente heterogêneos, regiões com muitos lisossomos podem acumular mais determinados inibidores de PARP, levando a maior morte local das células cancerosas, enquanto regiões próximas com menos lisossomos podem ficar subdosadas apesar de receberem o mesmo tratamento. Em termos práticos, este trabalho sugere que casar as propriedades químicas de um fármaco com a composição celular do tumor do paciente — como o conteúdo lisossomal — poderia melhorar respostas e superar alguns casos de aparente resistência a fármacos. Também aponta para estratégias diagnósticas futuras em que pequenas amostras tumorais são testadas ex vivo para identificar qual fármaco irá se distribuir e funcionar melhor para cada indivíduo.
Citação: R. Moncayo, C., Restuadi, R., Zhang, G. et al. Multimodal imaging reveals a lysosomal drug reservoir that drives heterogeneous distribution of PARP inhibitors. Nat Commun 17, 4086 (2026). https://doi.org/10.1038/s41467-026-70558-1
Palavras-chave: câncer de ovário, inibidores de PARP, lisossomos, resistência a fármacos, heterogeneidade tumoral