Clear Sky Science · sv
Multimodal avbildning avslöjar ett lysosomalt läkemedelsförråd som driver heterogen fördelning av PARP-hämmare
Varför denna forskning är viktig för cancerbehandling
Många moderna cancerläkemedel är utformade med stor precision, men misslyckas ändå för vissa patienter. En underutforskad anledning är att läkemedel kanske inte når samma koncentration inne i varje cancercell, även inom en enda tumör. Denna artikel undersöker hur tre allmänt använda läkemedel mot äggstockscancer, så kallade PARP‑hämmare, sprids genom tumörer och enskilda celler, och visar att små återvinningskompartiment i celler, kända som lysosomer, kan fungera som ett dolt läkemedelsförråd som påverkar om behandlingen lyckas eller misslyckas.
Ojämna läkemedelsnivåer inom samma tumör
Forskarna fokuserade på höggradigt seröst äggstockscarcinom, en aggressiv och mycket varierande form av äggstockscancer. Med färska tumörprover borttagna under operation höll de tunna skivor av patientvävnad vid liv i laboratoriet och exponerade dem för tre kliniskt använda PARP‑hämmare. Med avancerad masspektrometriavbildning kunde de se var läkemedlen samlades i varje skiva. Trots att varje region utsattes för samma dos var läkemedelsfördelningen slående ojämn – vissa områden var läkemedels"hotspots" medan närliggande zoner hade väldigt lite. Denna fläckighet syntes mellan olika patienter, mellan olika tumörer hos samma patient och till och med inom ett enda tumörprov, vilket tyder på att cellinterna egenskaper starkt påverkar hur mycket läkemedel varje område absorberar. 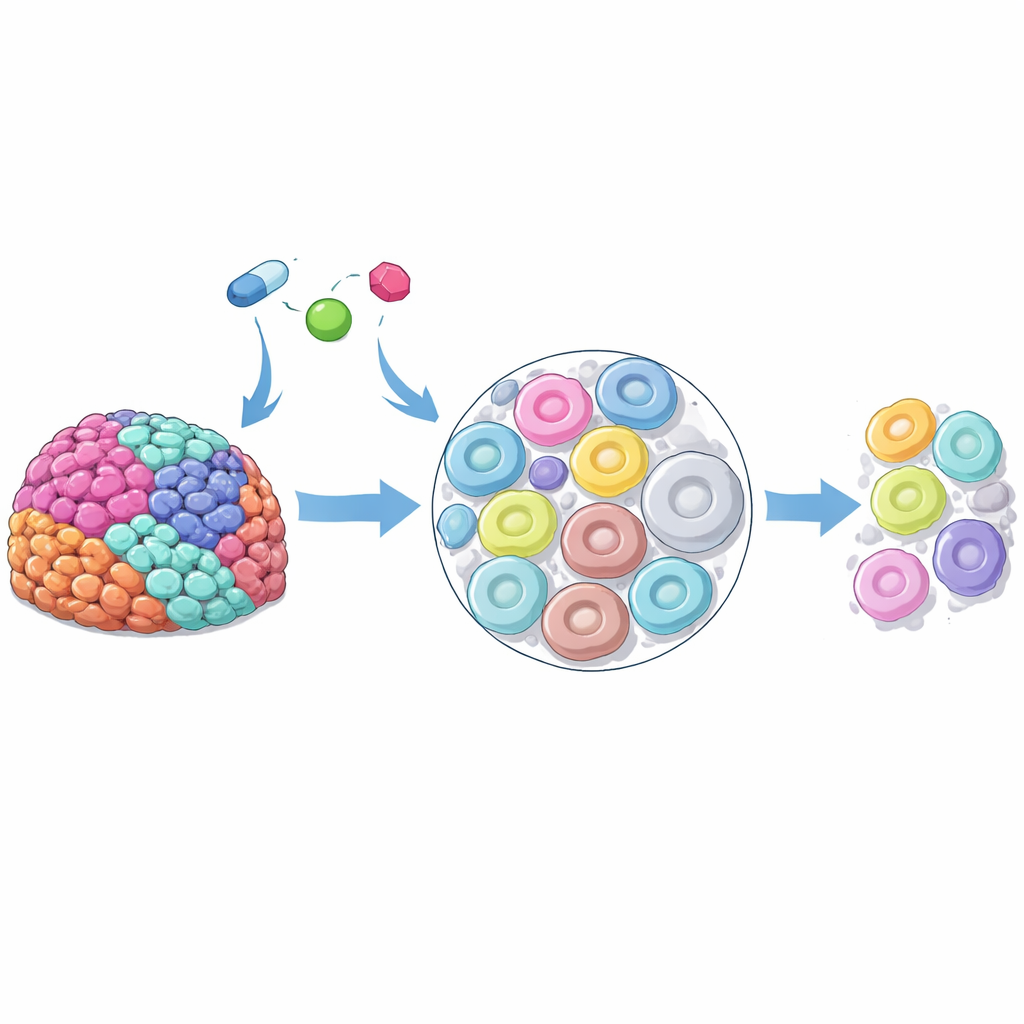
Läkemedelsrika regioner svarar bättre men avslöjar en cellulär ledtråd
För att ta reda på vad som utmärkte hotspots från regioner med låg läkemedelsnivå använde teamet spatial transkriptomik, en teknik som läser genaktivitet samtidigt som vävnadens layout bevaras. Jämförelser mellan regioner med höga respektive låga nivåer av två PARP‑hämmare (rucaparib och niraparib) visade att läkemedelsrika områden uppvisade starkare tecken på DNA‑skada, cellcykelstopp och programmerad celldöd – precis det dessa läkemedel är avsedda att utlösa. Samtidigt uttryckte dessa hög‑läkemedelsregioner konsekvent fler gener kopplade till lysosomer, de sura kompartimenten som bryter ner cellulärt avfall och återvinner komponenter. Flera lysosom‑associerade gener visade en tydlig korrelation med lokal läkemedelskoncentration, vilket antyder att skillnader i lysosominnehåll kan bidra till hur mycket läkemedel en cell kan hålla och hur starkt den svarar.
Enskilda celler visar icke‑genetiska skillnader i läkemedelsupptag
För att zooma in ytterligare riktade forskarna in sig på äggstockscellinjer odlade i kultur. Ett av läkemedlen, rucaparib, fluorescerar under mikroskop, vilket gjorde det möjligt för dem att mäta dess nivå i tusentals enskilda celler. De såg upp till fem gånger skillnad i intracellulär läkemedelssignal mellan de celler som ackumulerade mest respektive minst, trots att alla exponerats för samma koncentration. Genom att sortera ut de mest lysande och svagaste cellerna och odla dem i flera veckor visade det sig att dessa skillnader inte var permanent fastlagda av genetik: över tid återgick populationerna till en liknande fördelning. Detta tyder på att icke‑genetiska faktorer – såsom varierande organellinnehåll eller metabolt tillstånd – ligger bakom mångfalden i läkemedelsupptag.
Hur lysosomer blir ett användbart läkemedelsförråd
Proteomiska analyser av celler med höga respektive låga rucaparib‑nivåer visade att de hög‑läkemedelscellernas proteom var rikt på lysosomala proteiner. Avbildning bekräftade att rucaparib snabbt tog sig in i cellerna och sedan ackumulerades i punktlika strukturer som överlappade med lysosomspecifika färgningar. Celler med starkare lysosomsignal hade mer intracellulärt läkemedel, och att manipulera lysosomer förändrade läkemedelsnivåerna: att öka lysosombildning eller surhetsgrad ökade rucaparib‑ackumuleringen, medan neutralisering av lysosomernas surhet minskade den. Viktigt är att läkemedlet inte förblev ofarligt instängt. Lysosom‑rika celler hade mer DNA‑skador och långsammare tillväxt efter behandling, och att störa lysosomfunktionen sänkte nukleära läkemedelsnivåer och försvagade läkemedlets långsiktiga dödande effekt efter en kort exponering.
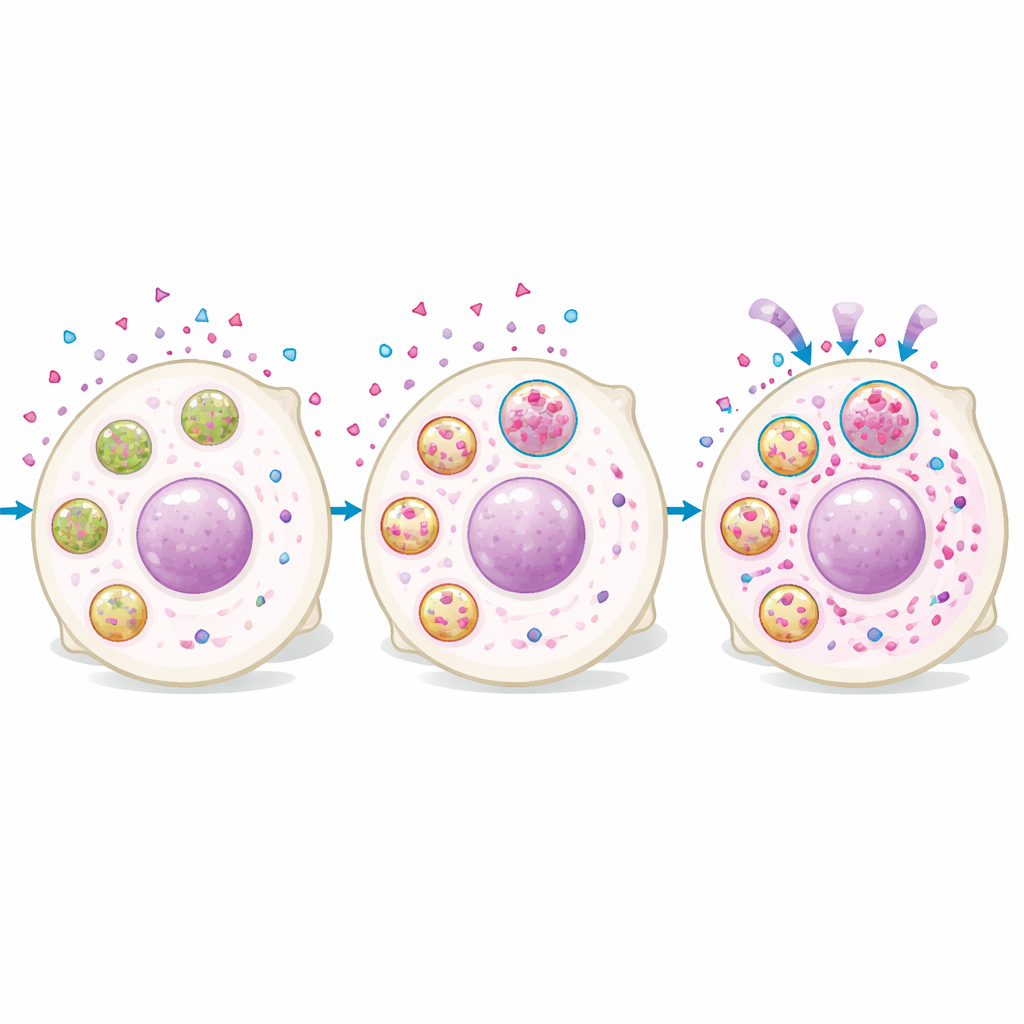
Varför endast vissa PARP‑läkemedel beter sig så här
Inte alla PARP‑hämmare uppvisade samma beteende. Rucaparib och niraparib är svaga baser, vilket innebär att de tar upp laddning och blir mindre benägna att korsa membraner i lysosomernas sura miljö, vilket gynnar deras ansamling där. En annan ofta använd PARP‑hämmare, olaparib, har mycket annorlunda kemiska egenskaper och visade inte denna typ av pH‑beroende lysosomal ackumulering. När teamet mätte läkemedelsinnehåll med masspektrometri minskade neutralisering av lysosomer de intracellulära nivåerna av rucaparib och niraparib men lämnade olaparib oförändrad. På motsvarande sätt påverkade ändringar i lysosominnehåll endast DNA‑skaderesponsen till de svaga baserna, inte till olaparib. Detta antyder att patienter vars tumörer naturligt har fler lysosomer kan svara bättre på vissa PARP‑hämmare än på andra.
Vad detta betyder för patienter och framtida terapier
Denna studie visar att lysosomer i cancerceller kan fungera inte som en återvändsgränd utan som ett förråd som lagrar vissa läkemedel och långsamt för dem tillbaka till där de verkar, i detta fall i kärnan. Eftersom tumörer är mycket heterogena kan regioner med många lysosomer ackumulera mer av specifika PARP‑hämmare, vilket leder till bättre lokalt utplånande av cancerceller, medan närliggande regioner med färre lysosomer kan bli underdoserade trots att de får samma behandling. I praktiska termer antyder detta arbete att anpassning av ett läkemedels kemiska egenskaper till den cellulära sammansättningen i en patients tumör – till exempel lysosominnehåll – skulle kunna förbättra responsen och övervinna vissa fall av upplevd läkemedelsresistens. Det pekar också mot framtida diagnostiska strategier där små tumörprover testas ex vivo för att identifiera vilket läkemedel som kommer att fördelas och fungera bäst för varje individ.
Citering: R. Moncayo, C., Restuadi, R., Zhang, G. et al. Multimodal imaging reveals a lysosomal drug reservoir that drives heterogeneous distribution of PARP inhibitors. Nat Commun 17, 4086 (2026). https://doi.org/10.1038/s41467-026-70558-1
Nyckelord: äggstockscancer, PARP-hämmare, lysosomer, läkemedelsresistens, tumörheterogenitet