Clear Sky Science · de
Multimodale Bildgebung zeigt ein lysosomales Arzneimittel-Reservoir, das die heterogene Verteilung von PARP-Inhibitoren antreibt
Warum diese Forschung für die Krebsbehandlung wichtig ist
Viele moderne Krebstherapien sind hochpräzise entwickelt, versagen jedoch dennoch bei einigen Patientinnen und Patienten. Ein wenig untersuchter Grund dafür ist, dass Arzneimittel nicht in jeder Krebszelle dieselbe Konzentration erreichen, selbst innerhalb eines einzigen Tumors. Diese Studie untersucht, wie drei weit verbreitete PARP-Inhibitoren bei Eierstockkrebs sich durch Tumoren und einzelne Zellen verteilen, und zeigt, dass winzige Recycling-Kompartimente in Zellen, sogenannte Lysosomen, als verstecktes Arzneimittelreservoir wirken können, das darüber mitbestimmt, ob eine Behandlung erfolgreich ist oder nicht.
Ungleichmäßige Arzneimittelspiegel innerhalb desselben Tumors
Die Forschenden konzentrierten sich auf das high-grade seröse Ovarialkarzinom, eine aggressive und sehr variable Form von Eierstockkrebs. Sie entnahmen frische Tumorproben während Operationen, hielten dünne Gewebeschnitte im Labor lebensfähig und setzten sie drei klinisch eingesetzten PARP-Inhibitoren aus. Mit fortschrittlicher Massenspektrometrie-Bildgebung konnten sie sehen, wo sich die Medikamente in den Schnitten anreicherten. Obwohl alle Bereiche derselben Dosis ausgesetzt waren, war die Arzneimittelverteilung auffallend ungleich – einige Areale waren Arzneimittel-„Hotspots“, während benachbarte Zonen nur sehr wenig enthielten. Diese Fleckenbildung zeigte sich zwischen verschiedenen Patientinnen, zwischen unterschiedlichen Tumoren derselben Patientin und sogar innerhalb einer einzelnen Tumorprobe, was darauf hindeutet, dass zellintrinsische Eigenschaften stark beeinflussen, wie viel Arzneimittel ein Bereich aufnimmt. 
Arzneimittelreiche Regionen sprechen besser an, geben aber einen zellulären Hinweis
Um herauszufinden, was Hotspots von Bereichen mit wenig Arzneimittel unterscheidet, nutzte das Team räumliche Transkriptomik, eine Methode, die Genaktivität bei erhaltener Gewebeanordnung liest. Beim Vergleich von Regionen mit hohen versus niedrigen Konzentrationen zweier PARP-Inhibitoren (rucaparib und niraparib) fanden sie, dass arzneimittelreiche Areale stärkere Signaturen von DNA-Schaden, Zellzyklusstopp und programmierter Zelltod zeigten – genau die Effekte, die diese Medikamente auslösen sollen. Gleichzeitig exprimierten diese hoch belasteten Regionen beständig mehr Gene, die mit Lysosomen verknüpft sind, den sauren Kompartimenten, die zellulären Abfall abbauen und Komponenten recyceln. Mehrere lysosomassoziierte Gene korrelierten eng mit der lokalen Arzneimittelkonzentration, was nahelegt, dass Unterschiede im Lysosomengehalt mitbestimmen könnten, wie viel Arzneimittel eine Zelle aufnehmen und wie stark sie reagiert.
Einzelne Zellen zeigen nicht-genetische Unterschiede in der Arzneimittelaufnahme
Um noch genauer hinzusehen, arbeiteten die Forschenden mit in Kultur gezüchteten Eierstockkrebs-Zelllinien. Eines der Medikamente, rucaparib, fluoresziert unter dem Mikroskop, sodass sie seine Menge in Tausenden einzelner Zellen messen konnten. Sie beobachteten bis zu fünffache Unterschiede im intrazellulären Arzneimittelsignal zwischen Zellen mit der höchsten und der niedrigsten Anreicherung, obwohl alle derselben Exposition ausgesetzt waren. Die Sortierung der hellsten und dunkelsten Zellen und deren anschließendes Wachstum über mehrere Wochen zeigte, dass diese Unterschiede nicht genetisch fixiert waren: Mit der Zeit kehrten die Populationen zu einer ähnlichen Verteilung zurück. Das deutet darauf hin, dass nicht-genetische Faktoren – etwa unterschiedliche Organellenausstattung oder metabolische Zustände – der Vielfalt in der Arzneimittelaufnahme zugrunde liegen.
Wie Lysosomen ein nützliches Arzneimittelreservoir werden
Proteomische Analysen von Zellen mit hohen versus niedrigen Rucaparib-Spiegeln zeigten, dass Zellen mit hoher Arzneimittelbelastung in Lysosomenproteine angereichert waren. Bildgebende Verfahren bestätigten, dass Rucaparib schnell in Zellen eindringt und sich dann in punktförmigen Strukturen anreichert, die mit lysosomspezifischen Farbstoffen überlappen. Zellen mit stärkerem lysosomalen Signal enthielten mehr intrazelluläres Arzneimittel, und die gezielte Beeinflussung der Lysosomen veränderte die Arzneimittelmenge: Die Förderung von Lysosomenbildung oder -ansäuerung erhöhte die Rucaparib-Anreicherung, während die Neutralisierung der Lysosomenazidität sie verringerte. Wichtig ist, dass das Arzneimittel nicht harmlos gefangen blieb. Lysosomreiche Zellen zeigten nach Behandlung mehr DNA-Schaden und langsameres Wachstum, und die Störung der Lysosomenfunktion senkte die zellkernnahe Arzneimittelmenge und schwächte die langfristige tödliche Wirkung des Medikaments nach einer kurzen Expositionspuls.
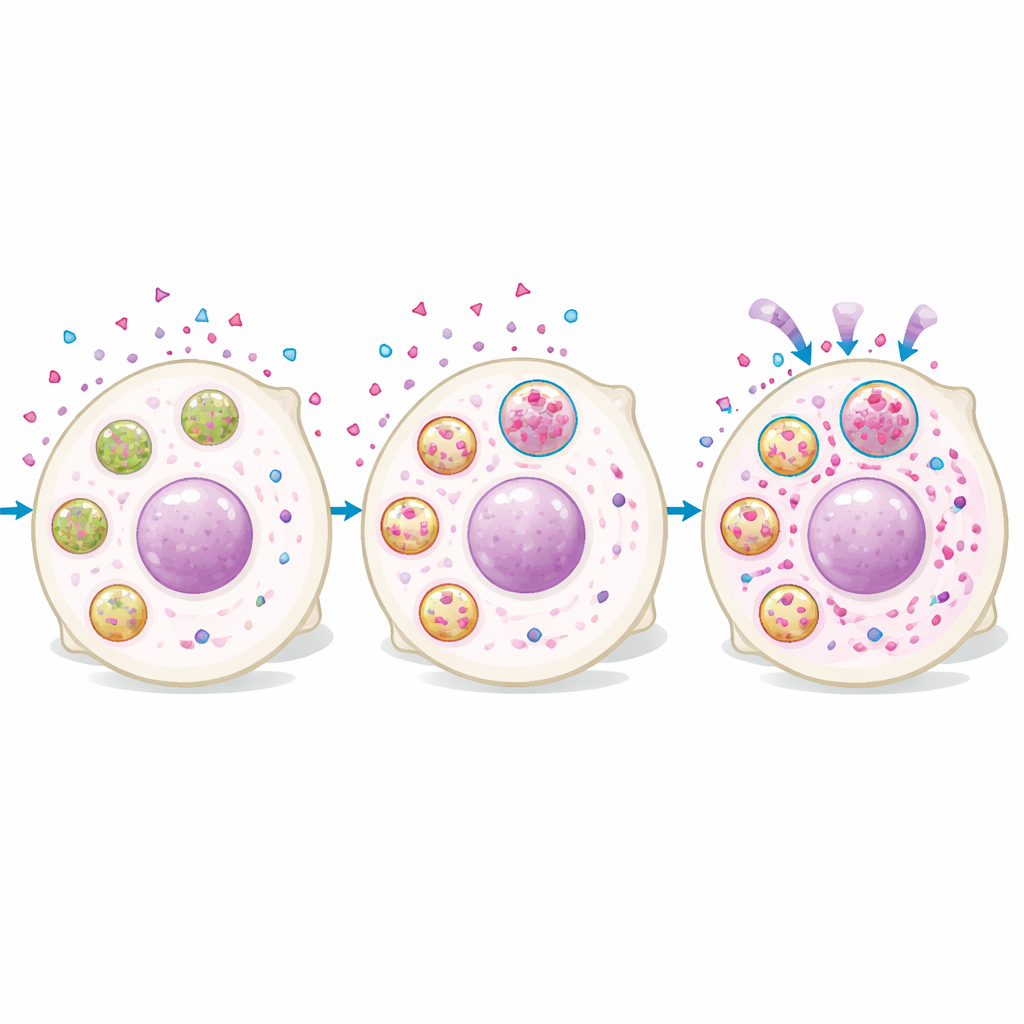
Warum nur einige PARP-Wirkstoffe sich so verhalten
Nicht alle PARP-Inhibitoren zeigten dasselbe Verhalten. Rucaparib und niraparib sind schwache Basen, das heißt, sie nehmen in saurer Umgebung eine Ladung an und werden dadurch weniger membranegängig, was ihre Anreicherung in Lysosomen begünstigt. Ein anderer weit verbreiteter PARP-Inhibitor, Olaparib, hat sehr unterschiedliche chemische Eigenschaften und zeigte keine solche pH‑abhängige lysosomale Akkumulation. Als das Team die Arzneimittelgehalte per Massenspektrometrie maß, reduzierte die Neutralisation der Lysosomen die intrazellulären Konzentrationen von rucaparib und niraparib, ließ Olaparib jedoch unverändert. Ebenso veränderte die Modulation des Lysosomengehalts nur die DNA-Schadensantwort auf die schwach basischen Wirkstoffe, nicht jedoch auf Olaparib. Das legt nahe, dass Patientinnen oder Patienten, deren Tumoren von Natur aus mehr Lysosomen enthalten, auf manche PARP-Inhibitoren besser ansprechen könnten als auf andere.
Was das für Patientinnen, Patienten und künftige Therapien bedeutet
Die Studie zeigt, dass Lysosomen in Krebszellen nicht einfach ein Sackgassenfallen sind, sondern als Reservoir dienen können, das bestimmte Medikamente speichert und langsam dorthin zurückführt, wo sie wirken – in diesem Fall in den Zellkern. Da Tumoren hoch heterogen sind, können Regionen mit vielen Lysosomen mehr bestimmter PARP-Inhibitoren anreichern und so lokal eine bessere Abtötung von Krebszellen bewirken, während benachbarte Regionen mit weniger Lysosomen trotz gleicher Behandlung unterversorgt sein können. Praktisch bedeutet dies, dass das Abgleichen der chemischen Eigenschaften eines Medikaments mit der zellulären Zusammensetzung des Tumors einer Patientin oder eines Patienten – etwa dem Lysosomengehalt – die Ansprechraten verbessern und einige Fälle scheinbarer Arzneimittelresistenz überwinden könnte. Zudem weist die Arbeit in Richtung diagnostischer Strategien, bei denen kleine Tumorproben ex vivo getestet werden, um zu ermitteln, welches Medikament sich am besten verteilt und am wirksamsten ist.
Zitation: R. Moncayo, C., Restuadi, R., Zhang, G. et al. Multimodal imaging reveals a lysosomal drug reservoir that drives heterogeneous distribution of PARP inhibitors. Nat Commun 17, 4086 (2026). https://doi.org/10.1038/s41467-026-70558-1
Schlüsselwörter: Eierstockkrebs, PARP-Inhibitoren, Lysosomen, Arzneimittelresistenz, Tumorheterogenität