Clear Sky Science · es
Imágenes multimodales revelan un reservorio lisosomal de fármaco que condiciona la distribución heterogénea de inhibidores de PARP
Por qué esta investigación importa para el tratamiento del cáncer
Muchos fármacos oncológicos modernos se diseñan con gran especificidad, pero aún así fallan en algunos pacientes. Una razón poco explorada es que los fármacos pueden no alcanzar la misma concentración dentro de cada célula tumoral, incluso dentro de un único tumor. Este artículo investiga cómo tres fármacos ampliamente usados contra el cáncer de ovario, conocidos como inhibidores de PARP, se distribuyen por los tumores y las células individuales, y revela que pequeños compartimentos de reciclaje dentro de las células, los lisosomas, pueden actuar como un reservorio oculto de fármaco que determina si el tratamiento funciona o fracasa.
Niveles desiguales de fármaco dentro del mismo tumor
Los investigadores se centraron en el carcinoma seroso de alto grado de ovario, una forma agresiva y altamente variable de cáncer de ovario. Usando muestras tumorales frescas extraídas durante la cirugía, mantuvieron finas secciones de tejido del paciente viables en el laboratorio y las expusieron a tres inhibidores de PARP utilizados clínicamente. Con imágenes avanzadas por espectrometría de masas pudieron observar dónde se acumulaban los fármacos en cada sección. Aunque todas las regiones recibieron la misma dosis, la distribución fue sorprendentemente desigual: algunas áreas eran "puntos calientes" de fármaco mientras que zonas cercanas tenían muy poco. Esta irregularidad apareció entre distintos pacientes, entre tumores diferentes en el mismo paciente e incluso dentro de una sola muestra tumoral, lo que sugiere que propiedades intrínsecas de las células influyen fuertemente en cuánto fármaco absorbe cada región. 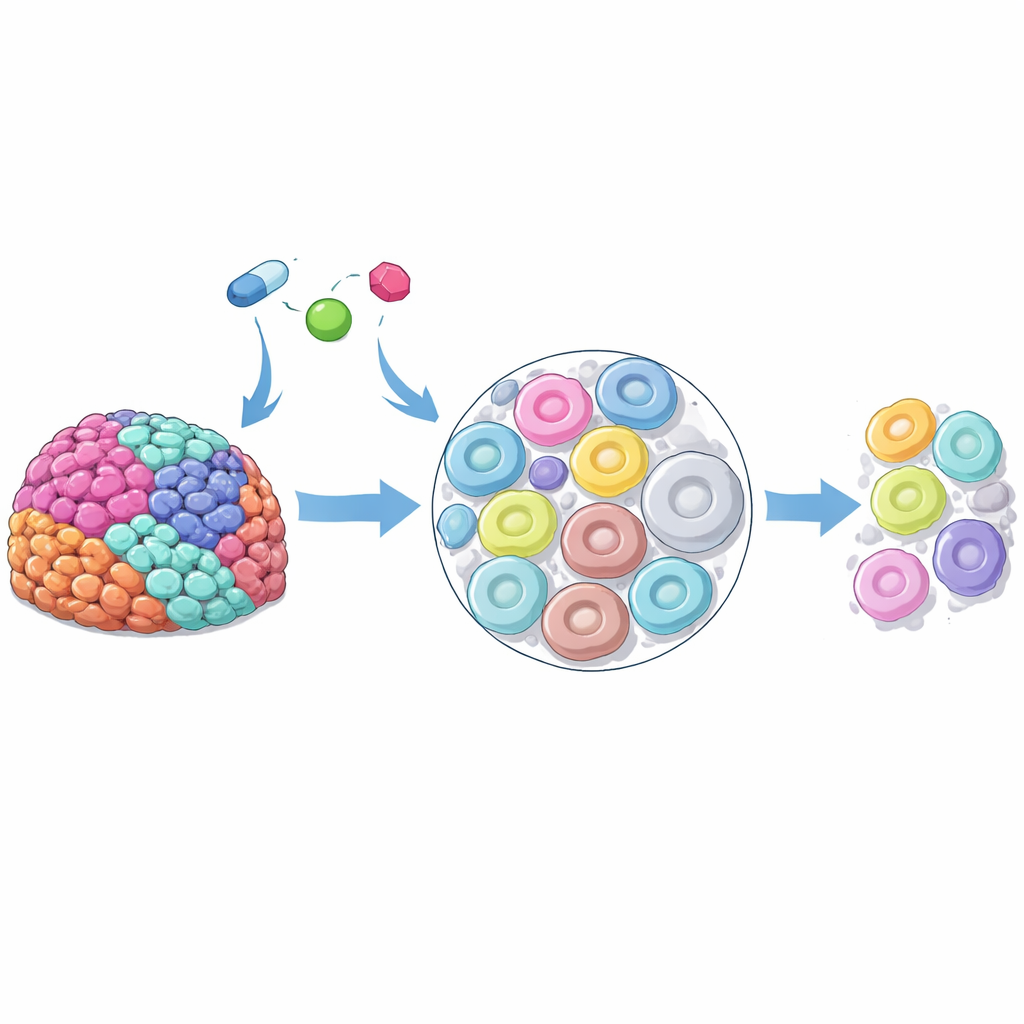
Las regiones ricas en fármaco responden mejor pero revelan una pista celular
Para determinar qué diferenciaba los puntos calientes de las regiones con poco fármaco, el equipo usó transcriptómica espacial, una tecnología que lee la actividad génica preservando la disposición del tejido. Al comparar regiones con niveles altos frente a bajos de dos inhibidores de PARP (rucaparib y niraparib), encontraron que las zonas ricas en fármaco mostraban señales más fuertes de daño en el ADN, detención del ciclo celular y muerte programada, precisamente lo que estos fármacos pretenden inducir. Al mismo tiempo, estas regiones con alta concentración expresaron de forma consistente más genes asociados a lisosomas, los compartimentos ácidos que digieren desechos celulares y reciclan componentes. Múltiples genes ligados a lisosomas mostraron una correlación estrecha con la concentración local de fármaco, lo que sugiere que las diferencias en el contenido lisosomal podrían ayudar a determinar cuánto fármaco puede almacenar una célula y cuán intensamente responde.
Las células individuales muestran diferencias no genéticas en la captación de fármaco
Para acercarse más, los científicos trabajaron con líneas celulares de cáncer de ovario cultivadas en laboratorio. Uno de los fármacos, rucaparib, emite fluorescencia bajo el microscopio, lo que les permitió medir su nivel dentro de miles de células individuales. Observaron hasta cinco veces de diferencia en la señal intracelular entre las células que acumulaban más y las que acumulaban menos, aun cuando todas estuvieron expuestas a la misma concentración. Al ordenar las células más brillantes y las más débiles y cultivarlas durante varias semanas, vieron que estas diferencias no estaban fijadas por la genética: con el tiempo, las poblaciones volvieron a una distribución similar. Esto sugiere que factores no genéticos —como la variabilidad en el contenido de orgánulos o el estado metabólico— subyacen a la diversidad en la captación del fármaco.
Cómo los lisosomas se convierten en un reservorio útil de fármaco
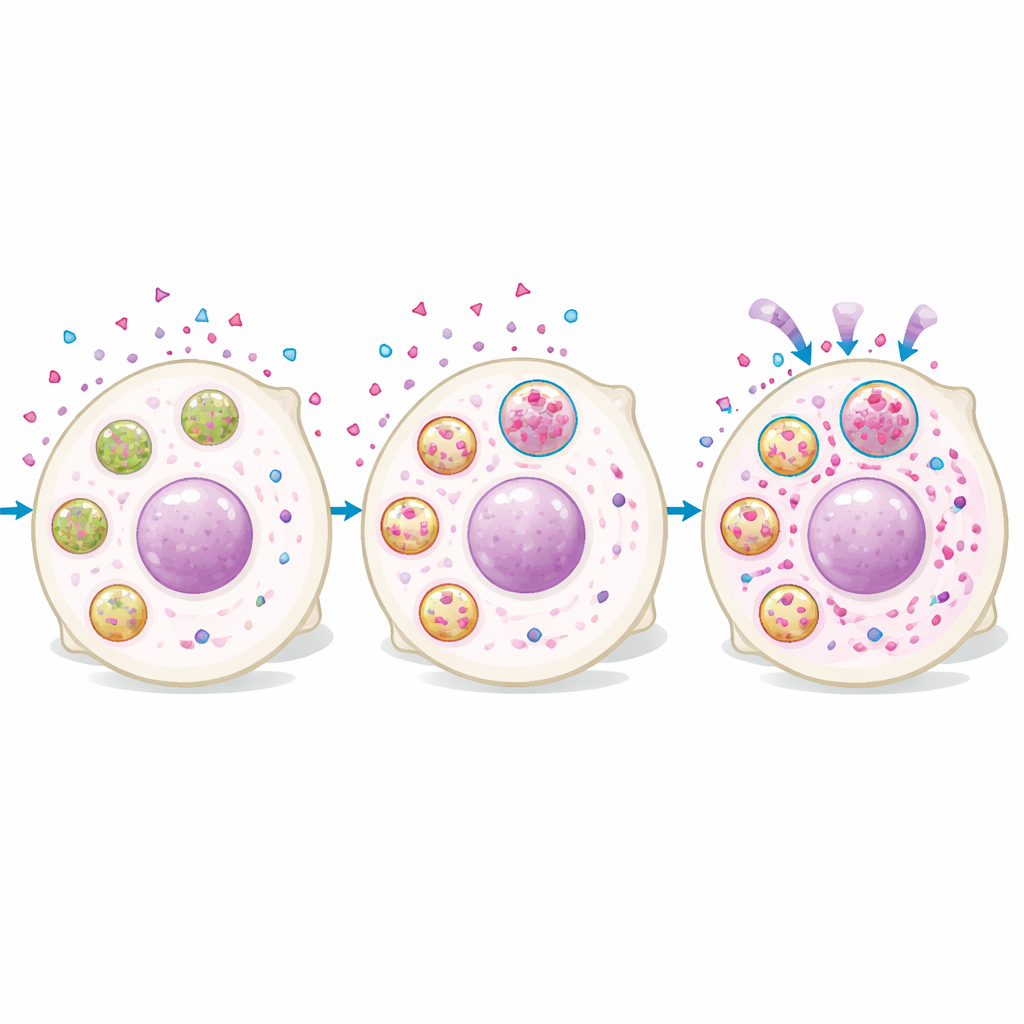
Análisis proteómicos de células con niveles altos frente a bajos de rucaparib mostraron que las células con más fármaco estaban enriquecidas en proteínas lisosomales. La microscopía confirmó que rucaparib entraba rápidamente en las células y luego se acumulaba en estructuras puntiformes que se solapan con colorantes específicos de lisosomas. Las células con mayor señal lisosomal tenían más fármaco intracelular, y manipular los lisosomas cambió los niveles de fármaco: aumentar la formación lisosomal o su acidificación incrementó la acumulación de rucaparib, mientras que neutralizar la acidez lisosomal la redujo. Es importante destacar que el fármaco no quedó atrapado de forma inofensiva. Las células ricas en lisosomas presentaron más daño en el ADN y crecimiento más lento tras el tratamiento, y alterar la función lisosomal redujo los niveles nucleares de fármaco y debilitó el efecto citotóxico a largo plazo después de una exposición breve.
Por qué solo algunos inhibidores de PARP se comportan así
No todos los inhibidores de PARP se comportaron igual. Rucaparib y niraparib son bases débiles, lo que significa que ganan carga y se vuelven menos capaces de atravesar membranas en el entorno ácido de los lisosomas, favoreciendo su acumulación allí. Otro inhibidor de PARP de uso generalizado, olaparib, tiene propiedades químicas muy diferentes y no mostró este tipo de acumulación lisosomal dependiente del pH. Cuando el equipo midió el contenido de fármaco por espectrometría de masas, neutralizar los lisosomas redujo los niveles intracelulares de rucaparib y niraparib pero dejó olaparib sin cambios. De igual modo, alterar el contenido lisosomal solo modificó la respuesta por daño en el ADN a los fármacos base-débiles, no a olaparib. Esto sugiere que los pacientes cuyos tumores tengan naturalmente más lisosomas podrían responder mejor a algunos inhibidores de PARP que a otros.
Qué significa esto para los pacientes y las terapias futuras
Este estudio revela que los lisosomas en las células cancerosas pueden actuar no como una trampa final, sino como un reservorio que almacena ciertos fármacos y los libera lentamente hacia donde actúan, en este caso el núcleo. Debido a la alta heterogeneidad tumoral, las regiones con muchos lisosomas pueden acumular más de determinados inhibidores de PARP, provocando una mayor eliminación local de células tumorales, mientras que zonas cercanas con menos lisosomas podrían recibir una dosis insuficiente a pesar de recibir el mismo tratamiento. En términos prácticos, este trabajo sugiere que emparejar las propiedades químicas de un fármaco con la composición celular del tumor de un paciente —por ejemplo, el contenido lisosomal— podría mejorar las respuestas y superar algunos casos de aparente resistencia al fármaco. También apunta a futuras estrategias diagnósticas en las que pequeñas muestras tumorales se prueban ex vivo para identificar qué fármaco se distribuirá y funcionará mejor para cada individuo.
Cita: R. Moncayo, C., Restuadi, R., Zhang, G. et al. Multimodal imaging reveals a lysosomal drug reservoir that drives heterogeneous distribution of PARP inhibitors. Nat Commun 17, 4086 (2026). https://doi.org/10.1038/s41467-026-70558-1
Palabras clave: cáncer de ovario, inhibidores de PARP, lisosomas, resistencia a fármacos, heterogeneidad tumoral