Clear Sky Science · it
L’imaging multimodale rivela un serbatoio lisosomiale di farmaco che determina la distribuzione eterogenea degli inibitori PARP
Perché questa ricerca conta per il trattamento del cancro
Molti farmaci oncologici moderni sono progettati con grande precisione, eppure falliscono in alcuni pazienti. Un motivo poco esplorato è che i farmaci possono non raggiungere la stessa concentrazione all’interno di tutte le cellule tumorali, anche all’interno di un singolo tumore. Questo studio indaga come tre farmaci ampiamente usati nel carcinoma ovarico, gli inibitori PARP, si distribuiscono nei tumori e nelle singole cellule, e rivela che minuscoli compartimenti di riciclo intracellulare, noti come lisosomi, possono funzionare come un serbatoio nascosto di farmaco che influenza il successo o il fallimento del trattamento.
Livelli di farmaco disomogenei all’interno dello stesso tumore
I ricercatori si sono concentrati sul carcinoma sieroso di alto grado dell’ovaio, una forma aggressiva e altamente variabile di cancro ovarico. Utilizzando campioni di tumore freschi asportati durante l’intervento chirurgico, hanno mantenuto sottili fette di tessuto vive in laboratorio e le hanno esposte a tre inibitori PARP usati clinicamente. Con l’imaging avanzato tramite spettrometria di massa hanno potuto osservare dove i farmaci si accumulavano in ciascuna sezione. Pur essendo tutte le aree esposte alla stessa dose, la distribuzione del farmaco era sorprendentemente irregolare: alcune zone erano veri e propri “hotspot” di farmaco mentre aree vicine ne avevano molto poco. Questa disomogeneità si è osservata tra pazienti diversi, tra tumori differenti nello stesso paziente e persino all’interno di un singolo campione tumorale, suggerendo che proprietà intrinseche alle cellule influenzano fortemente quanto farmaco ogni area assorbe. 
Le regioni ricche di farmaco rispondono meglio ma forniscono un indizio cellulare
Per capire cosa distinguesse gli hotspot dalle regioni a basso contenuto di farmaco, il team ha utilizzato la transcriptomica spaziale, una tecnologia che legge l’attività genica preservando l’organizzazione tissutale. Confrontando le aree con alti e bassi livelli di due inibitori PARP (rucaparib e niraparib), hanno trovato che le regioni ricche di farmaco mostravano segnature più forti di danno al DNA, arresto del ciclo cellulare e morte programmata — esattamente gli effetti che questi farmaci dovrebbero innescare. Allo stesso tempo, queste aree ad alto contenuto di farmaco esprimevano costantemente più geni legati ai lisosomi, i compartimenti acidi che digeriscono i rifiuti cellulari e riciclano componenti. Molti geni associati ai lisosomi mostravano una correlazione stretta con la concentrazione locale di farmaco, suggerendo che differenze nel contenuto lisosomiale potrebbero influenzare quanto farmaco una cellula può trattenere e quanto intensamente risponde.
Le singole cellule mostrano differenze non genetiche nell’assorbimento del farmaco
Per ingrandire ulteriormente, gli scienziati hanno usato linee cellulari di carcinoma ovarico coltivate in vitro. Uno dei farmaci, il rucaparib, è fluorescente al microscopio, permettendo di misurarne il livello all’interno di migliaia di singole cellule. Hanno osservato fino a una differenza di cinque volte nel segnale intracellulare tra le cellule che accumulavano di più e quelle che accumulavano di meno, nonostante tutte fossero esposte alla stessa concentrazione. Selezionando le cellule più brillanti e le più deboli e facendole crescere per diverse settimane, le differenze non si sono mantenute fisse: col tempo le popolazioni sono tornate a una distribuzione simile. Ciò suggerisce che sono fattori non genetici — come il contenuto variabile di organelli o lo stato metabolico — a determinare la diversità nell’assorbimento del farmaco.
Come i lisosomi diventano un serbatoio utile di farmaco
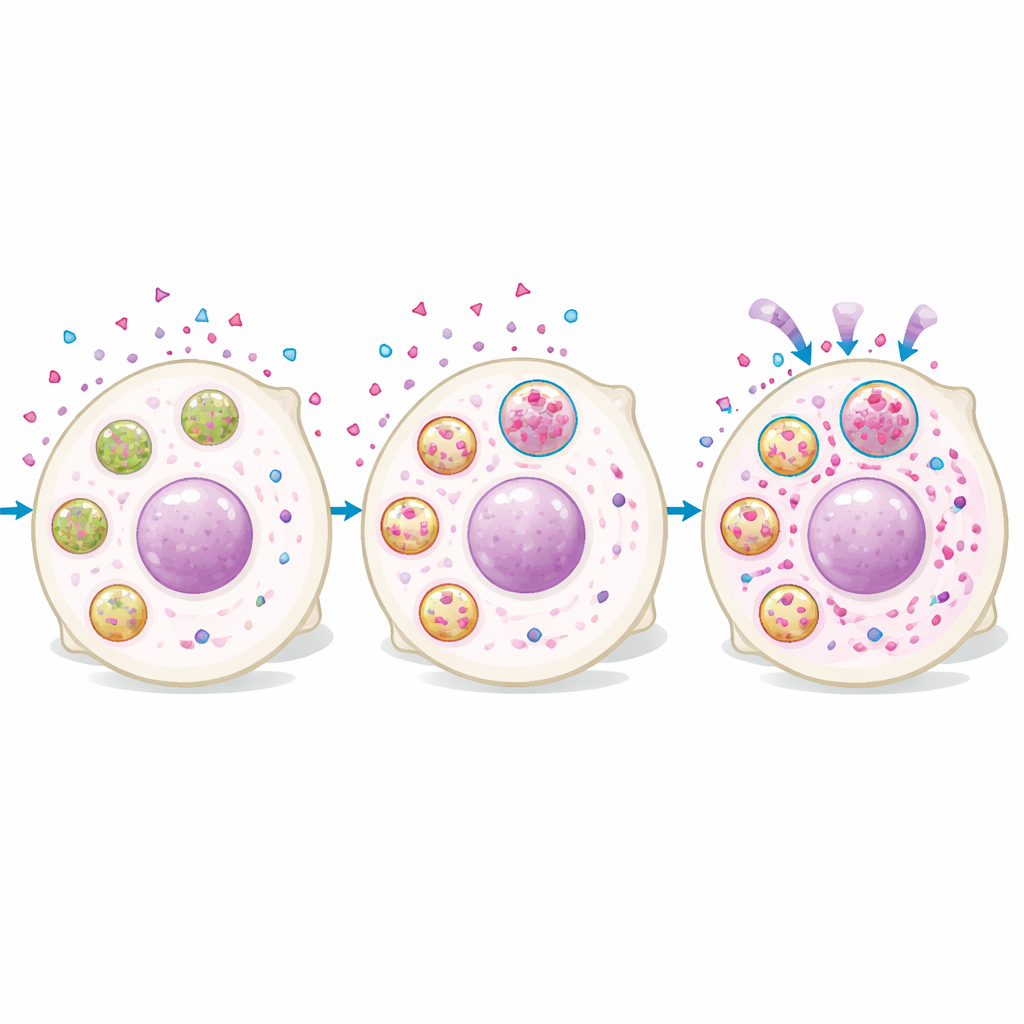
L’analisi proteomica delle cellule con livelli elevati rispetto a bassi di rucaparib ha mostrato che le cellule con alto contenuto di farmaco erano arricchite in proteine lisosomiali. L’imaging ha confermato che il rucaparib entra rapidamente nelle cellule e poi si accumula in strutture puntiformi che si sovrappongono con coloranti specifici per i lisosomi. Le cellule con segnale lisosomiale più intenso avevano più farmaco intracellulare, e manipolare i lisosomi cambiava i livelli di farmaco: incrementare la formazione o l’acidificazione dei lisosomi aumentava l’accumulo di rucaparib, mentre neutralizzare l’acidità lisosomiale lo riduceva. È importante sottolineare che il farmaco non rimaneva intrappolato in modo innocuo: le cellule ricche di lisosomi mostravano più danno al DNA e una crescita più lenta dopo il trattamento, e compromettere la funzione lisosomiale abbassava i livelli nucleari di farmaco e indeboliva l’effetto citotossico a lungo termine dopo un’esposizione breve.
Perché solo alcuni PARP si comportano in questo modo
Non tutti gli inibitori PARP si comportano allo stesso modo. Rucaparib e niraparib sono basi deboli, il che significa che acquistano carica e diventano meno in grado di attraversare le membrane nell’ambiente acido dei lisosomi, favorendo così il loro accumulo lì. Un altro inibitore PARP ampiamente usato, l’olaparib, ha proprietà chimiche molto diverse e non ha mostrato questo tipo di accumulo lisosomiale dipendente dal pH. Quando il team ha misurato il contenuto di farmaco con la spettrometria di massa, la neutralizzazione dei lisosomi ha ridotto i livelli intracellulari di rucaparib e niraparib ma non ha influenzato olaparib. Allo stesso modo, alterare il contenuto lisosomiale ha cambiato solo la risposta al danno al DNA indotta dai farmaci base deboli, non quella indotta da olaparib. Questo suggerisce che i pazienti i cui tumori hanno naturalmente più lisosomi potrebbero rispondere meglio ad alcuni inibitori PARP rispetto ad altri.
Cosa significa per i pazienti e per le terapie future
Questo studio mostra che i lisosomi nelle cellule tumorali possono agire non come una trappola finale, ma come un serbatoio che immagazzina certi farmaci e li rilascia lentamente verso i loro bersagli, in questo caso il nucleo. Poiché i tumori sono altamente eterogenei, le regioni con molti lisosomi possono accumulare più di specifici inibitori PARP, portando a una maggiore distruzione locale delle cellule tumorali, mentre aree vicine con meno lisosomi possono essere sotto-dosate nonostante ricevano lo stesso trattamento. In termini pratici, questo lavoro suggerisce che abbinare le proprietà chimiche di un farmaco alla composizione cellulare del tumore di un paziente — per esempio il contenuto lisosomiale — potrebbe migliorare le risposte e superare alcuni casi di apparente resistenza ai farmaci. Indica inoltre possibili strategie diagnostiche future in cui piccoli campioni tumorali sono testati ex vivo per identificare quale farmaco si distribuirà e funzionerà meglio per ciascun individuo.
Citazione: R. Moncayo, C., Restuadi, R., Zhang, G. et al. Multimodal imaging reveals a lysosomal drug reservoir that drives heterogeneous distribution of PARP inhibitors. Nat Commun 17, 4086 (2026). https://doi.org/10.1038/s41467-026-70558-1
Parole chiave: cancro ovarico, inibitori PARP, lisosomi, resistenza ai farmaci, eterogeneità tumorale