Clear Sky Science · ja
マルチモーダルイメージングが明らかにする、PARP阻害薬の不均一な分布を生むリソソーム内薬物リザーバー
なぜこの研究ががん治療に重要か
現代の多くのがん薬は極めて精密に設計されていますが、それでも一部の患者には効かないことがあります。そのあまり探られてこなかった理由のひとつが、薬が単一の腫瘍内であってもすべてのがん細胞に同じ濃度で到達しない可能性です。本論文は、卵巣がんで広く使われるPARP阻害薬のうち3剤が腫瘍や個々の細胞内でどのように広がるかを調べ、細胞内の小さなリサイクル区画であるリソソームが、治療の成否を左右する隠れた薬物リザーバーとして働くことを明らかにしています。
同一腫瘍内での薬物濃度の不均一性
研究者たちは、攻撃性が高く変異の幅も大きい高悪性度漿液性卵巣がんに着目しました。手術で摘出した新鮮な腫瘍試料を薄切りにして培養条件で生かし、臨床で用いられる3種類のPARP阻害薬を含ませました。高性能の質量分析イメージングにより、各スライスで薬がどこに蓄積するかを可視化できました。すべての領域が同じ投与量にさらされているにも関わらず、薬の分布は著しく不均一で、薬物の“ホットスポット”となる領域とごく近接したごく少量の領域が共存していました。この斑状性は患者間、同一患者内の異なる腫瘍、さらには単一の腫瘍試料内でも見られ、細胞内在性の性質が局所ごとの薬物取り込み量を強く左右していることを示唆しています。 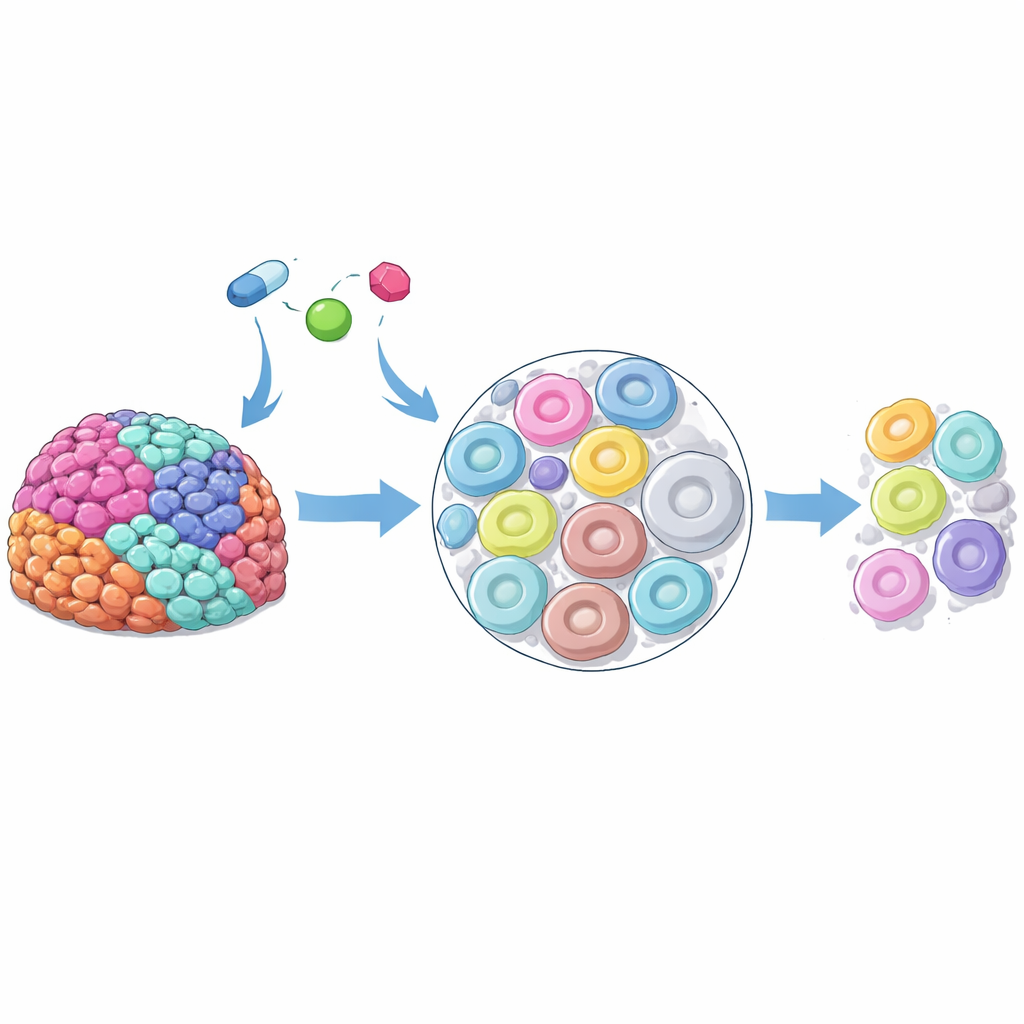
薬物に富む領域はより良く反応するが、細胞内に手がかりがある
ホットスポットと低薬物領域を区別するため、チームは組織の空間的配置を保持したまま遺伝子発現を読む空間トランスクリプトミクスを用いました。2つのPARP阻害薬(ルカパリブとニラパリブ)の高濃度領域と低濃度領域を比較すると、薬物が多く蓄積する領域は、DNA損傷、細胞周期停止、プログラム細胞死のシグネチャーが強く現れており、これらの薬が誘導する応答が局所でより顕著であることが分かりました。同時に、これらの高薬物領域は一貫してリソソームに関連する遺伝子の発現が高く、複数のリソソーム関連遺伝子が局所的な薬物濃度と強い相関を示しました。これはリソソーム含有量の差が細胞が保持できる薬物量や反応性を決める要因の一つであり得ることを示唆しています。
単一細胞レベルで見られる非遺伝的な薬物取り込み差
さらに詳細を調べるため、研究者たちは培養下の卵巣がん細胞株に注目しました。うち1剤であるルカパリブは顕微鏡下で蛍光を示すため、何千もの個々の細胞内での取り込み量を測定できます。すべて同一濃度にさらされているにもかかわらず、細胞間で最大5倍の差が観察されました。最も明るい集団と最も暗い集団を分離して数週間培養すると、これらの差は遺伝的に固定されたものではなく、時間とともに分布が戻ることが分かりました。このことは、オルガネラの量や代謝状態などの非遺伝的要因が薬物取り込みの多様性の基盤になっていることを示しています。
リソソームが有効な薬物リザーバーになる仕組み
ルカパリブ量の多い細胞と少ない細胞のプロテオーム解析は、高薬物細胞がリソソーム関連タンパク質に富んでいることを示しました。イメージングでも、ルカパリブは細胞内に素早く取り込まれ、リソソーム特異的な染色と重なる斑点状構造に蓄積することが確認されました。リソソーム信号の強い細胞ほど細胞内薬物量が多く、リソソームを増やしたり酸性化を促すとルカパリブの蓄積が増え、逆にリソソームの酸性を中和すると蓄積が減りました。重要なのは、薬が無害に閉じ込められるだけではない点です。リソソームに富む細胞は処理後により多くのDNA損傷を示し増殖が遅くなり、リソソーム機能を乱すと短い曝露後の長期的な殺細胞効果が弱まることが示されました。 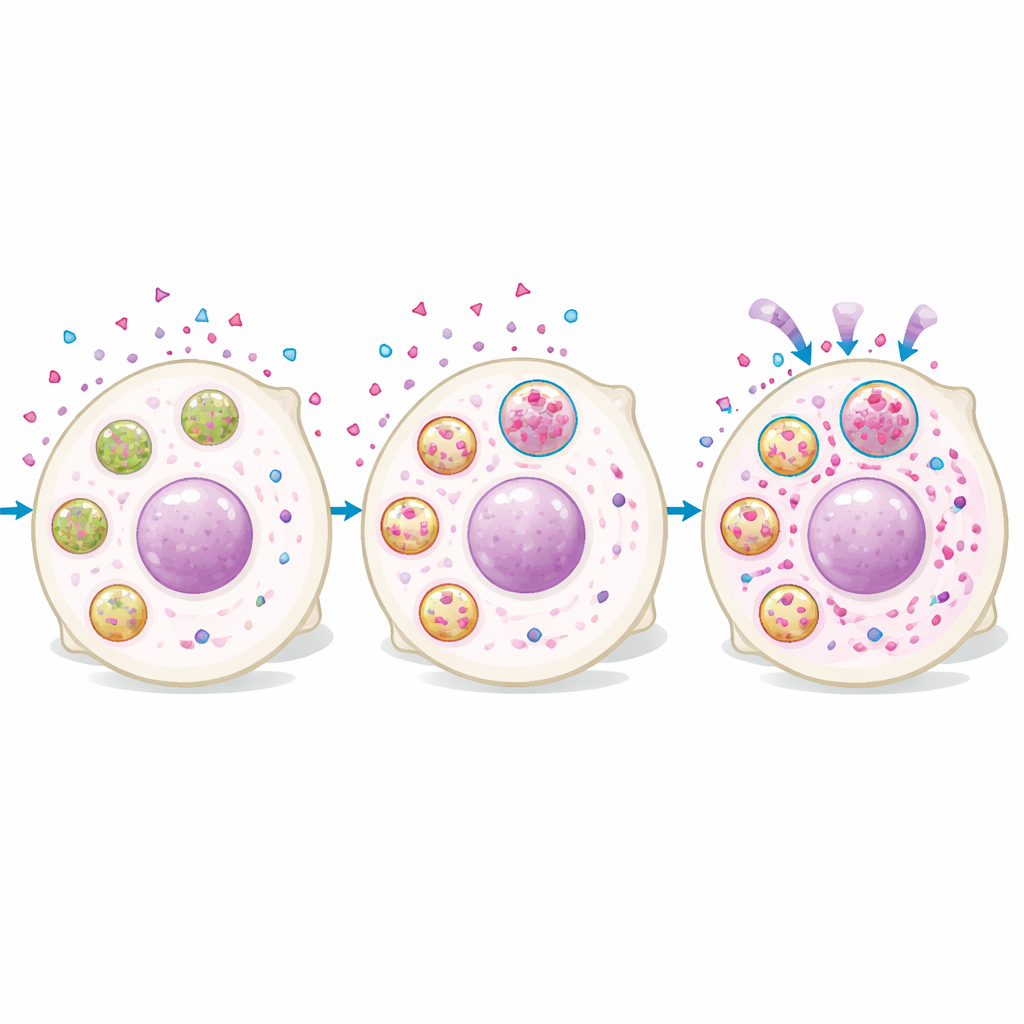
なぜ一部のPARP薬だけがこの振る舞いを示すのか
すべてのPARP阻害薬が同じ挙動を示すわけではありませんでした。ルカパリブとニラパリブは弱塩基性で、リソソームの酸性環境でプロトンを取りやすくなり帯電することで膜透過性が低下し、リソソーム内に蓄積しやすくなります。一方、他の広く用いられるPARP阻害薬オラパリブは化学的性質が異なり、pH依存性のリソソーム蓄積を示しませんでした。質量分析で薬物含量を測ると、リソソームを中和するとルカパリブとニラパリブの細胞内量は減少しましたが、オラパリブは変わりませんでした。同様に、リソソーム量を変えてもDNA損傷応答が変化するのは弱塩基性薬のみで、オラパリブには影響しませんでした。これは、腫瘍が元々リソソームを多く含む患者では、薬の化学的性質によって一部のPARP阻害薬に対する反応が異なる可能性があることを示唆します。
患者と今後の治療への含意
本研究は、がん細胞内のリソソームが単なる行き止まりのトラップではなく、特定の薬剤を貯蔵し徐々に薬を作用部位(本例では核)に供給するリザーバーとして働き得ることを明らかにしました。腫瘍は高度に不均一であるため、リソソームの多い領域は特定のPARP阻害薬をより多く蓄積して局所での細胞死を促す一方、隣接するリソソームの少ない領域は同じ治療を受けていても実質的に十分な薬が届かない可能性があります。実用的には、薬の化学的性質を患者の腫瘍の細胞組成(例:リソソーム含有量)に合わせることが治療反応を改善し、見かけ上の薬剤耐性の一部を克服する手助けになることが示唆されます。また、小さな腫瘍サンプルをex vivoで試験して、どの薬が各患者にとって最もよく分布し有効かを見極める診断戦略の可能性も示しています。
引用: R. Moncayo, C., Restuadi, R., Zhang, G. et al. Multimodal imaging reveals a lysosomal drug reservoir that drives heterogeneous distribution of PARP inhibitors. Nat Commun 17, 4086 (2026). https://doi.org/10.1038/s41467-026-70558-1
キーワード: 卵巣がん, PARP阻害薬, リソソーム, 薬剤耐性, 腫瘍の不均一性