Clear Sky Science · ru
Мультимодальная визуализация выявляет лизосомный резервуар для препаратов, определяющий неоднородное распределение ингибиторов PARP
Почему это исследование важно для лечения рака
Многие современные противораковые препараты созданы с высокой точностью, но все же не помогают всем пациентам. Одна малоизученная причина — то, что лекарство может достигать разной концентрации внутри отдельных раковых клеток, даже в пределах одной опухоли. В этой работе исследуют, как три широко применяемых препарата при раке яичников — ингибиторы PARP — распространяются по опухоли и отдельным клеткам, и показывают, что крошечные перерабатывающие отделы в клетке, известные как лизосомы, могут выступать в роли скрытого лекарственного резервуара, который определяет, удастся ли лечение.
Неравномерные уровни лекарства внутри одной опухоли
Исследователи сосредоточились на высокозлокачественной серозной карциноме яичников — агрессивной и сильно переменной форме рака яичников. Используя свежие образцы опухоли, удалённые во время операции, они сохраняли тонкие срезы тканей живыми в лаборатории и выдерживали их в растворе с тремя клинически применяемыми ингибиторами PARP. С помощью продвинутой визуализации масс-спектрометрией они могли видеть, где накапливались препараты по всему срезу. Хотя все области подвергались одинаковой «дозе», распределение лекарств было поразительно неравномерным — в некоторых зонах формировались лекарственные «горячие точки», тогда как рядом лежали области с очень низким содержанием препарата. Такая пятнистость наблюдалась между разными пациентами, между различными опухолями у одного пациента и даже внутри одного образца опухоли, что указывает на важную роль клеточных внутренних свойств в том, сколько препарата поглощает каждая область. 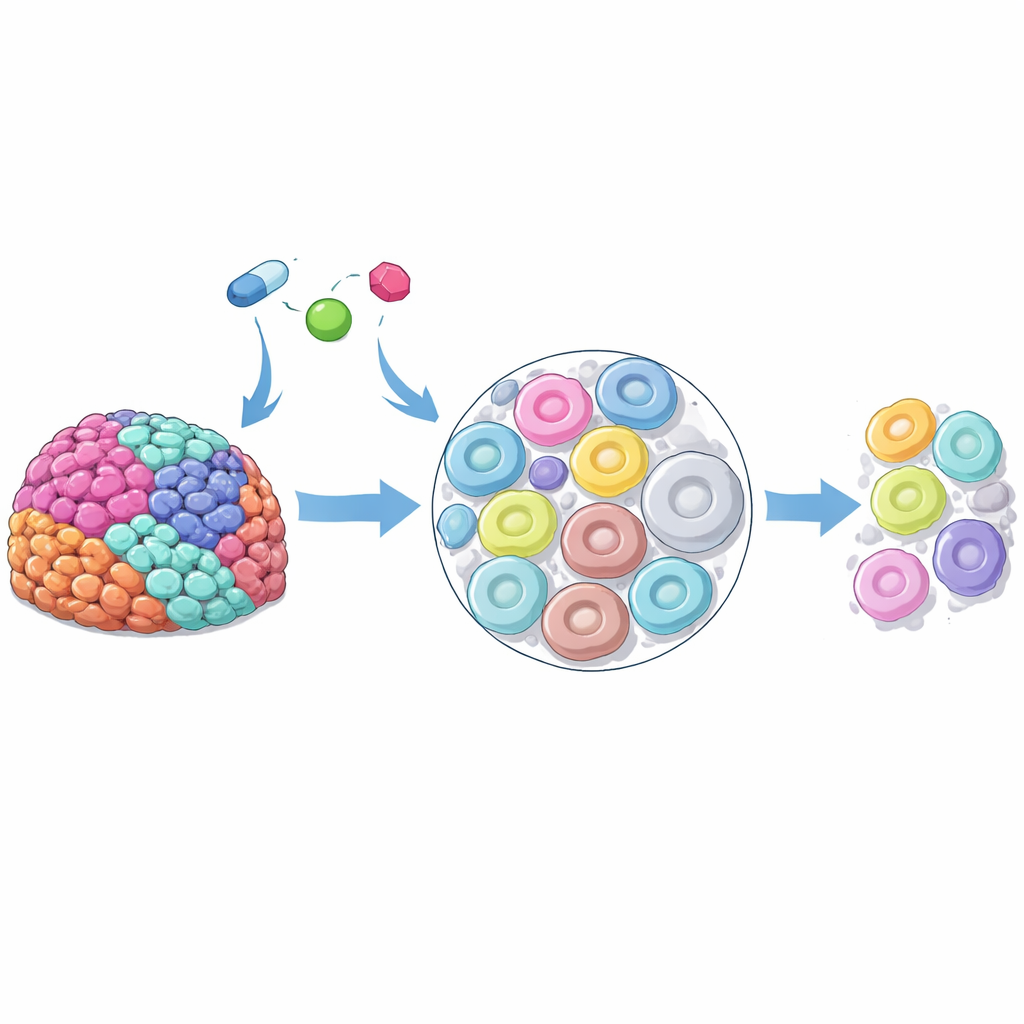
Области с высоким содержанием препарата лучше реагируют, но дают подсказку на уровне клетки
Чтобы понять, чем отличаются «горячие» зоны от областей с низким содержанием лекарства, команда использовала пространственную транскриптомику — технологию, которая фиксирует активность генов с сохранением пространственной организации ткани. Сравнивая области с высоким и низким уровнем двух ингибиторов PARP (рукапариб и нирапариб), они обнаружили, что богатые лекарством зоны демонстрируют более сильные признаки повреждения ДНК, остановки клеточного цикла и программируемой гибели — именно те эффекты, которые должны вызывать эти препараты. В то же время в зонах с высоким содержанием препаратов постоянно повышалась экспрессия генов, связанных с лизосомами — кислотными компартментами, которые переваривают клеточный мусор и перерабатывают компоненты. Несколько генов, ассоциированных с лизосомами, показали тесную корреляцию с локальной концентрацией препарата, что навевает мысль: различия в содержимом лизосом могут определять, сколько препарата клетка способна удержать и насколько сильно она на него реагирует.
Отдельные клетки демонстрируют негентетические различия в поглощении лекарства
Чтобы приблизить картину, учёные переключились на линии клеток рака яичников, выращиваемые в культуре. Один из препаратов, рукапариб, флуоресцировал под микроскопом, что позволило измерять его уровень внутри тысяч отдельных клеток. Они наблюдали до пятикратной разницы в интенсивности внутриклеточного сигнала между клетками с наибольшим и наименьшим накоплением, хотя все они подвергались одной и той же концентрации. Отсортировав самые яркие и самые тусклые клетки и выращивая их в течение нескольких недель, исследователи показали, что эти различия не фиксированы генетически: со временем популяции возвращались к схожему распределению. Это указывает на то, что за разнообразием поглощения стоят негентетические факторы — например, вариабельное содержание органелл или метаболическое состояние.
Как лизосомы становятся полезным лекарственным резервуаром
Протеомный анализ клеток с высоким и низким уровнем рукапариба показал, что в клетках с большим содержанием препарата обогащены лизосомальные белки. Визуализация подтвердила, что рукапариб быстро входит в клетки, затем накапливается в пунктатных структурах, которые совпадают с красителями, специфичными для лизосом. Клетки с более выраженным лизосомальным сигналом имели больше внутриклеточного препарата, а манипуляции с лизосомами меняли уровни лекарства: усиление образования лизосом или их закисления повышало накопление рукапариба, тогда как нейтрализация кислотности лизосом снижала его. Важно, что препарат не оставался безвредно «запертым» — клетки с большим количеством лизосом имели больше повреждений ДНК и медленнее росли после лечения, а нарушение функции лизосом снижало ядерные уровни препарата и ослабляло долговременный цитотоксический эффект после кратковременной экспозиции. 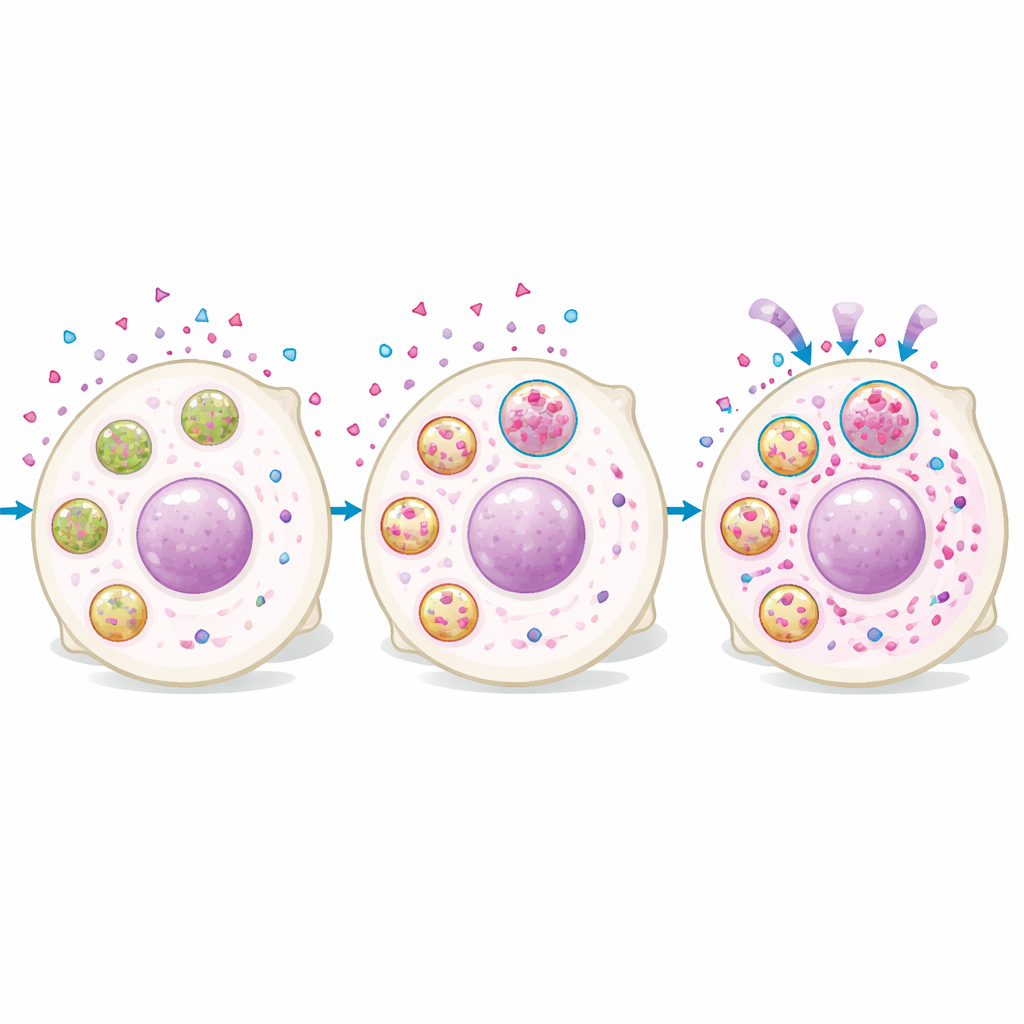
Почему только некоторые препараты PARP ведут себя таким образом
Не все ингибиторы PARP вели себя одинаково. Рукапариб и нирапариб являются слабыми основаниями: в кислой среде лизосом они заряжаются и теряют способность легко пересекать мембраны, что способствует их накоплению в лизосомах. Другой широко используемый ингибитор PARP, олапариб, имеет иные химические свойства и не демонстрировал такого pH-зависимого лизосомального накопления. Когда команда измеряла содержание препаратов масс-спектрометрией, нейтрализация лизосом снижала внутриклеточные уровни рукапариба и нирапариба, но не влияла на олапариб. Аналогично, изменение содержания лизосом меняло ответ повреждения ДНК только для слабых оснований, но не для олапариба. Это подразумевает, что у пациентов с естественно более высоким содержанием лизосом в опухолях одни ингибиторы PARP могут работать лучше других.
Что это значит для пациентов и будущих терапий
Это исследование показывает, что лизосомы в раковых клетках могут выступать не как тупиковая ловушка, а как резервуар, который хранит определённые препараты и медленно возвращает их в те участки, где они действуют — в данном случае в ядро. Поскольку опухоли сильно гетерогенны, области с большим числом лизосом могут накапливать больше конкретных ингибиторов PARP, что приводит к более эффективному локальному уничтожению раковых клеток, тогда как соседние участки с меньшим количеством лизосом могут фактически получать недостаточную дозу, хотя формально получают то же лечение. В практическом плане это означает: подбор препарата с учётом химических свойств и клеточного состава опухоли пациента — например, содержания лизосом — может улучшить отклик и преодолеть часть кажущейся лекарственной резистентности. Работа также указывает на возможные диагностические стратегии, при которых крошечные образцы опухоли тестируют экз vivo, чтобы определить, какой препарат будет лучше распределяться и работать для конкретного пациента.
Цитирование: R. Moncayo, C., Restuadi, R., Zhang, G. et al. Multimodal imaging reveals a lysosomal drug reservoir that drives heterogeneous distribution of PARP inhibitors. Nat Commun 17, 4086 (2026). https://doi.org/10.1038/s41467-026-70558-1
Ключевые слова: рак яичников, ингибиторы PARP, лизосомы, лекарственная резистентность, гетерогенность опухоли