Clear Sky Science · ar
تصوير متعدد الوسائط يكشف عن مخزون دوائي في الليسوزومات يسبب توزيعًا غير متجانس لمثبطات PARP
لماذا يهم هذا البحث لعلاج السرطان
تم تصميم العديد من أدوية السرطان الحديثة بدقة عالية، ومع ذلك تفشل في علاج بعض المرضى. سبب لم يُستكشف كفاية هو أن الدواء قد لا يصل إلى نفس التركيز داخل كل خلية سرطانية، حتى داخل ورم واحد. تبحث هذه الورقة في كيفية انتشار ثلاثة أدوية مستخدمة على نطاق واسع لعلاج سرطان المبيض، تُسمى مثبطات PARP، عبر الأورام والخلايا الفردية، وتكشف أن مقصورات إعادة التدوير الدقيقة داخل الخلايا، المعروفة بالليسوزومات، يمكن أن تعمل كمخزون دوائي خفي يشكل ما إذا كان العلاج سينجح أم سيفشل.
اختلاف مستويات الدواء داخل نفس الورم
ركز الباحثون على السرطان المبيضي المصلي عالي الدرجة، شكل عدواني ومتنوع بشدة من سرطان المبيض. باستخدام عينات ورمية طازجة أزيلت أثناء الجراحة، احتفظوا بشرائح رقيقة من نسيج المرضى حية في المختبر ونقعوها بثلاثة من مثبطات PARP المستخدمة سريريًا. بفضل تصوير الطيف الكتلي المتقدم، تمكنوا من رؤية أماكن تراكم الأدوية عبر كل شريحة. على الرغم من تعرض كل منطقة لنفس الجرعة، كان توزيع الدواء متفاوتًا بشكل لافت — بعض المناطق كانت "نقاط ساخنة" للدواء في حين أن مناطق مجاورة كانت تفتقر إليه. بدا هذا التقطع بين مرضى مختلفين، وبين أورام مختلفة في نفس المريض، وحتى داخل عينة ورمية واحدة، مما يشير إلى أن خصائص داخلية للخلايا تؤثر بقوة في مقدار ما تمتصه كل منطقة من الدواء. 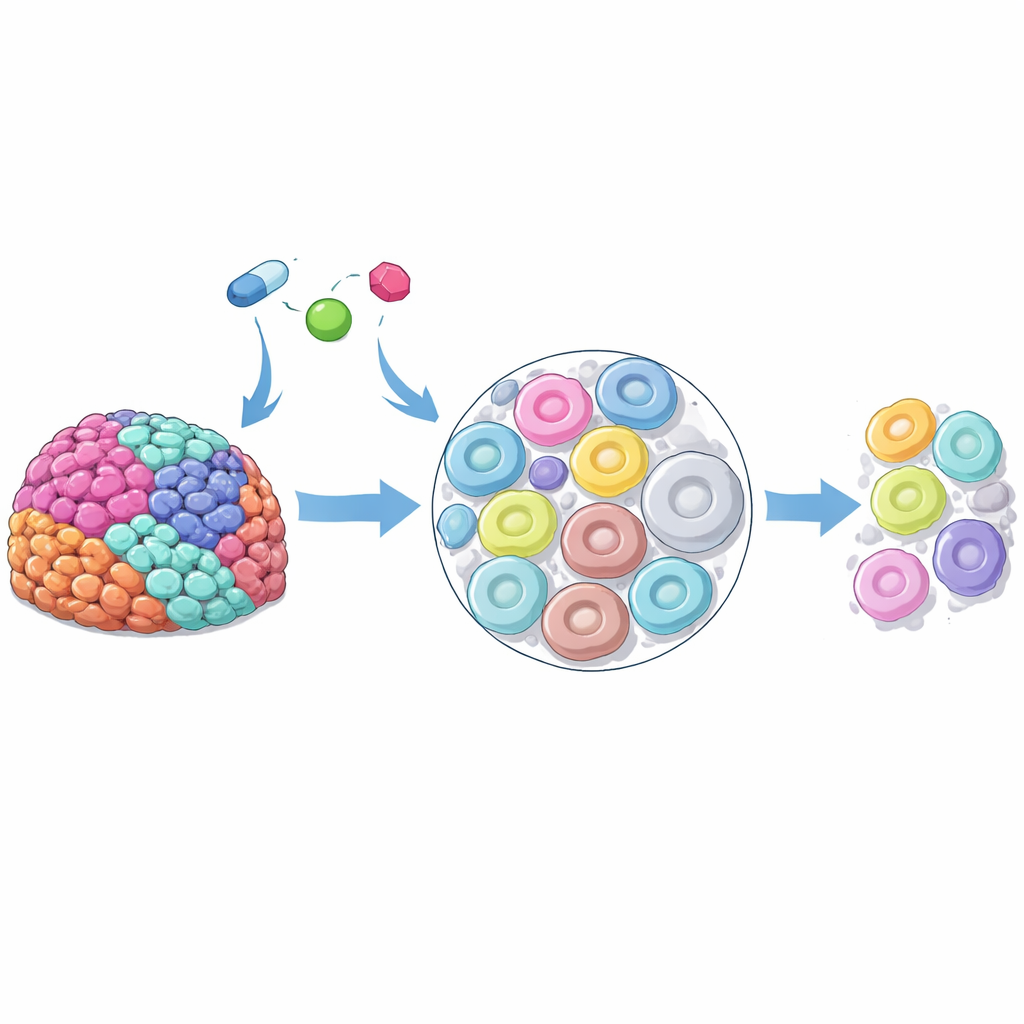
المناطق الغنية بالدواء تستجيب بشكل أفضل لكنها تكشف دليلًا خلويًا
لاكتشاف ما يميز النقاط الساخنة عن المناطق منخفضة الدواء، استخدمت الفريق النسخ المكانية، وهي تقنية تقرأ نشاط الجينات مع الحفاظ على بنية النسيج. بمقارنة المناطق ذات المستويات العالية مقابل المنخفضة لمثبطين اثنين من PARP (روكاباريب ونيراباريب)، وجدوا أن المناطق الغنية بالدواء أظهرت توقيعات أقوى من تلف الحمض النووي، وتوقف دورة الخلية، والموت الخلوي المبرمج — وهي بالضبط الاستجابات التي تهدف هذه الأدوية إلى تحفيزها. في الوقت نفسه، عبرت هذه المناطق ذات التركيزات العالية باستمرار عن مزيد من الجينات المرتبطة بالليسوزومات، المقصورات الحمضية التي تهضم نفايات الخلايا وتعيد تدوير مكوناتها. أظهرت عدة جينات مرتبطة بالليسوزوم ارتباطًا وثيقًا مع تركيز الدواء المحلي، مما يوحي أن اختلافات محتوى الليسوزومات قد تساعد في تحديد مقدار الدواء الذي تستطيع الخلية تخزينه ومدى استجابتها له.
الخلايا المفردة تظهر اختلافات غير جينية في امتصاص الدواء
لتقريب الصورة أكثر، توجه العلماء إلى سلالات خلايا سرطان المبيض المزروعة في المزرعة الخلوية. أحد الأدوية، روكاباريب، يتوهج تحت المجهر، مما أتاح لهم قياس مستواه داخل آلاف الخلايا الفردية. لاحظوا اختلافًا يصل إلى خمسة أضعاف في إشارة الدواء داخل الخلايا بين الخلايا الأعلى والأدنى تراكمًا، على الرغم من تعرض جميعها لنفس التركيز. فصل الخلايا الأكثر سطوعًا والأكثر خفوتًا ونموّها لعدة أسابيع أظهر أن هذه الاختلافات لم تكن ثابتة وراثيًا: مع مرور الوقت عادت التوزيعات إلى نمط مماثل. هذا يوحي بأن عوامل غير جينية — مثل اختلاف محتوى العضيات أو الحالة الأيضية — تقف وراء التنوع في امتصاص الدواء.
كيف تصبح الليسوزومات مخزونًا دوائيًا مفيدًا
أظهرت تحليلات البروتيوم للخلايا ذات مستويات روكاباريب العالية مقابل المنخفضة أن الخلايا الغنية بالدواء مُثقلة ببروتينات ليسوزومية. وأكد التصوير أن روكاباريب دخل الخلايا بسرعة ثم تراكم في هياكل نقطية تداخلت مع صبغات محددة لليسوزومات. الخلايا ذات الإشارة الليسوزومية الأعلى احتوت على كمية أكبر من الدواء داخل الخلية، وتغيير الليسوزومات غيّر مستويات الدواء: زيادة تكوين الليسوزومات أو تحمضها عزز تراكم روكاباريب، بينما قلّلت معادلة حموضة الليسوزومات من ذلك. والمهم أن الدواء لم يبق محبوسًا بلا ضرر؛ فقد أظهرت الخلايا الغنية بالليسوزومات المزيد من تلف الحمض النووي ونموًا أبطأ بعد العلاج، وتعطيل وظيفة الليسوزومات قلل من مستوى الدواء النووي وضعف التأثير القاتل طويل الأمد للدواء بعد نبضة تعرض قصيرة. 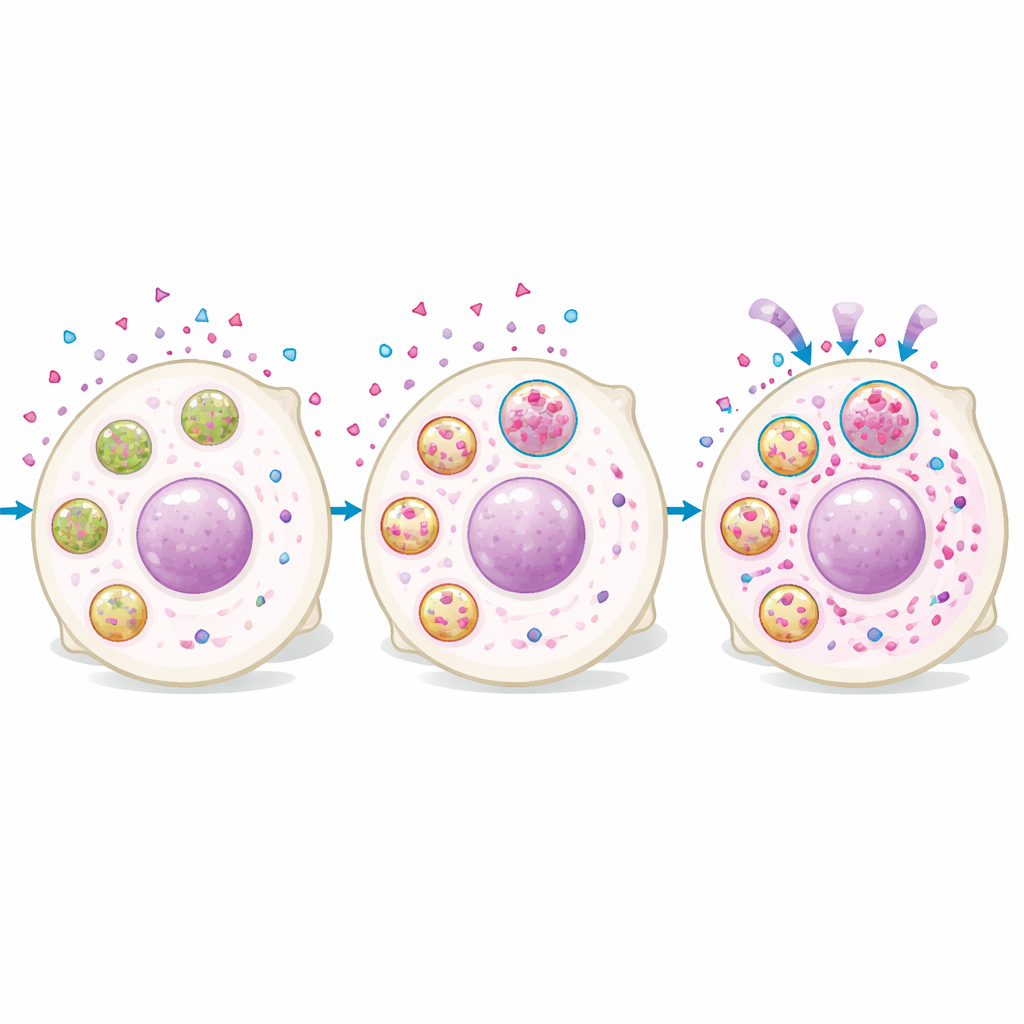
لماذا تتصرف بعض مثبطات PARP بهذه الطريقة فقط
لم تتصرف جميع مثبطات PARP بالمثل. روكاباريب ونيراباريب هما قواعد ضعيفة، ما يعني أنهما يكتسبان شحنة ويصبحان أقل قدرة على عبور الأغشية في بيئة الليسوزومات الحمضية، مما يفضّل تراكمهما هناك. مثبط PARP آخر مستخدم على نطاق واسع، أولاباريب، له خصائص كيميائية مختلفة للغاية ولم يظهر هذا النوع من التراكم الحامضي المعتمد على pH في الليسوزومات. عندما قاس الفريق محتوى الدواء بالتحليل الطيفي الكتلي، أدت معادلة الليسوزومات إلى خفض المستويات داخل الخلايا لروكاباريب ونيراباريب لكنها تركت أولاباريب دون تغيير. وبالمثل، غيّر تعديل محتوى الليسوزومات فقط استجابة تلف الحمض النووي للأدوية ذات القواعد الضعيفة، وليس لأولاباريب. يشير هذا إلى أن المرضى الذين تحتوي أورامهم طبيعيًا على مزيد من الليسوزومات قد يستجيبون بشكل أفضل لبعض مثبطات PARP دون غيرها.
ماذا يعني هذا للمرضى والعلاجات المستقبلية
تكشف هذه الدراسة أن الليسوزومات في خلايا السرطان قد تعمل ليس ككمين قاتل، بل كمخزون يخزن بعض الأدوية ويغذيها ببطء إلى حيث تؤثر، في هذه الحالة النواة. وبما أن الأورام متغايرة للغاية، فقد تتراكم بعض مثبطات PARP في المناطق التي تحتوي على الكثير من الليسوزومات، مما يؤدي إلى قتل محلي أفضل لخلايا السرطان، بينما قد تكون المناطق المجاورة ذات الليسوزومات الأقل معرضة لجرعات منخفضة رغم تلقيها نفس العلاج. عمليًا، يقترح هذا العمل أن مطابقة الخصائص الكيميائية للدواء مع التركيب الخلوي لورم المريض — مثل محتوى الليسوزومات — قد تحسّن الاستجابات وتتغلب على بعض حالات المقاومة الظاهرة للدواء. كما يشير إلى استراتيجيات تشخيصية مستقبلية حيث تُختبر عينات ورمية صغيرة خارج الجسم لتحديد أي دواء سيوزع ويعمل بشكل أفضل لكل فرد.
الاستشهاد: R. Moncayo, C., Restuadi, R., Zhang, G. et al. Multimodal imaging reveals a lysosomal drug reservoir that drives heterogeneous distribution of PARP inhibitors. Nat Commun 17, 4086 (2026). https://doi.org/10.1038/s41467-026-70558-1
الكلمات المفتاحية: سرطان المبيض, مثبطات PARP, الليسوزومات, مقاومة الدواء, تغايرية الورم