Clear Sky Science · pl
Obrazowanie multimodalne ujawnia lizosomalny magazyn leku, który napędza heterogeniczne rozmieszczenie inhibitorów PARP
Dlaczego te badania mają znaczenie dla leczenia nowotworów
Wiele nowoczesnych leków przeciwnowotworowych jest zaprojektowanych z dużą precyzją, a mimo to zawodzi u części pacjentów. Jednym z mało zbadanych powodów jest to, że lek może nie osiągać tej samej koncentracji w każdej komórce nowotworowej, nawet w obrębie jednego guza. W pracy tej zbadano, jak trzy powszechnie stosowane leki w raku jajnika, zwane inhibitorami PARP, rozprzestrzeniają się w guzach i w pojedynczych komórkach, oraz ujawniono, że maleńkie komórkowe „recyklingowe” przedziały, znane jako lizosomy, mogą działać jak ukryty magazyn leku wpływający na to, czy leczenie się powiedzie czy nie.
Nierównomierne poziomy leku w obrębie tego samego guza
Naukowcy skoncentrowali się na gruczolakoraku surowiczym wysokiego stopnia, agresywnej i silnie zróżnicowanej postaci raka jajnika. Korzystając ze świeżych próbek guza pobranych podczas operacji, utrzymywali cienkie plastry tkanki pacjenta przy życiu w laboratorium i eksponowali je na trzy klinicznie stosowane inhibitory PARP. Za pomocą zaawansowanego obrazowania spektrometrii mas mogli zobaczyć, gdzie leki się kumulowały w każdym plastrze. Mimo że każdy obszar był wystawiony na tę samą dawkę, rozmieszczenie leku było wyraźnie nierównomierne – niektóre rejony były „ogniskami” wysokiego stężenia, podczas gdy sąsiednie strefy zawierały go bardzo mało. Ta mozaikowatość pojawiała się między różnymi pacjentami, między różnymi guzami u tego samego pacjenta, a nawet wewnątrz pojedynczej próbki guza, co sugeruje, że właściwości komórkowe istotnie wpływają na to, ile leku dany obszar absorbuje. 
Obszary bogate w lek reagują lepiej, ale wskazują na komórkową wskazówkę
Aby ustalić, co odróżnia ogniska od obszarów z niskim stężeniem leku, zespół zastosował transkryptomikę przestrzenną, technologię odczytującą aktywność genów przy zachowaniu układu tkanki. Porównując rejony o wysokim i niskim poziomie dwóch inhibitorów PARP (rucaparibu i niraparibu), odkryli, że obszary bogate w lek wykazywały silniejsze sygnatury uszkodzeń DNA, zatrzymania cyklu komórkowego i zaprogramowanej śmierci komórkowej – dokładnie to, co te leki mają wywoływać. Jednocześnie regiony o wysokim stężeniu leku konsekwentnie cechowały się większą ekspresją genów związanych z lizosomami, kwaśnymi przedziałami, które trawią odpady komórkowe i recyklingują składniki. Wiele genów powiązanych z lizosomami wykazywało silną korelację z lokalnym stężeniem leku, co sugeruje, że zróżnicowanie zawartości lizosomalnej może wpływać na to, ile leku komórka potrafi zmagazynować i jak silnie odpowiada.
Pojedyncze komórki pokazują niegenetyczne różnice w pobieraniu leku
Aby przyjrzeć się bliżej, naukowcy sięgnęli po linie komórkowe raka jajnika hodowane in vitro. Jeden z leków, rucaparib, świeci pod mikroskopem, co pozwoliło zmierzyć jego poziom w tysiącach pojedynczych komórek. Zaobserwowali do pięciokrotnej różnicy sygnału wewnątrzkomórkowego między komórkami o najwyższym i najniższym nagromadzeniu, mimo tej samej ekspozycji na stężenie leku. Posortowanie najjaśniejszych i najciemniejszych komórek i hodowla tych populacji przez kilka tygodni wykazały, że różnice te nie są ustalone genetycznie: z czasem populacje wracały do podobnego rozkładu. To sugeruje, że przyczyną różnorodności w pobieraniu leku są czynniki niegenetyczne – na przykład zmienna zawartość organelli lub stan metaboliczny.
Jak lizosomy stają się użytecznym magazynem leku
Analizy proteomiczne komórek o wysokim i niskim poziomie rucaparibu wykazały, że komórki z dużą ilością leku były wzbogacone w białka lizosomalne. Obrazowanie potwierdziło, że rucaparib szybko wnika do komórek, a następnie kumuluje się w punktowych strukturach pokrywających się z barwnikami specyficznymi dla lizosomów. Komórki z większym sygnałem lizosomalnym zawierały więcej leku wewnątrz, a manipulacje lizosomami zmieniały poziomy leku: zwiększenie formowania lizosomów lub ich zakwaszenia podnosiło akumulację rucaparibu, podczas gdy neutralizacja kwasowości lizosomów ją obniżała. Co istotne, lek nie pozostawał bezpiecznie uwięziony. Komórki bogate w lizosomy wykazywały więcej uszkodzeń DNA i wolniejszy wzrost po leczeniu, a zaburzenie funkcji lizosomów obniżało poziom leku w jadrach i osłabiało długoterminowy efekt zabijający leku po krótkiej ekspozycji. 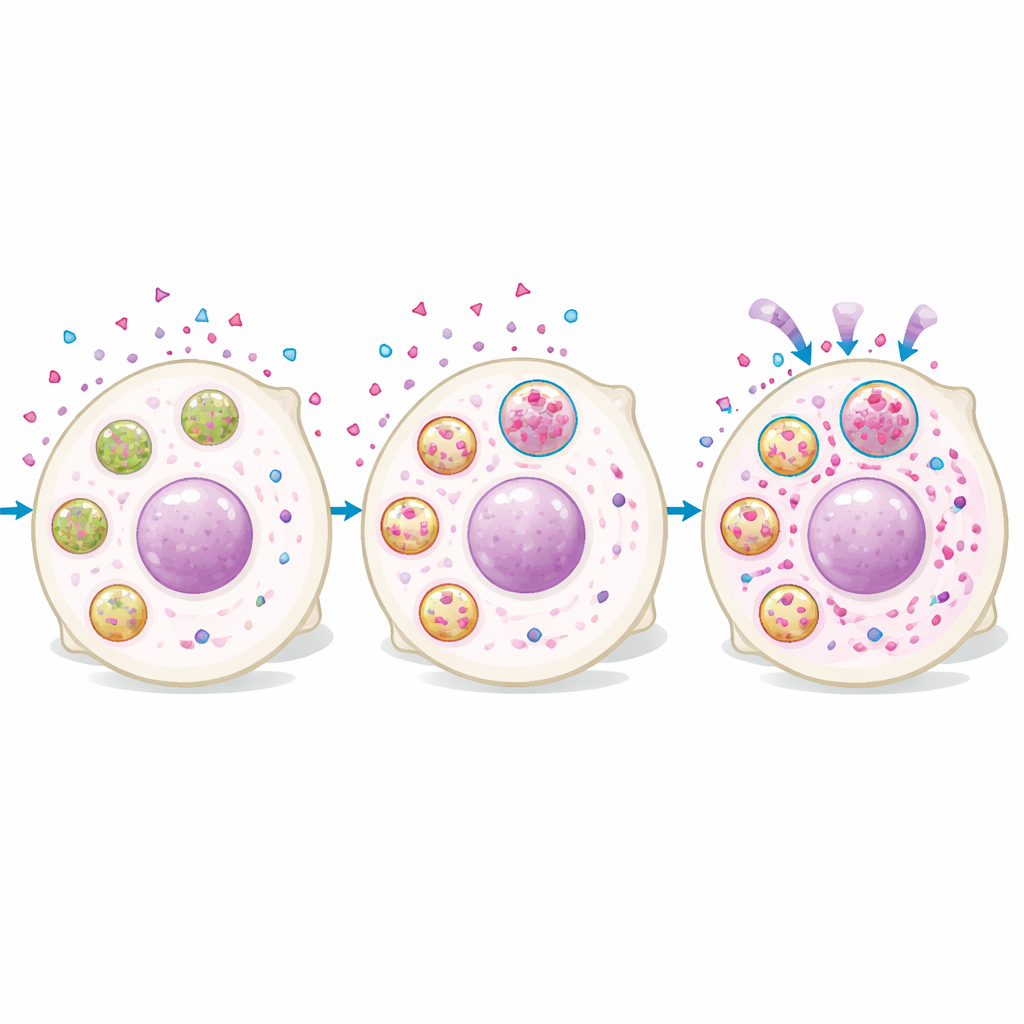
Dlaczego tylko niektóre leki PARP zachowują się w ten sposób
Nie wszystkie inhibitory PARP zachowywały się tak samo. Rucaparib i niraparib są słabymi zasadami, co oznacza, że w kwaśnym środowisku lizosomów zyskują ładunek i stają się mniej zdolne do przechodzenia przez błony, co sprzyja ich kumulacji w tych przedziałach. Inny szeroko stosowany inhibitor PARP, olaparib, ma zupełnie inne właściwości chemiczne i nie wykazywał tego rodzaju pH-zależnej akumulacji w lizosomach. Gdy zespół mierzył zawartość leku za pomocą spektrometrii mas, neutralizacja lizosomów zmniejszała poziomy rucaparibu i niraparibu wewnątrzkomórkowo, ale nie wpływała na olaparib. Podobnie zmiany zawartości lizosomów modyfikowały odpowiedź uszkodzeń DNA jedynie na leki będące słabymi zasadami, nie zaś na olaparib. To sugeruje, że pacjenci, których guzy naturalnie zawierają więcej lizosomów, mogą lepiej reagować na niektóre inhibitory PARP niż na inne.
Co to oznacza dla pacjentów i przyszłych terapii
Badanie to ujawnia, że lizosomy w komórkach nowotworowych mogą działać nie jako ślepy zaułek, lecz jako magazyn, który przechowuje określone leki i stopniowo oddaje je tam, gdzie działają – w tym przypadku do jądra komórkowego. Ponieważ guzy są wysoce heterogeniczne, obszary z dużą liczbą lizosomów mogą gromadzić więcej określonych inhibitorów PARP, prowadząc do lepszego lokalnego zabijania komórek nowotworowych, podczas gdy pobliskie regiony z mniejszą liczbą lizosomów mogą być niedostatecznie dawkowane pomimo otrzymania tego samego leczenia. W praktyce praca ta sugeruje, że dopasowanie właściwości chemicznych leku do komórkowego składu guza pacjenta – na przykład zawartości lizosomów – mogłoby poprawić odpowiedzi i przezwyciężyć niektóre przypadki pozornej oporności na lek. Wskazuje też na przyszłe strategie diagnostyczne, w których niewielkie próbki guza są testowane ex vivo, aby zidentyfikować, który lek najlepiej rozprowadzi się i zadziała u danego pacjenta.
Cytowanie: R. Moncayo, C., Restuadi, R., Zhang, G. et al. Multimodal imaging reveals a lysosomal drug reservoir that drives heterogeneous distribution of PARP inhibitors. Nat Commun 17, 4086 (2026). https://doi.org/10.1038/s41467-026-70558-1
Słowa kluczowe: rak jajnika, inhibitory PARP, lizosomy, oporność na leki, heterogeniczność guza