Clear Sky Science · tr
XA-Novo: monoklonal antikorlar ve antikor karışımları için yüksek verimli kütle spektrometrisi tabanlı de novo dizileme teknolojisi
Antikorların şifresini çözmenin önemi
Antikorlar, virüsleri, bakterileri ve hatta kanser hücrelerini olağanüstü bir doğrulukla tanıyan küçük Y biçimli proteinlerdir. Bunları güçlü ilaçlar veya tanı araçları haline getirmek için araştırmacıların doğru amino asit “hecelemelerini”—yani dizilerini—bilmesi gerekir. Ancak bu diziyi okumak genellikle yavaş, maliyetli ve mevcut DNA tabanlı yöntemlerle bazen imkânsızdır. Bu çalışma, antikor dizilerini doğrudan proteinlerden okuyan XA‑Novo adında yeni bir teknoloji tanıtıyor; yöntem kütle spektrometrisi ve akıllı algoritmaları kullanarak işi daha hızlı, daha doğru ve karmaşık antikor karışımları için bile mümkün kılıyor.
Antikor tariflerini okumadaki mevcut engeller
Antikorları çözmenin geleneksel yolları genellikle onları üreten hücrelerden başlar. Araştırmacılar hibritoma hücreleri yetiştirir veya B hücrelerini izole eder, genetik materyallerini çıkarır ve ardından DNA veya RNA’yı dizeleyerek analiz eder. Bu yaklaşımlar haftalar hatta aylar alabilir, kırılgan veya kaybolmuş olabilecek canlı hücrelere ihtiyaç duyar ve bazen hâlâ boşluklar veya hatalar bırakır. Ayrıca kanda veya mukusta dolaşan antikorların, onları üreten B hücre popülasyonuyla nasıl gerçekten ilişkili olduğunu belirlemekte zorlanırlar. Bir alternatif, antikorlar üzerinde protein düzeyinde çalışmak; antikorları küçük parçalara ayırıp kütle spektrometrisi ile analiz etmektir. Yine de mevcut kütle spektrometrisi yöntemleri genellikle büyük örnek miktarları gerektirir, düşük verimlidir ve özellikle birçok benzer antikor aynı anda bulunduğunda dizileri yanlış birleştirebilir.
Proteinlerden başlayan yeni bir iş akışı
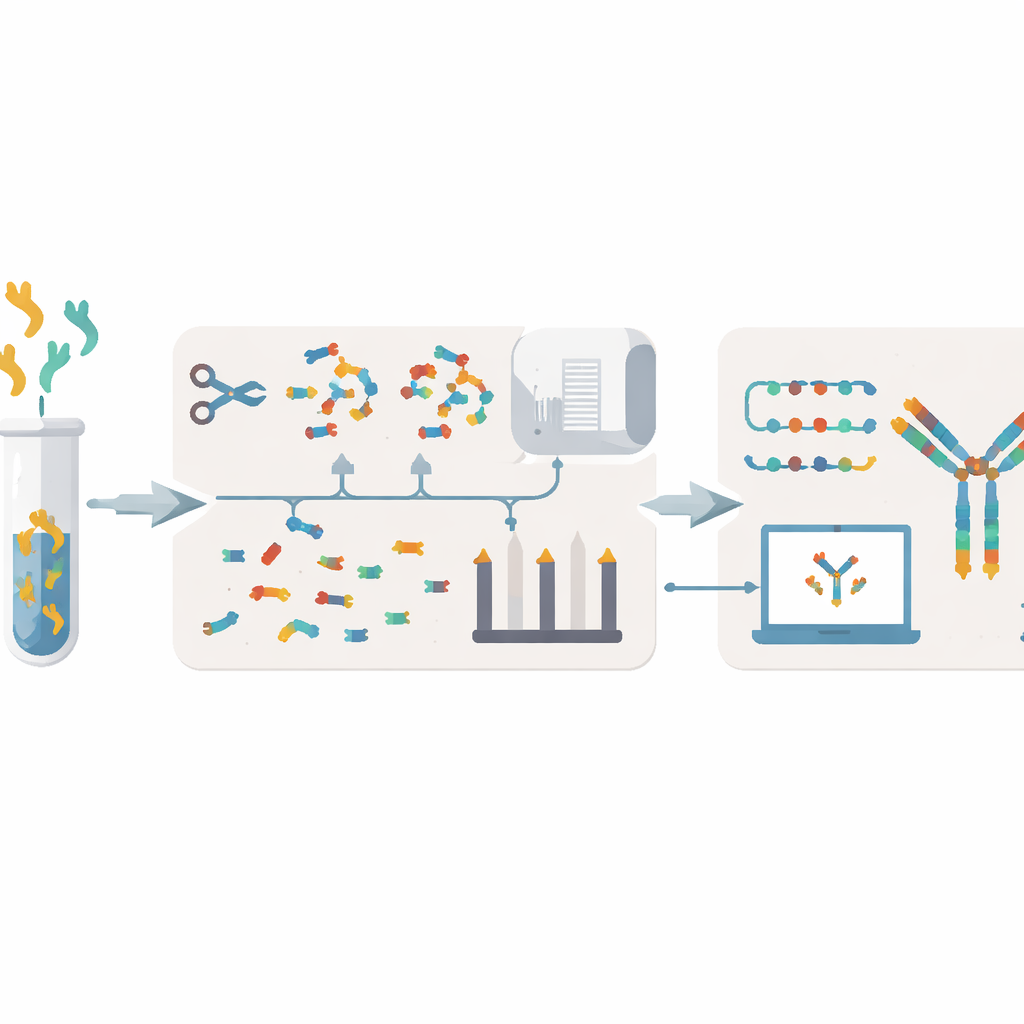
XA‑Novo bu sorunları geliştirilmiş kimya, ileri düzey kütle spektrometrisi ve modern makine öğrenimini tek bir düzenli iş akışında birleştirerek ele alır. Önce, antikorlar beş farklı enzimin zaman farkıyla görev yaptığı bir “tek‑kap çok‑enzimatik gradyan sindirimi” stratejisi kullanılarak nazik ama kapsamlı biçimde örtüşen peptit parçalarına bölünür. Bu, kıymetli numuneyi boşa harcamadan parça çeşitliliğini ve örtüşmesini artırır. Ardından bu parçalar, her peptidin nasıl parçalandığını yakalayan zengin spektral bilgiler üreten iki tamamlayıcı parçalanma modunda yüksek çözünürlüklü kütle spektrometrisi ile analiz edilir.
Derin öğrenme ve akıllı birleştirme
Spektra toplandıktan sonra XA‑Novo, Casanovo adlı bir derin öğrenme modeli kullanarak kütle tepe noktalarının karmaşık desenlerini tahmini peptit dizilerine çevirir; bu, diller arasında çeviri yapan bir dil modeline benzetilebilir. Bu çok sayıda kısa “okuma” daha sonra Fusion adında yeni bir birleştiriciye iletilir. Fusion, örtüşen peptitleri ağır ve hafif zincirler halinde tam dizilere dikmek için bir beam‑search stratejisi ve bilinen antikor şablonlarından gelen bilgileri kullanır. Neredeyse aynı kütleye sahip amino asitler ve bağlanma için en çok değişen bölgeler olan tamamlayıcılık‑belirleyen bölgeler gibi yaygın problem noktalarını ele almak üzere tasarlanmıştır ve işlevi bozabilecek boşluklar, eklemeler veya yanlış sıralanmış dizimleri önlemeyi hedefler.
Yöntemi teste koymak
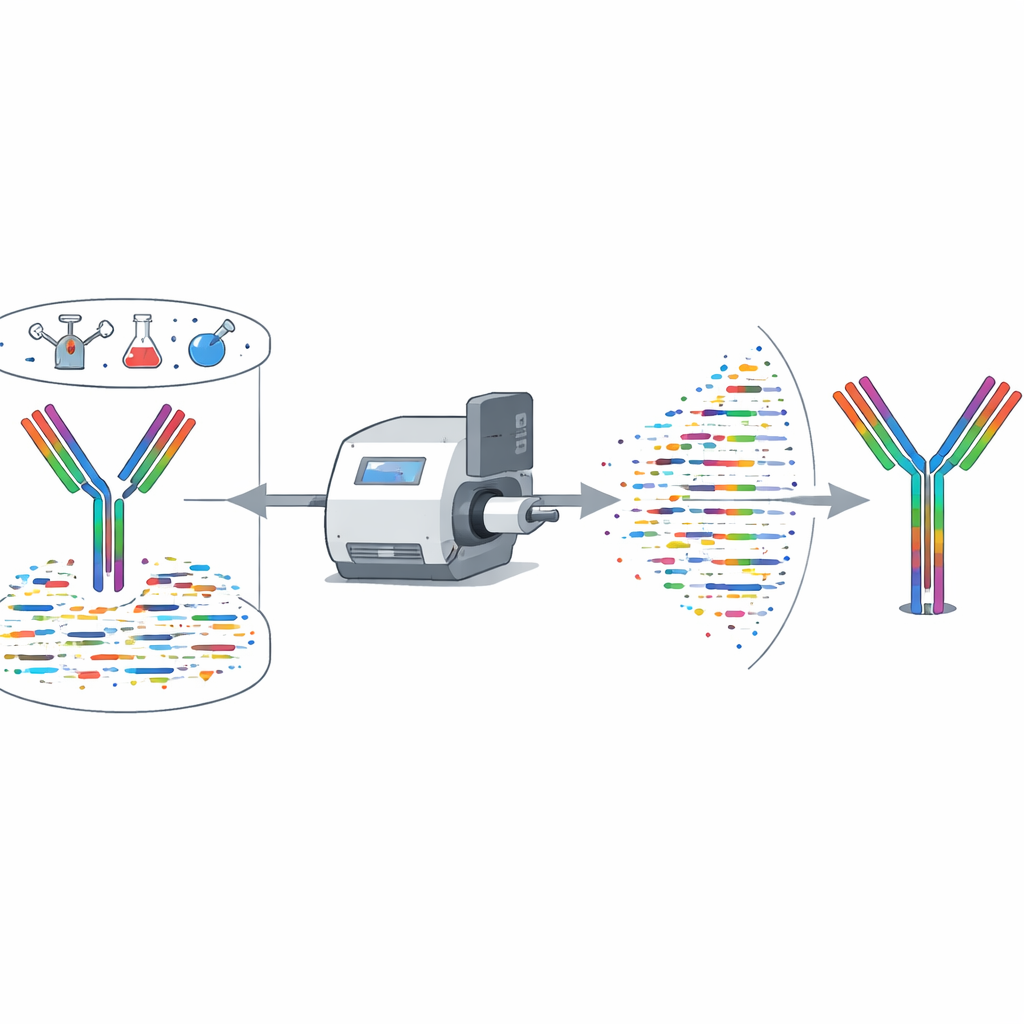
Yazarlar XA‑Novo’yu insan ve fare kaynaklı, dizileri bilinen antikorlar üzerinde titizlikle kıyasladılar; bunların arasında SARS‑CoV‑2’yi nötralize eden birkaç antikor da vardı. Ticari araçlar ve açık algoritmalarla karşılaştırıldığında XA‑Novo, kritik bağlanma bölgelerinde tam ve hatasız yeniden yapılandırmayla sürekli olarak daha yüksek dizi kapsama ve doğruluk sağladı. Sadece 50 mikrogram antikorla başlansa bile güvenilir çalıştı. Ekip sonra dizileri kamuya açık olmayan altı terapötik antikorla uğraştı. XA‑Novo ağır ve hafif zincirlerini çözdü, diziler klonlanıp eksprese edildi ve ortaya çıkan antikorlar farelerde test edildi. İn vivo deneyler, yeniden oluşturulan antikorların hedef immün hücreleri veya makrofajları orijinal ticari versiyonlar kadar etkin biçimde azalttığını gösterdi; bu da çözülen dizilerin fonksiyonel olarak doğru olduğunu doğruladı.
Aynı anda antikor karışımlarını yönetmek
Gerçek dünya örneklerinin çoğu tek, saf bir antikor yerine antikor karışımları içerir. XA‑Novo, hem insan hem fare antikorları için aynı anda iki veya üç COVID‑19 nötralize edici antikorun karışımlarıyla sınandı. Sistem her bileşenin dizisini en az %99.54 doğrulukla ve sık sık %100 ile geri kazandı; en değişken bağlanma döngüleri dahil. Bu performans tipik olarak tek antikora sınırlı olan mevcut birleştiricileri geride bırakıyor. Yazarlar ayrıca araştırmacıların kütle spektrometrisi verilerini yükleyip yeniden oluşturulmuş antikor dizileri ve kapsama haritaları alabilecekleri, özel donanım veya karmaşık kurulum gerektirmeyen web tabanlı bir arayüz de kurdular.
Gelecekteki antikor ilaçları için anlamı
XA‑Novo, artık protein örneklerinden, hatta karışımlardan bile tam ve yüksek doğrulukta antikor dizilerini nispeten az materyal kullanarak ve büyük ölçüde otomatik bir iş akışıyla okuyabilmenin mümkün olduğunu gösteriyor. Uzman olmayanlar için bu, laboratuvarda veya klinikte keşfedilen umut verici antikorların daha hızlı tersine mühendislik ile yeniden üretilebileceği, güvenilir şekilde klonlanıp geliştirilebileceği anlamına geliyor. Antikor dizilemesini daha hızlı, daha ölçeklenebilir ve hassas hücre hatlarına daha az bağımlı hale getirerek XA‑Novo temel immünoloji çalışmalarını hızlandırabilir, COVID‑19 gibi enfeksiyonlara karşı bağışıklık tepkilerini izlemeye yardımcı olabilir ve antikor tabanlı terapilerin geliştirilmesi ile optimizasyonunu hızlandırabilir.
Atıf: Xiong, Y., Jiang, W., Xiao, J. et al. XA-Novo: high-throughput mass spectrometry-based de novo sequencing technology for monoclonal antibodies and antibody mixtures. Nat Commun 17, 3391 (2026). https://doi.org/10.1038/s41467-026-70496-y
Anahtar kelimeler: antikor dizileme, kütle spektrometrisi, monoklonal antikorlar, COVID-19 nötralize edici antikorlar, protein mühendisliği