Clear Sky Science · fr
XA-Novo : technologie de séquençage de novo à haut débit par spectrométrie de masse pour anticorps monoclonaux et mélanges d’anticorps
Pourquoi il importe de décoder les anticorps
Les anticorps sont de petites protéines en forme de Y qui reconnaissent virus, bactéries et même cellules cancéreuses avec une grande précision. Pour en faire des médicaments puissants ou des outils diagnostiques, les scientifiques ont besoin de leur orthographe exacte en acides aminés — leur séquence. Mais lire cette séquence est souvent lent, coûteux, et parfois impossible avec les méthodes basées sur l’ADN actuelles. Cette étude présente XA-Novo, une nouvelle technologie qui lit les séquences d’anticorps directement à partir des protéines elles‑mêmes, en utilisant la spectrométrie de masse et des algorithmes intelligents pour accomplir la tâche plus rapidement, avec plus de précision, et même pour des mélanges complexes d’anticorps.
Obstacles actuels à la lecture des recettes d’anticorps
Les méthodes traditionnelles de décodage des anticorps partent généralement des cellules qui les produisent. Les chercheurs cultivent des hybridomes ou isolent des cellules B, extraient leur matériel génétique, puis séquencent l’ADN ou l’ARN. Ces approches peuvent prendre de quelques semaines à plusieurs mois, nécessitent des cellules vivantes qui peuvent être fragiles ou perdues, et laissent parfois des lacunes ou des erreurs. Elles peinent aussi à établir comment les anticorps présents dans le sang ou les muqueuses se rapportent réellement à la population de cellules B qui les a produits. Une alternative consiste à travailler au niveau protéique en fragmentant les anticorps en petits peptides et en les analysant par spectrométrie de masse. Pourtant, les méthodes de spectrométrie existantes exigent souvent de grandes quantités d’échantillon, ont un faible débit, et peuvent mal assembler les séquences, en particulier lorsque plusieurs anticorps similaires sont présents simultanément.
Une nouvelle chaîne de traitement qui part des protéines
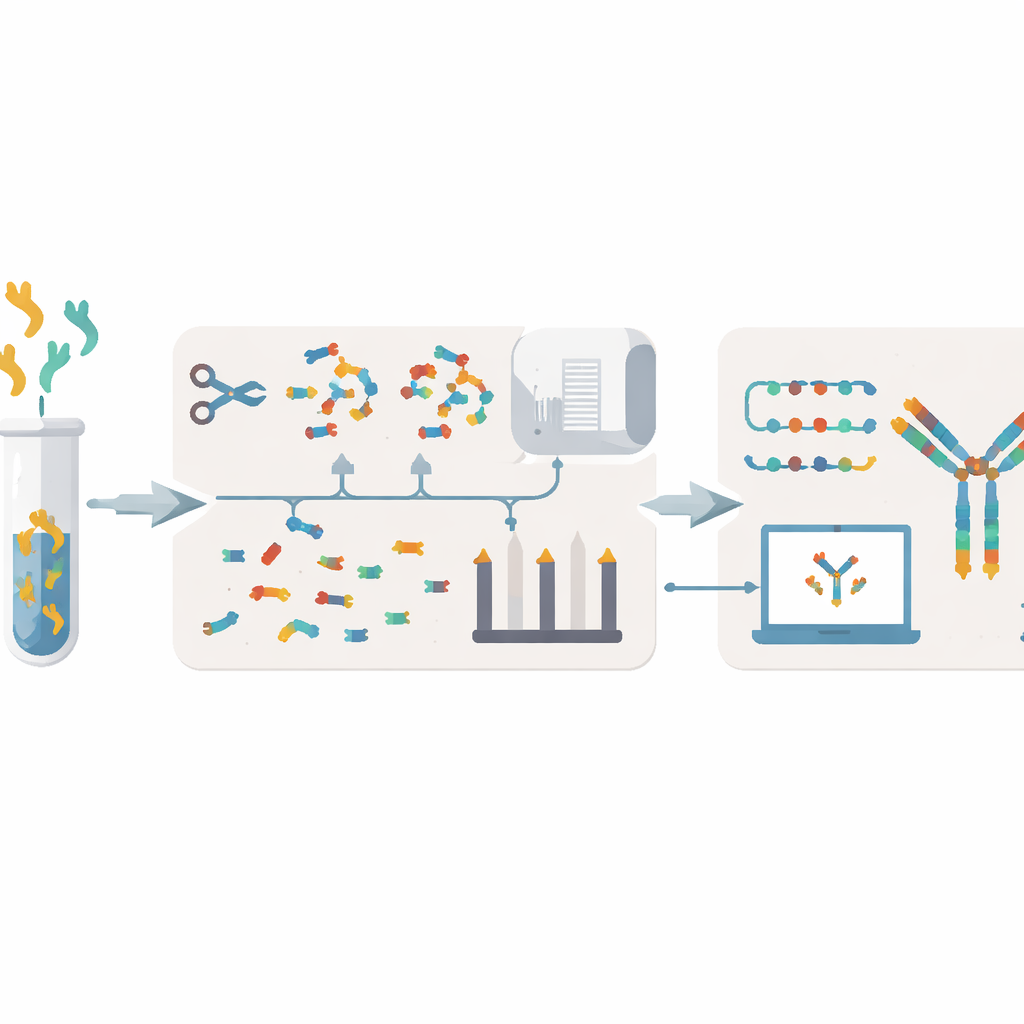
XA-Novo aborde ces problèmes en combinant une chimie améliorée, une spectrométrie de masse avancée et l’apprentissage automatique moderne dans un flux de travail rationalisé. D’abord, les anticorps sont doucement mais efficacement découpés en fragments peptidiques chevauchants à l’aide d’une stratégie de « digestion en gradient multi‑enzymatique en pot unique », où cinq enzymes différentes agissent de manière décalée dans le temps. Cela augmente la diversité et le chevauchement des fragments sans gaspiller d’échantillon précieux. Ensuite, ces fragments sont analysés par spectrométrie de masse haute résolution sous deux modes de fragmentation complémentaires, générant des spectres riches qui capturent la façon dont chaque peptide se désintègre.
Apprentissage profond et assemblage intelligent
Une fois les spectres collectés, XA-Novo utilise un modèle d’apprentissage profond nommé Casanovo pour traduire les motifs complexes des pics de masse en séquences peptidiques prédites, à la manière d’un modèle de langage qui traduit entre langues. Ces nombreuses courtes « lectures » sont ensuite transmises à un nouvel assembleur appelé Fusion. Fusion emploie une stratégie de recherche en faisceau (beam‑search) et s’appuie sur des informations issues de modèles d’anticorps connus pour coudre les peptides chevauchants en chaînes lourdes et légères complètes. Il est conçu pour gérer les points problématiques courants — comme les acides aminés de masses presque identiques et les régions où les anticorps varient le plus pour la liaison, appelées régions déterminantes de la complémentarité — tout en évitant les lacunes, insertions et séquences mal ordonnées qui peuvent compromettre la fonction.
Mise à l’épreuve de la méthode
Les auteurs ont évalué rigoureusement XA-Novo sur des anticorps aux séquences connues provenant d’humains et de souris, y compris plusieurs neutralisant le SARS‑CoV‑2. Par rapport aux outils commerciaux et aux algorithmes publics, XA-Novo a systématiquement obtenu une meilleure couverture et exactitude de séquence, avec des reconstructions complètes et sans erreur dans les régions critiques de liaison. Il a fonctionné de manière fiable même à partir d’aussi peu que 50 microgrammes d’anticorps. L’équipe a ensuite appliqué la méthode à six anticorps thérapeutiques dont les séquences n’étaient pas publiques. XA-Novo a décodé leurs chaînes lourdes et légères, les séquences ont été clonées et exprimées, et les anticorps résultants ont été testés chez la souris. Les expérimentations in vivo ont montré que ces anticorps reconstruits éliminaient leurs cellules immunitaires cibles ou macrophages aussi efficacement que les versions commerciales originales, confirmant que les séquences décodées étaient fonctionnellement correctes.
Traiter des mélanges d’anticorps en une seule fois
De nombreux échantillons du monde réel contiennent des mélanges d’anticorps plutôt qu’un seul anticorps pur. XA-Novo a été testé sur des mélanges de deux ou trois anticorps neutralisants du COVID‑19 simultanément, pour des anticorps humains et murins. Le système a récupéré la séquence de chaque composant avec une couverture précise d’au moins 99,54 %, et souvent 100 %, y compris pour les boucles de liaison les plus variables. Cette performance dépasse celle des assembleurs existants, généralement limités à un seul anticorps. Les auteurs ont également mis en place une interface web permettant aux chercheurs de téléverser des données de spectrométrie de masse et d’obtenir des séquences d’anticorps reconstituées et des cartes de couverture sans matériel spécialisé ni configuration complexe.
Ce que cela signifie pour les futurs médicaments à base d’anticorps
XA-Novo démontre qu’il est désormais possible de lire des séquences d’anticorps complètes et très précises directement à partir d’échantillons protéiques, même en présence de mélanges, en utilisant des quantités modestes de matériel et un flux de travail largement automatisé. Pour les non‑spécialistes, cela signifie que les anticorps prometteurs découverts en laboratoire ou en clinique peuvent être rétroconçus plus rapidement, reproduits de façon fiable et optimisés. En rendant le séquençage des anticorps plus rapide, plus évolutif et moins dépendant de lignées cellulaires fragiles, XA-Novo pourrait accélérer les études fondamentales en immunologie, aider à suivre les réponses immunitaires aux infections comme le COVID‑19, et accélérer le développement et l’optimisation des thérapies à base d’anticorps.
Citation: Xiong, Y., Jiang, W., Xiao, J. et al. XA-Novo: high-throughput mass spectrometry-based de novo sequencing technology for monoclonal antibodies and antibody mixtures. Nat Commun 17, 3391 (2026). https://doi.org/10.1038/s41467-026-70496-y
Mots-clés: séquençage d’anticorps, spectrométrie de masse, anticorps monoclonaux, anticorps neutralisants du COVID-19, ingénierie des protéines