Clear Sky Science · nl
XA-Novo: hoogdoorvoerde massaspectrometrie-gebaseerde de-novo sequentiebepalingstechnologie voor monoklonale antilichamen en antilichaammengsels
Waarom het ontcijferen van antilichamen ertoe doet
Antilichamen zijn kleine Y‑vormige eiwitten die virussen, bacteriën en zelfs kankercellen met opmerkelijke precisie herkennen. Om ze om te zetten in krachtige geneesmiddelen of diagnostische hulpmiddelen hebben wetenschappers de exacte aminozuur"spelling"—de sequentie—nodig. Het lezen van die sequentie is vaak traag, duur en soms onmogelijk met de huidige DNA‑gebaseerde methoden. Deze studie introduceert XA‑Novo, een nieuwe technologie die antilichaamsequenties direct van de eiwitten zelf leest met behulp van massaspectrometrie en slimme algoritmen, waardoor het proces sneller, nauwkeuriger en toepasbaar op complexe antilichaammengsels wordt.
Huidige obstakels bij het lezen van antilichaamrecepten
Traditionele methoden om antilichamen te decoderen beginnen meestal bij de cellen die ze produceren. Onderzoekers kweken hybridomacellen of isoleren B‑cellen, halen hun genetisch materiaal eruit en sequencen vervolgens het DNA of RNA. Deze benaderingen kunnen weken tot maanden duren, vereisen levende cellen die fragiel of verloren kunnen gaan, en laten soms nog steeds hiaten of fouten achter. Ze hebben ook moeite te laten zien hoe de antilichamen die in bloed of slijm zweven werkelijk gerelateerd zijn aan de B‑celpopulatie die ze produceerde. Een alternatief is werken op eiwitniveau: antilichamen in kleine stukjes breken en die analyseren met massaspectrometrie. Toch vereisen bestaande massaspectrometriemethoden vaak grote hoeveelheden monster, hebben ze een lage doorvoer en kunnen ze sequenties verkeerd samenvoegen, vooral wanneer veel vergelijkbare antilichamen samen aanwezig zijn.
Een nieuwe pijplijn die bij eiwitten begint
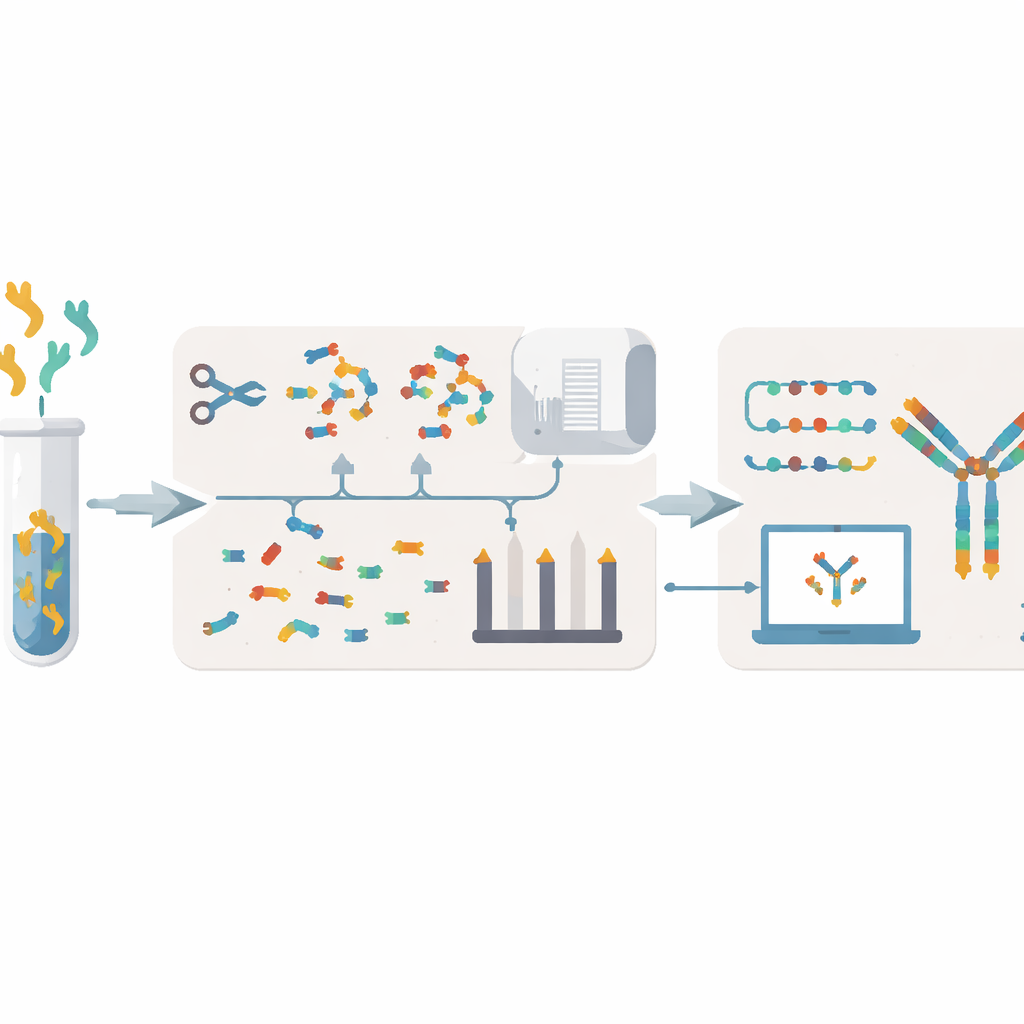
XA‑Novo pakt deze problemen aan door verbeterde chemie, geavanceerde massaspectrometrie en moderne machine learning te combineren in één gestroomlijnde workflow. Eerst worden antilichamen zacht maar grondig in overlappende peptidenfragmenten geknipt met een "single‑pot multi‑enzymatic gradient digestion"‑strategie, waarbij vijf verschillende enzymen op tijdgestaggerde wijze werken. Dit vergroot de diversiteit en overlap van fragmenten zonder kostbaar monster te verspillen. Vervolgens worden deze fragmenten geanalyseerd met hoogresolutie massaspectrometrie onder twee aanvullende fragmentatiemodi, wat rijke spectrale informatie oplevert over hoe elk peptide uiteenvalt.
Deep learning en slimme assemblage
Zodra spectra zijn verzameld gebruikt XA‑Novo een deep‑learningmodel genaamd Casanovo om de complexe patronen van massasignalen te vertalen naar voorspelde peptidesequenties, vergelijkbaar met een taalmodel dat tussen talen vertaalt. Deze vele korte "reads" worden daarna doorgegeven aan een nieuwe assembler genaamd Fusion. Fusion gebruikt een beam‑searchstrategie en informatie uit bekende antilichaamtemplates om overlappende peptiden aan elkaar te rijgen tot volledige zware en lichte ketens. Het is ontworpen om veelvoorkomende probleemzones aan te kunnen—zoals aminozuren met vrijwel identieke massa's en regio's waar antilichamen het meest variëren voor binding, de zogenoemde complementarity‑determining regions—terwijl het gaten, inserties en verkeerd geordende stukken vermijdt die de functie kunnen aantasten.
De methode aan de tand gevoeld
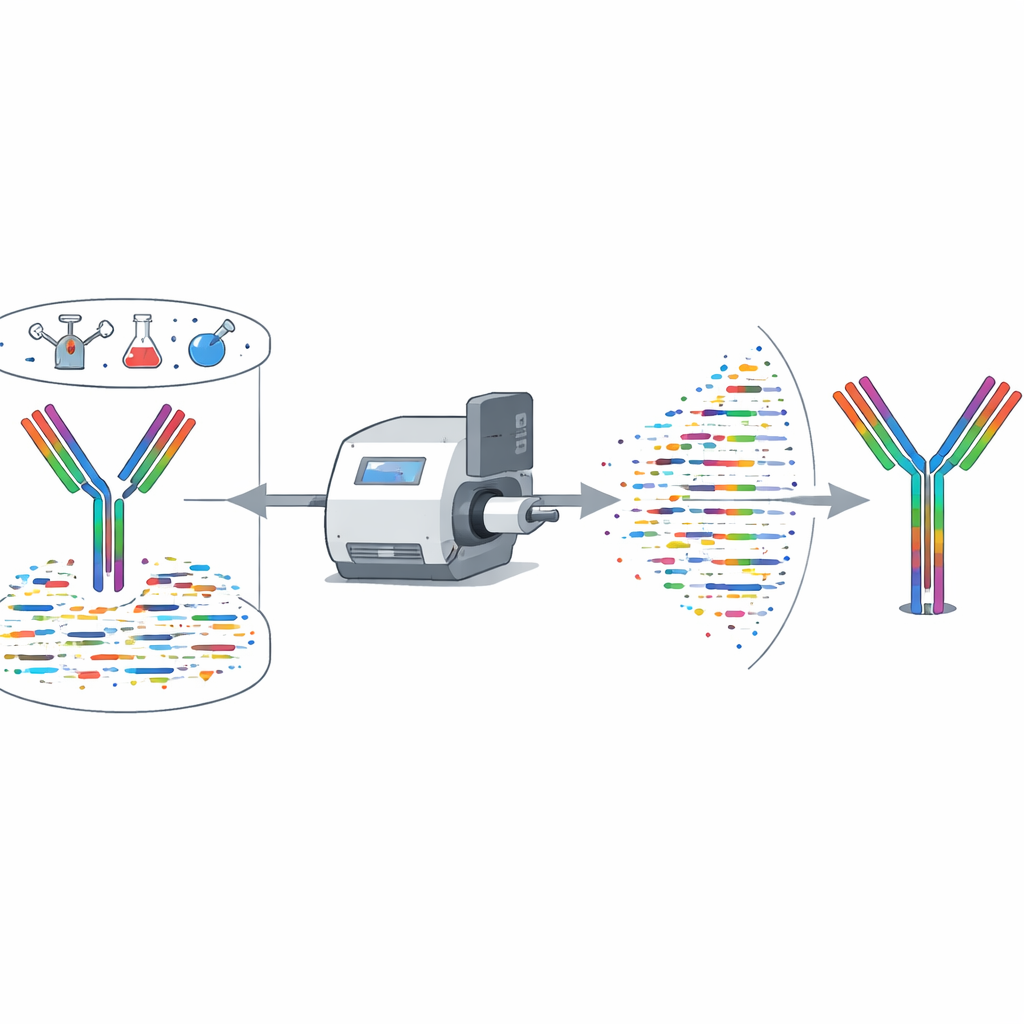
De auteurs hebben XA‑Novo grondig gebenchmarkt op antilichamen met bekende sequenties van mensen en muizen, inclusief verschillende die SARS‑CoV‑2 neutraliseren. Vergeleken met commerciële tools en openbare algoritmen behaalde XA‑Novo consequent hogere sequentiedekking en nauwkeurigheid, met volledige en foutloze reconstructie in kritieke bindingsregio's. Het werkte betrouwbaar zelfs bij aanvang met slechts 50 microgram antilichaam. Het team ging vervolgens aan de slag met zes therapeutische antilichamen waarvan de sequenties niet publiekelijk beschikbaar waren. XA‑Novo decodeerde hun zware en lichte ketens, de sequenties werden gekloond en tot expressie gebracht, en de resulterende antilichamen werden in muizen getest. In vivo‑experimenten toonden dat deze gereconstrueerde antilichamen hun doelimmuuncellen of macrofagen even effectief verminderden als de oorspronkelijke commerciële versies, wat bevestigt dat de gedecodeerde sequenties functioneel correct waren.
Het gelijktijdig afhandelen van antilichaammengsels
Veel reële monsters bevatten mengsels van antilichamen in plaats van een enkel, zuiver exemplaar. XA‑Novo werd getest met mengsels van twee of drie COVID‑19 neutraliserende antilichamen tegelijk, voor zowel menselijke als muizenantilichamen. Het systeem herstelde de sequentie van elk component met minstens 99,54% nauwkeurige dekking, en vaak 100%, inclusief de meest variabele bindingslussen. Deze prestatie overtreft bestaande assemblers die doorgaans beperkt zijn tot individuele antilichamen. De auteurs bouwden ook een webgebaseerde interface zodat onderzoekers massaspectrometriegegevens kunnen uploaden en gereconstrueerde antilichamsequenties en dekkingskaarten kunnen verkrijgen zonder gespecialiseerde hardware of complexe inrichting.
Wat dit betekent voor toekomstige antilichaamgeneesmiddelen
XA‑Novo laat zien dat het nu mogelijk is volledige, zeer nauwkeurige antilichamsequenties rechtstreeks uit eiwitmonsters te lezen, zelfs in mengsels, met bescheiden materiaalhoeveelheden en een grotendeels geautomatiseerde workflow. Voor niet‑specialisten betekent dit dat veelbelovende antilichamen die in het lab of de kliniek worden ontdekt sneller reverse‑engineered, betrouwbaar gereproduceerd en verder geoptimaliseerd kunnen worden. Door antilichaamsequenering sneller, beter schaalbaar en minder afhankelijk van kwetsbare cellijnen te maken, kan XA‑Novo fundamenteel immunologisch onderzoek versnellen, helpen immuunresponsen op infecties zoals COVID‑19 te volgen en de ontwikkeling en optimalisatie van antilichaamgebaseerde therapieën bespoedigen.
Bronvermelding: Xiong, Y., Jiang, W., Xiao, J. et al. XA-Novo: high-throughput mass spectrometry-based de novo sequencing technology for monoclonal antibodies and antibody mixtures. Nat Commun 17, 3391 (2026). https://doi.org/10.1038/s41467-026-70496-y
Trefwoorden: antilichaamsequenering, massaspectrometrie, monoklonale antilichamen, COVID-19 neutraliserende antilichamen, eiwittenengineering