Clear Sky Science · de
XA-Novo: Hochdurchsatz-De‑novo-Sequenzierungstechnologie basierend auf Massenspektrometrie für monoklonale Antikörper und Antikörpergemische
Warum das Entschlüsseln von Antikörpern wichtig ist
Antikörper sind winzige, Y‑förmige Proteine, die Viren, Bakterien und sogar Krebszellen mit bemerkenswerter Präzision erkennen. Um sie in leistungsfähige Wirkstoffe oder Diagnostika zu verwandeln, brauchen Forschende ihre genaue Aminosäure‑„Schreibweise“—also die Sequenz. Das Auslesen dieser Sequenz ist jedoch oft langsam, teuer und mit aktuellen DNA‑basierten Methoden manchmal unmöglich. Diese Studie stellt XA‑Novo vor, eine neue Technologie, die Antikörpersequenzen direkt aus den Proteinen liest und dabei Massenspektrometrie und intelligente Algorithmen nutzt, um schneller, genauer und sogar für komplexe Antikörpergemische zu arbeiten.
Aktuelle Hindernisse beim Lesen von Antikörperrezepten
Traditionelle Methoden zur Entschlüsselung von Antikörpern beginnen in der Regel bei den Zellen, die sie produzieren. Forschende kultivieren Hybridomzellen oder isolieren B‑Zellen, extrahieren deren genetisches Material und sequenzieren dann DNA oder RNA. Diese Ansätze können Wochen bis Monate dauern, benötigen lebende Zellen, die empfindlich sein oder verloren gehen können, und hinterlassen manchmal Lücken oder Fehler. Zudem fällt es ihnen schwer, eindeutig zuzuordnen, wie die in Blut oder Schleim nachweisbaren Antikörper tatsächlich zur B‑Zell‑Population stehen, die sie produziert hat. Eine Alternative ist, auf Proteinebene zu arbeiten: Antikörper werden in kleine Stücke zerlegt und mittels Massenspektrometrie analysiert. Bestehende Massenspektrometrie‑Methoden benötigen jedoch oft große Probenmengen, haben eine geringe Durchsatzrate und können Sequenzen falsch zusammensetzen—insbesondere wenn viele ähnliche Antikörper zusammen vorliegen.
Eine neue Pipeline, die bei Proteinen ansetzt
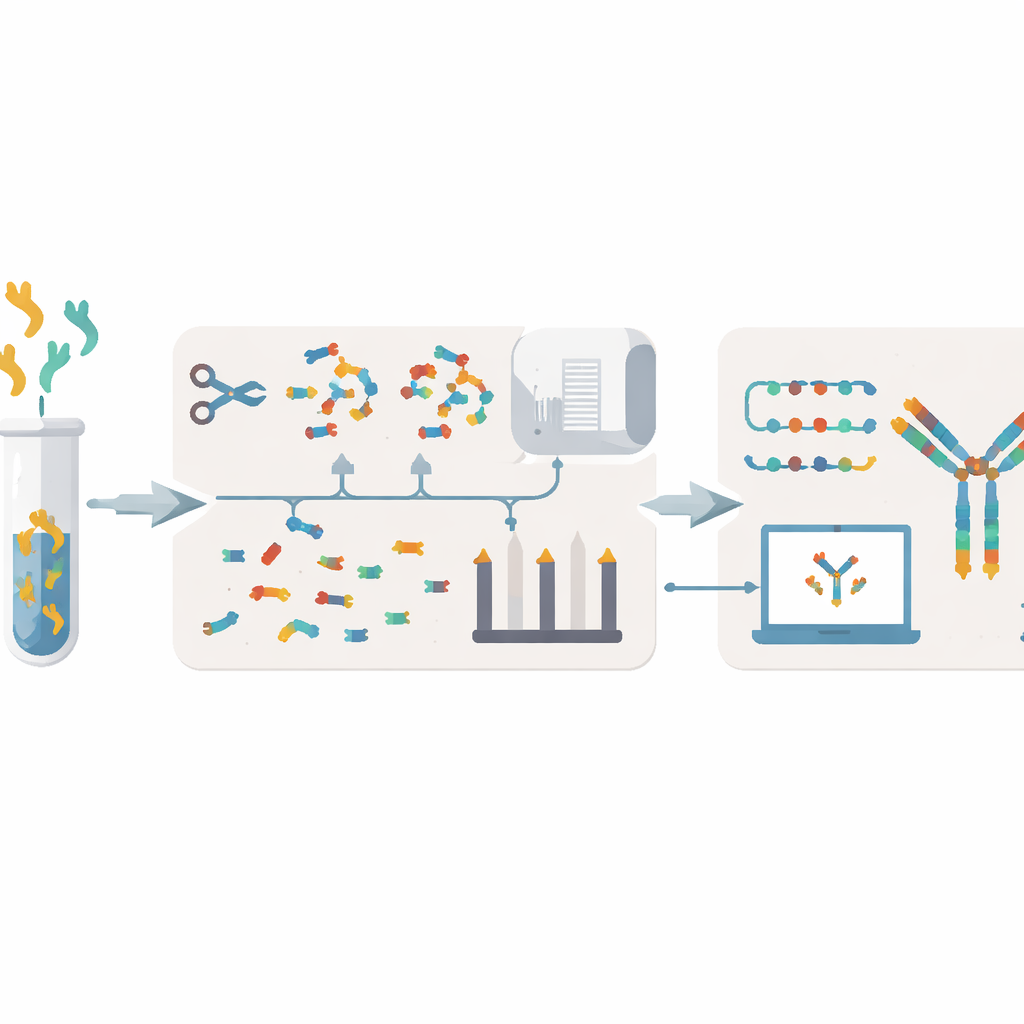
XA‑Novo begegnet diesen Problemen, indem es verbesserte Chemie, moderne Massenspektrometrie und maschinelles Lernen in einen schlanken Arbeitsablauf integriert. Zuerst werden Antikörper schonend, aber gründlich in überlappende Peptidfragmente zerteilt, mithilfe einer „Single‑Pot Multi‑Enzymatic Gradient Digestion“‑Strategie, bei der fünf verschiedene Enzyme zeitlich gestaffelt wirken. Das erhöht die Vielfalt und Überlappung der Fragmente, ohne kostbares Material zu verschwenden. Anschließend werden diese Fragmente mittels hochauflösender Massenspektrometrie unter zwei komplementären Fragmentierungsmodi analysiert, wodurch reichhaltige Spektralinformationen entstehen, die zeigen, wie jedes Peptid zerfällt.
Deep Learning und intelligentes Zusammensetzen
Sobald die Spektren erfasst sind, nutzt XA‑Novo ein Deep‑Learning‑Modell namens Casanovo, um die komplexen Muster der Massensignale in vorhergesagte Peptidsequenzen zu übersetzen—ähnlich wie ein Sprachmodell beim Übersetzen zwischen Sprachen. Diese vielen kurzen „Reads“ werden dann an einen neuen Assembler namens Fusion übergeben. Fusion verwendet eine Beam‑Search‑Strategie und Informationen aus bekannten Antikörpervorlagen, um überlappende Peptide zu vollständigen schweren und leichten Ketten zusammenzufügen. Das System ist darauf ausgelegt, häufige Problemstellen zu bewältigen—wie Aminosäuren mit nahezu identischer Masse und die Bereiche, in denen Antikörper am stärksten variieren für die Bindung, die sogenannten komplementaritätsbestimmenden Regionen—während es Lücken, Insertionen und falsch geordnete Abschnitte vermeidet, die die Funktion zerstören könnten.
Das Verfahren auf die Probe gestellt
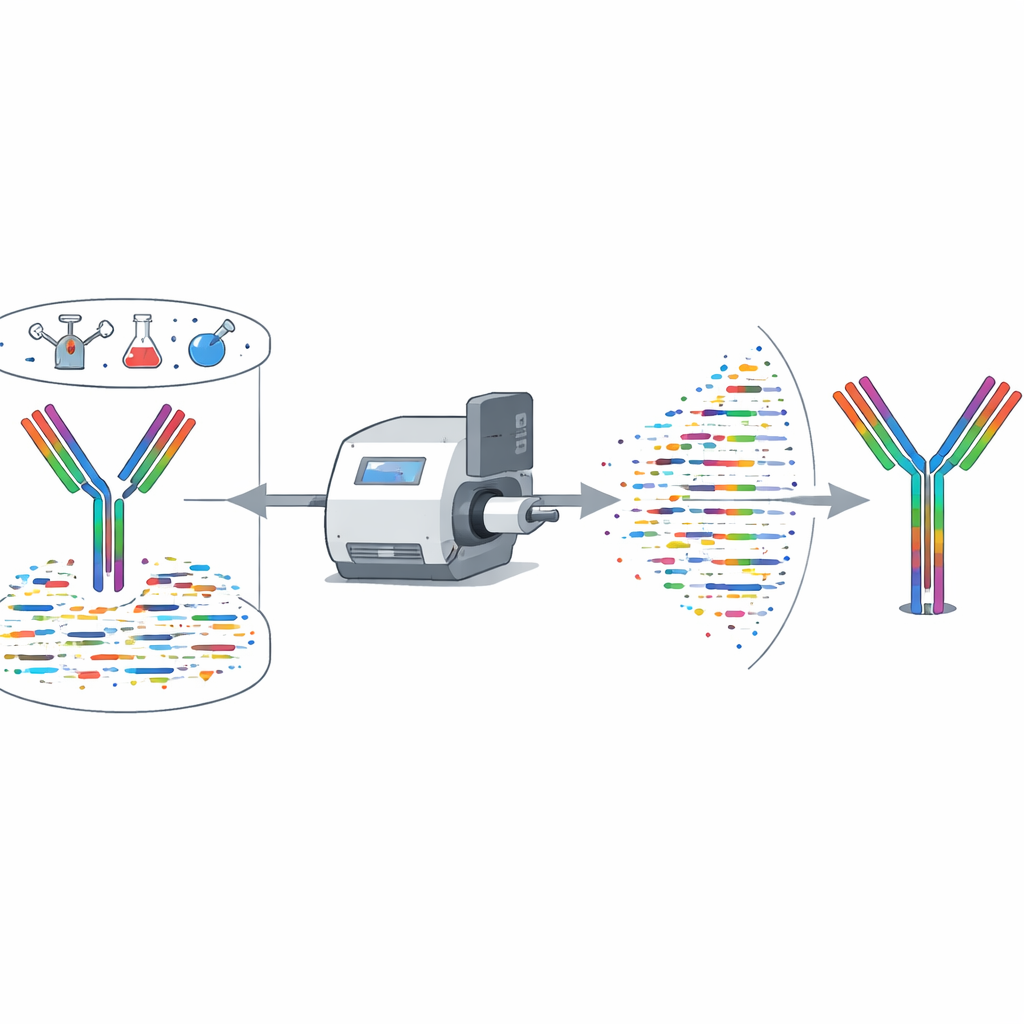
Die Autorinnen und Autoren haben XA‑Novo rigoros an Antikörpern mit bekannten Sequenzen aus Mensch und Maus getestet, einschließlich mehrerer SARS‑CoV‑2‑neutralisierender Antikörper. Im Vergleich zu kommerziellen Tools und öffentlich verfügbaren Algorithmen erzielte XA‑Novo durchgehend höhere Sequenzabdeckung und Genauigkeit, mit vollständiger und fehlerfreier Rekonstruktion in kritischen Bindungsregionen. Es funktionierte zuverlässig selbst bei Startmengen von nur 50 Mikrogramm Antikörper. Anschließend wurden sechs therapeutische Antikörper untersucht, deren Sequenzen nicht öffentlich waren. XA‑Novo entschlüsselte ihre schweren und leichten Ketten; die Sequenzen wurden kloniert und exprimiert, und die resultierenden Antikörper in Mäusen getestet. In‑vivo‑Experimente zeigten, dass diese rekonstruierten Antikörper Ziel‑Immunzellen oder Makrophagen genauso effektiv dezimierten wie die ursprünglichen kommerziellen Versionen, was bestätigt, dass die entschlüsselten Sequenzen funktionell korrekt waren.
Gleichzeitige Verarbeitung von Antikörpergemischen
Viele Proben aus der Praxis enthalten Gemische von Antikörpern statt eines einzelnen reinen Antikörpers. XA‑Novo wurde mit Mischungen aus zwei oder drei COVID‑19‑neutralisierenden Antikörpern gleichzeitig herausgefordert, sowohl für humane als auch für murine Antikörper. Das System rekonstruierte die Sequenz jedes Bestandteils mit mindestens 99,54 % korrekter Abdeckung und häufig 100 %, einschließlich der variabelsten Bindungsschleifen. Diese Leistung übertrifft bestehende Assembler, die typischerweise auf einzelne Antikörper beschränkt sind. Die Autorinnen und Autoren haben außerdem eine webbasierte Benutzeroberfläche geschaffen, über die Forschende Massenspektrometrie‑Daten hochladen und rekonstruktierte Antikörpersequenzen sowie Abdeckungs‑Karten ohne spezielle Hardware oder komplexe Einrichtung erhalten können.
Was das für zukünftige Antikörpermedikamente bedeutet
XA‑Novo zeigt, dass es jetzt möglich ist, vollständige, hochpräzise Antikörpersequenzen direkt aus Proteinproben auszulesen—selbst in Gemischen—unter Verwendung moderater Materialmengen und eines weitgehend automatisierten Workflows. Für Nicht‑Spezialistinnen und -Spezialisten bedeutet das, dass vielversprechende Antikörper, die im Labor oder in klinischen Proben entdeckt wurden, schneller rückentwickelt, zuverlässig reproduziert und in verbesserte Versionen überführt werden können. Indem die Antikörpersequenzierung schneller, skalierbarer und weniger abhängig von empfindlichen Zelllinien wird, könnte XA‑Novo Grundlagenforschung in der Immunologie beschleunigen, helfen, Immunantworten auf Infektionen wie COVID‑19 nachzuverfolgen, und die Entwicklung sowie Optimierung antikörperbasierter Therapien vorantreiben.
Zitation: Xiong, Y., Jiang, W., Xiao, J. et al. XA-Novo: high-throughput mass spectrometry-based de novo sequencing technology for monoclonal antibodies and antibody mixtures. Nat Commun 17, 3391 (2026). https://doi.org/10.1038/s41467-026-70496-y
Schlüsselwörter: Antikörpersequenzierung, Massenspektrometrie, monoklonale Antikörper, COVID-19-neutralisierende Antikörper, Proteinengineering