Clear Sky Science · es
XA-Novo: tecnología de secuenciación de novo basada en espectrometría de masas de alto rendimiento para anticuerpos monoclonales y mezclas de anticuerpos
Por qué importa decodificar los anticuerpos
Los anticuerpos son pequeñas proteínas con forma de Y que reconocen virus, bacterias e incluso células cancerosas con notable precisión. Para convertirlos en fármacos potentes o herramientas diagnósticas, los científicos necesitan su “ortografía” exacta de aminoácidos: su secuencia. Pero leer esa secuencia suele ser lento, caro y a veces imposible con los métodos actuales basados en ADN. Este estudio presenta XA-Novo, una nueva tecnología que lee las secuencias de anticuerpos directamente a partir de las proteínas, usando espectrometría de masas y algoritmos inteligentes para hacerlo más rápido, con mayor precisión e incluso en mezclas complejas de anticuerpos.
Obstáculos actuales para leer las “recetas” de los anticuerpos
Los métodos tradicionales para decodificar anticuerpos suelen partir de las células que los producen. Los investigadores cultivan hibridomas o aíslan linfocitos B, extraen su material genético y secuencian el ADN o ARN. Estos enfoques pueden tardar semanas o meses, requieren células vivas que pueden ser frágiles o perderse, y en ocasiones dejan huecos o errores. También tienen dificultades para determinar cómo se relacionan realmente los anticuerpos presentes en sangre o mucosas con la población de células B que los generó. Una alternativa es trabajar a nivel proteico, fragmentando los anticuerpos en péptidos pequeños y analizándolos por espectrometría de masas. Sin embargo, los métodos de espectrometría existentes a menudo necesitan grandes cantidades de muestra, tienen bajo rendimiento y pueden ensamblar mal las secuencias, especialmente cuando hay muchos anticuerpos similares presentes simultáneamente.
Un nuevo flujo de trabajo que parte de las proteínas
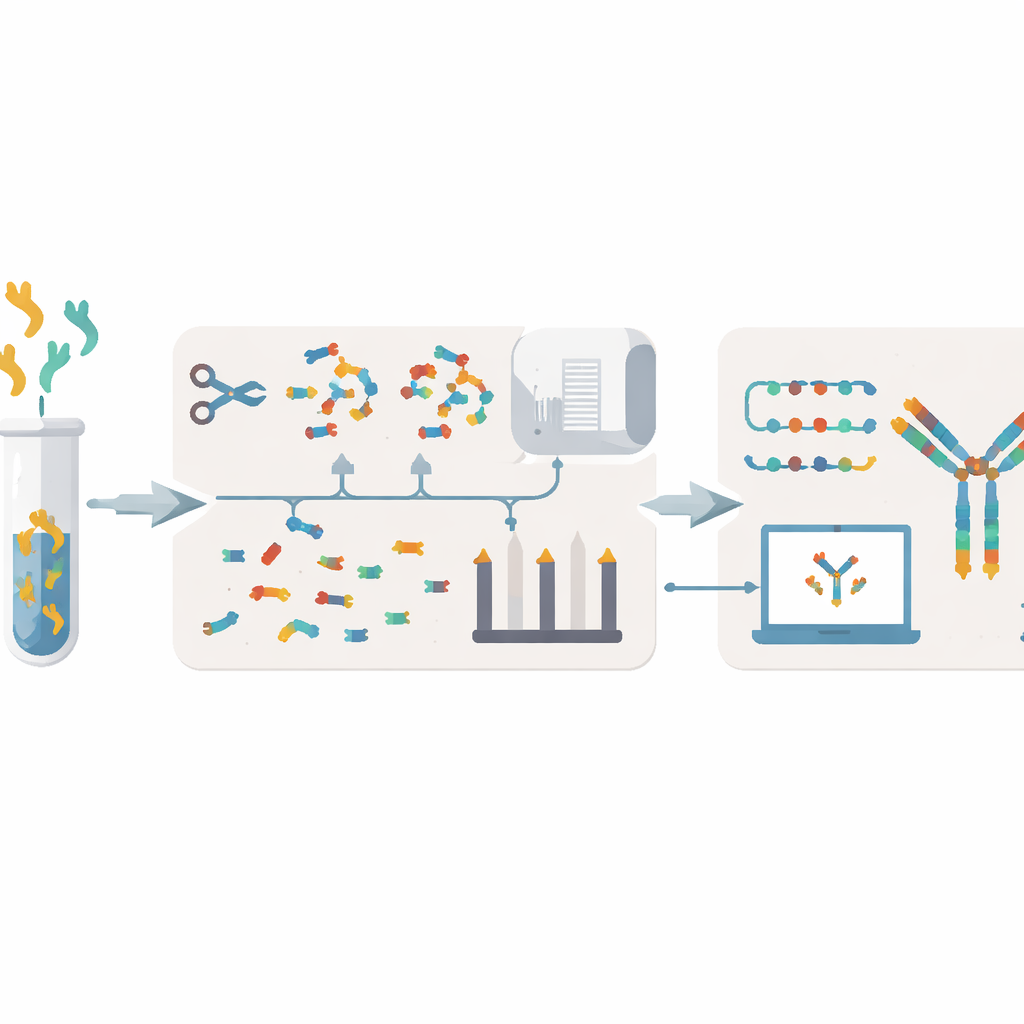
XA-Novo aborda estos problemas combinando química mejorada, espectrometría de masas avanzada y aprendizaje automático moderno en un flujo de trabajo integrado. Primero, los anticuerpos se fragmentan de forma suave pero exhaustiva en péptidos solapados mediante una estrategia de “digestión en gradiente multienzimática en una sola olla”, en la que cinco enzimas actúan de forma escalonada en el tiempo. Esto aumenta la diversidad y el solapamiento de los fragmentos sin desperdiciar muestra valiosa. A continuación, esos fragmentos se analizan por espectrometría de masas de alta resolución bajo dos modos complementarios de fragmentación, generando información espectral rica que captura cómo se descomponen cada uno de los péptidos.
Aprendizaje profundo y ensamblaje inteligente
Una vez recogidos los espectros, XA-Novo emplea un modelo de aprendizaje profundo llamado Casanovo para traducir los patrones complejos de picos de masa en secuencias de péptidos predichas, de forma similar a cómo un modelo de lenguaje traduce entre idiomas. Estas muchas “lecturas” cortas se pasan luego a un nuevo ensamblador llamado Fusion. Fusion utiliza una estrategia de búsqueda por haz (beam-search) y aprovecha información de plantillas de anticuerpos conocidas para unir péptidos solapados en cadenas pesadas y ligeras completas. Está diseñado para manejar puntos problemáticos comunes—como aminoácidos con masas casi idénticas y regiones donde los anticuerpos varían más para unirse (las regiones determinantes de la complementariedad)—al tiempo que evita huecos, inserciones y tramos mal ordenados que pueden arruinar la función.
Poniendo el método a prueba
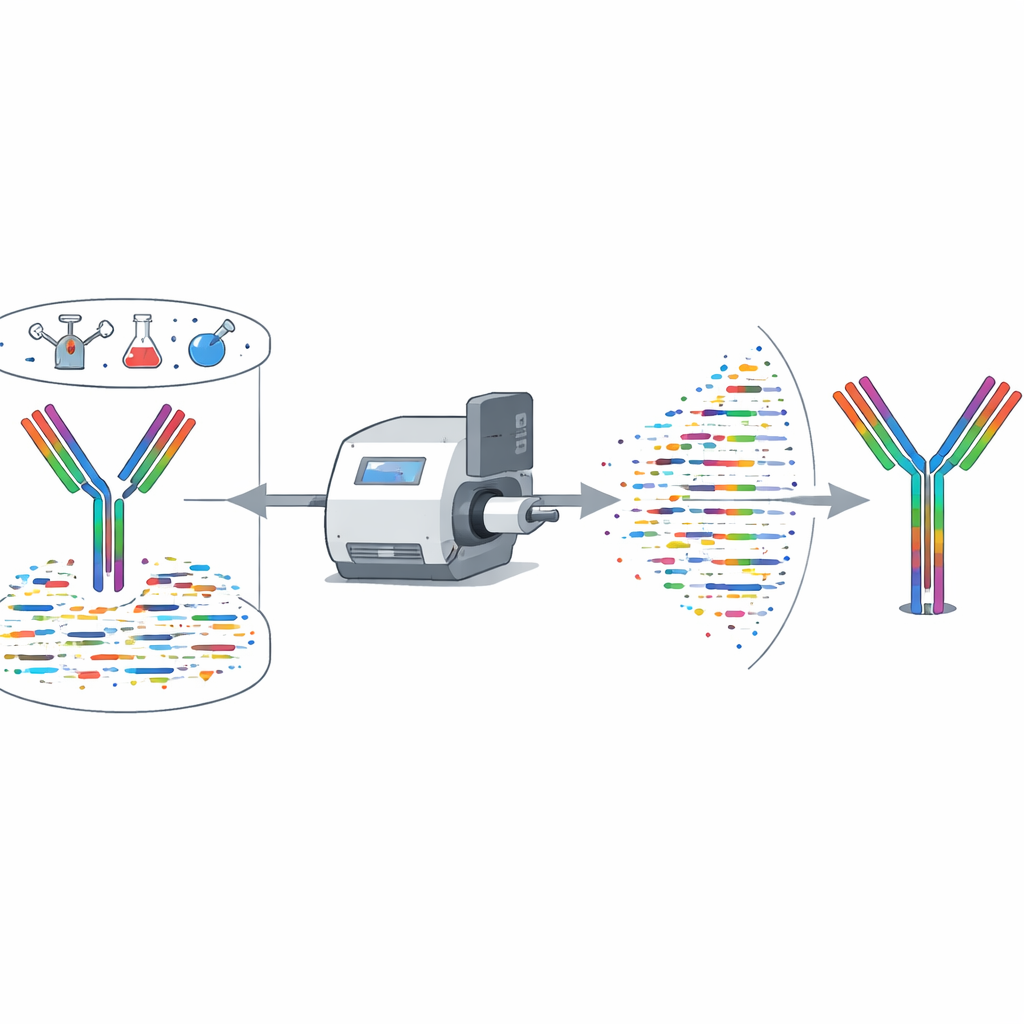
Los autores evaluaron rigurosamente XA-Novo en anticuerpos con secuencias conocidas de humanos y ratones, incluidos varios que neutralizan SARS-CoV-2. En comparación con herramientas comerciales y algoritmos públicos, XA-Novo logró de forma consistente mayor cobertura y precisión en las secuencias, con reconstrucciones completas y sin errores en regiones críticas de unión. Funcionó de manera fiable incluso partiendo de tan solo 50 microgramos de anticuerpo. El equipo también abordó seis anticuerpos terapéuticos cuyas secuencias no eran públicas. XA-Novo decodificó sus cadenas pesadas y ligeras; las secuencias se clonaron y expresaron, y los anticuerpos resultantes se probaron en ratones. Los experimentos in vivo mostraron que estos anticuerpos reconstruidos eliminaron sus células inmunes diana o macrófagos con la misma eficacia que las versiones comerciales originales, confirmando que las secuencias decodificadas eran funcionalmente correctas.
Procesar mezclas de anticuerpos a la vez
Muchas muestras del mundo real contienen mezclas de anticuerpos en lugar de uno solo y puro. XA-Novo fue desafiado con mezclas de dos o tres anticuerpos neutralizantes de COVID-19 a la vez, tanto humanos como de ratón. El sistema recuperó la secuencia de cada componente con al menos un 99,54% de cobertura precisa, y a menudo al 100%, incluidas las bucles de unión más variables. Este rendimiento supera a los ensambladores existentes, que normalmente están limitados a anticuerpos individuales. Los autores también desarrollaron una interfaz web para que los investigadores puedan subir datos de espectrometría de masas y obtener secuencias reconstruidas y mapas de cobertura sin necesidad de hardware especializado ni una configuración compleja.
Qué significa esto para los futuros medicamentos basados en anticuerpos
XA-Novo demuestra que ahora es posible leer secuencias completas y altamente precisas de anticuerpos directamente desde muestras proteicas, incluso en mezclas, utilizando cantidades moderadas de material y un flujo de trabajo en gran parte automatizado. Para los no especialistas, esto significa que los anticuerpos prometedores descubiertos en laboratorio o clínica pueden ser ingenierizados inversamente más rápido, reproducidos de forma fiable y optimizados para versiones mejoradas. Al hacer la secuenciación de anticuerpos más rápida, escalable y menos dependiente de líneas celulares frágiles, XA-Novo podría acelerar los estudios básicos de inmunología, ayudar a rastrear respuestas inmunitarias ante infecciones como COVID-19 y acelerar el desarrollo y la optimización de terapias basadas en anticuerpos.
Cita: Xiong, Y., Jiang, W., Xiao, J. et al. XA-Novo: high-throughput mass spectrometry-based de novo sequencing technology for monoclonal antibodies and antibody mixtures. Nat Commun 17, 3391 (2026). https://doi.org/10.1038/s41467-026-70496-y
Palabras clave: secuenciación de anticuerpos, espectrometría de masas, anticuerpos monoclonales, anticuerpos neutralizantes de COVID-19, ingeniería de proteínas