Clear Sky Science · tr
Adipogenezin sırasında PPARG2 aktivasyonunu kontrol eden kapsamlı enhancer etkileşimi
Yağ Hücresi Anahtarlarının Önemi
Yağ hücreleri sıklıkla obezitenin sorumlusu olarak gösterilir, ancak sağlıklı yağ dokusu enerjiyi güvenli şekilde depolamak ve kan şekeri ile kolesterolü dengede tutmak için gereklidir. Yağ hücreleri düzgün oluşamaz veya işlev görmezse yağ karaciğer, kas ve kalp gibi organlara sızar; bu da diyabet ve kalp hastalığı riskini artırır. Bu çalışma temel ama kritik bir soruyu soruyor: olgunlaşmamış bir hücreyi tam bir yağ hücresine dönüştürmek için tek bir anahtar gen nasıl tam zamanında açılır? Bu sorunun yanıtını ortaya koyarak çalışma, bazı insanların neden metabolik hastalıklara daha yatkın olabileceğini — ve genlerden uzak küçük DNA değişikliklerinin sağlığı nasıl derinden etkileyebileceğini — aydınlatıyor.
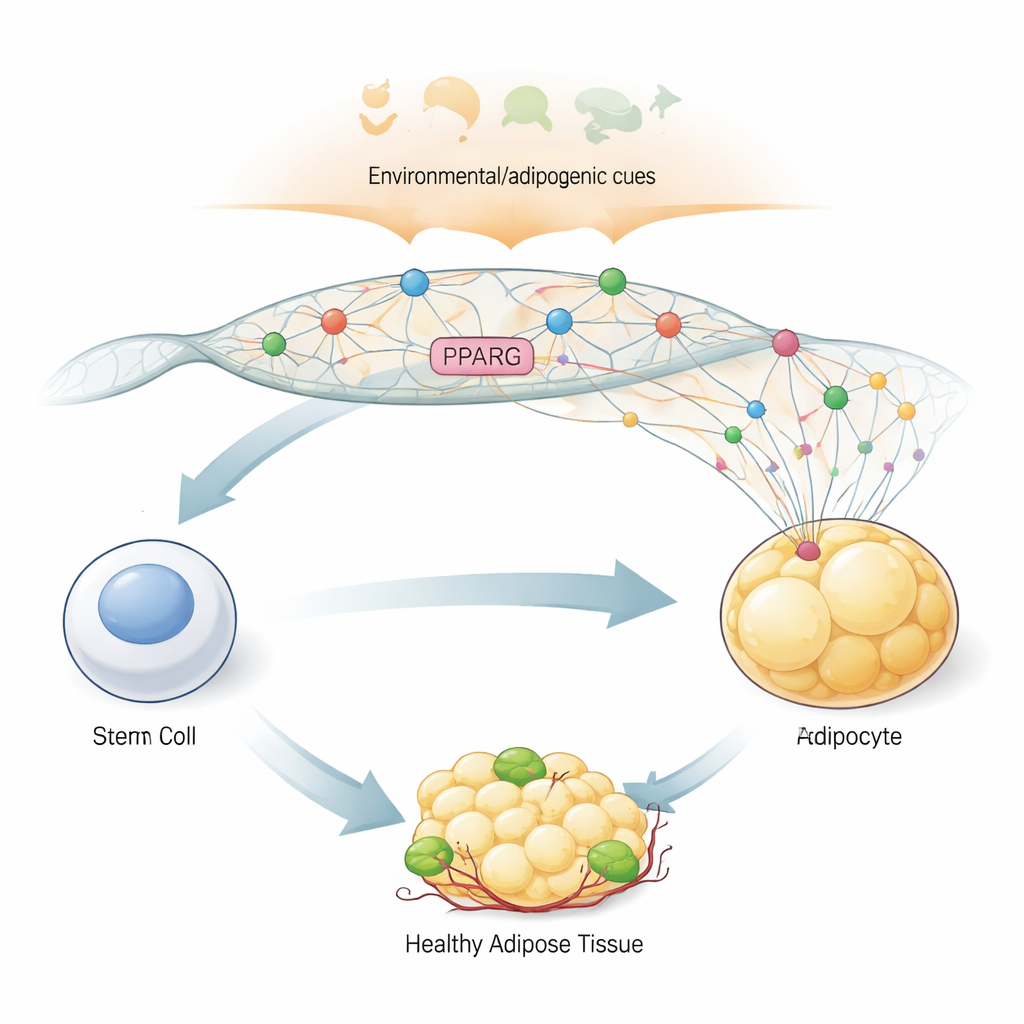
Yağ Hücresine Dönüşmenin Ana Anahtarı
Vücudun genel bir kök hücre benzeri hücreyi yağ hücresi haline getirmek için güvendiği “anahtar” gen PPARG2’dir; bu gen PPARγ2 proteininin üretimini sağlar. Bu protein, yağ depolama, insülin duyarlılığı ve yağ dokusundaki hormon üretimini yöneten yüzlerce başka geni kontrol eder. Merkezi rolü nedeniyle PPARG2, öncül hücrelerde kapalı kalmalı ve vücut “şimdi yağ hücresi yap” diyen adipojenik sinyaller gönderdiğinde hızla ve güçlü biçimde açılmalıdır. Yazarlar, laboratuvarda yağ hücrelerine yönlendirilebilen insan kemik iliği kaynaklı bir kök hücre modelini kullandılar; bu, farklılaşma sürecinde PPARG2 genom bölgesinin adım adım nasıl şekil değiştirdiğini ve etkinleştiğini izlemelerine olanak sağladı.
Değişime Hazırlıklı 3B Bir Komşuluk
PPARG2 geni, komşu genlerden fiziksel olarak izole edilmiş, alan olarak bilinen kendi kendine sınırlı 3B bir DNA komşuluğu içinde yer alır. Hücreler yağ olmaya karar vermeden çok önce bu bölge zaten “hazır”dır: DNA ve çevresindeki proteinlerdeki kimyasal işaretler, bir dizi kontrol elemanını — enhancer’ları — geleceğin düzenleyici merkezleri olarak işaretler. 3B genom haritalama yöntemleri kullanıldığında, araştırmacılar bu enhancer’ların uzun mesafelere yayılarak birbirleriyle iletişim kurduğunu ve PPARG2 etrafında sıkı bağlantılı bir topluluk oluşturduğunu buldular. Hücreler adipojenik sinyaller aldığında bu temaslar güçlenir, yeni etkinlik işaretleri belirir ve enhancer ağı PPARG2 promotörüne daha da odaklanır; bu da PPARG2 ifadesinde keskin bir artışla eşzamanlıdır.
Birçok Yardımcı, Az Yedek
Her bir enhancer’ın katkısını test etmek için ekip, CRISPR tabanlı genom düzenlemesi kullanarak PPARG2’nin yukarısında, yakınında ve aşağısında dağılmış dokuz ayrı enhancer segmentini sildi. Tek bir açma/kapama düğmesi bulmak yerine, bu enhancer’ların en az altısının tam PPARG2 aktivasyonu ve uygun yağ hücresi oluşumu için gerekli olduğunu keşfettiler. Bazı promotör-proksimal enhancer’ların veya büyük bir aşağı yönlü “süper-enhancer”ın parçalarının çıkarılması PPARG2 aktivitesini ciddi şekilde azaltmış ve ortaya çıkan hücrelerde lipid birikimini düşürmüştür. E+102 adı verilen bir aşağı yönlü enhancer özellikle kritik çıktı: onu silmek, genin geri kalanı ve diğer enhancer’lar sağlam olsa bile PPARG2’nin açılmasını neredeyse tamamen engelledi.
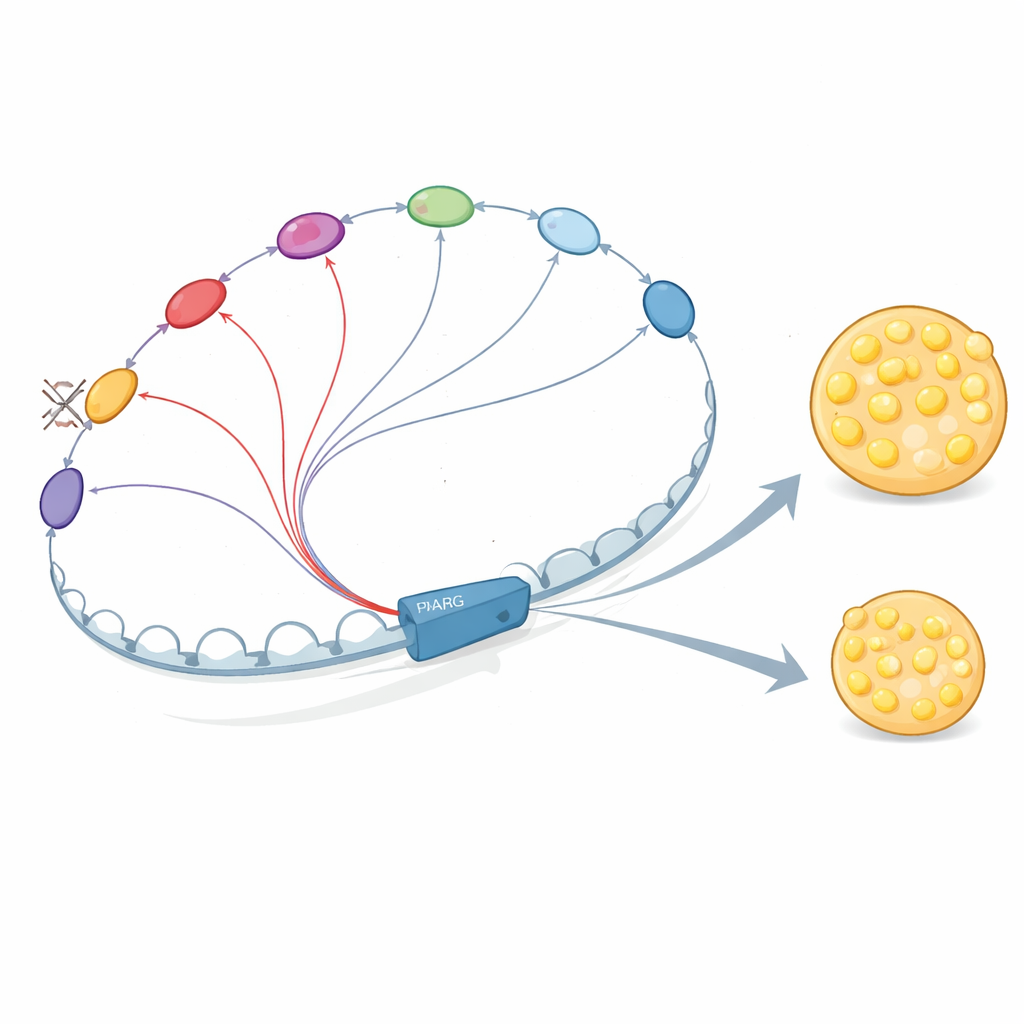
Enhancer’ların Karşılıklı Konuşması ve Güçlendirmesi
Bu DNA elemanları neden bu kadar birbirine bağımlı? Yazarlar, PPARG2 komşuluğundaki enhancer’ların izole davranmadığını gösteriyor. Bunlar erken etkili faktörler olan C/EBPβ gibi düzenleyici proteinleri ve daha sonra PPARγ ile C/EBPα’yı da içeren anahtar faktörleri çeker. Bu proteinler, fiziksel olarak birbirleriyle temas eden birden fazla enhancer’da bağlanarak birbirlerinin bağlanmasını stabilize eder ve transkripsiyonun başlamasına yardımcı olan Mediator kompleksinin işe alınmasını artırır. Araştırmacılar E+102’yi veya önemli bir promotör-proksimal enhancer’ı kaldırdıklarında, bu faktörlerin ve Mediator’ün bağlanması yalnızca silinen bölgede değil, bölgedeki diğer enhancer’larda da düşmüş ve 3B temas ağı zayıflamıştır. Bu da enhancer–enhancer “etkileşiminin” PPARG2 sinyalini yükselten işbirlikçi bir merkez oluşturduğunu destekler.
DNA Varyantlarından Hastalık Riskine
Son olarak çalışma, bu karmaşık kontrol sistemini insan metabolik hastalığı ile ilişkilendiriyor. Obezite, kolesterol düzeyleri veya tip 2 diyabetle ilişkili çoğu DNA varyantı genlerin dışında, enhancer gibi kodlamayan bölgelerde yer alır. Büyük genetik veri kümelerini genom regülasyonunun güçlü bir makine öğrenmesi modeliyle birleştirerek, yazarlar PPARG2 alanındaki en yüksek puanlı risk varyantlarının birçoğunun haritaladıkları en kritik enhancer’ların — E+102 ve promotör-proksimal bölgeler dahil — doğrudan içinde yer aldığını buldular. Bu varyantların bazıları, PPARγ veya diğer faktörlerin bağlanmasını nasıl etkilediği yönünde öngörülüyor — ve bir durumda gösteriliyor — bu da enhancer etkinliğini ve PPARG2 ifadesini ince biçimde değiştiriyor. Başka bir deyişle, bu enhancer ağındaki küçük oynamalar bir kişinin yağ hücrelerini daha sağlıklı veya daha az sağlıklı yönde itebilir.
Metabolik Sağlık İçin Anlamı
Günlük dilde bu çalışma, kilit yağ hücresi geni PPARG2’nin açılmasının tek bir anahtarın işi değil, üç boyutlu olarak birbirleriyle konuşan sıkı koordineli bir DNA kontrol elemanları takımı görevi olduğunu ortaya koyuyor. Özellikle önemli bir enhancer hem sürecin başlamasına yardımcı oluyor hem de PPARγ proteininin kendisinden gelen olumlu geri bildirimin başlıca hedefi olarak görev yaparak yağ hücresi kaderine hızlı ve sağlam bir bağlılık sağlıyor. Bu enhancer topluluğunun parçalarını zayıflatan genetik varyantlar PPARG2 aktivasyonunu düşürebilir, yağ hücresi oluşumunu veya işlevini bozabilir ve böylece kardiyometabolik hastalığa katkıda bulunabilir. Bu ağ tabanlı kontrol sistemini anlamak, riski daha hassas değerlendirme ve potansiyel olarak metabolik sağlığı iyileştirmek için yağ hücresi biyolojisini ayarlama yollarını açıyor.
Atıf: Cetnarowska, A., Hyldahl, M., Nygård, M. et al. Extensive enhancer crosstalk controls PPARG2 activation during adipogenesis. Nat Commun 17, 3824 (2026). https://doi.org/10.1038/s41467-026-70401-7
Anahtar kelimeler: PPARG2, enhancer'lar, adipogenez, gen regülasyonu, kardiyometabolik hastalık