Clear Sky Science · es
Extensa comunicación entre potenciadores controla la activación de PPARG2 durante la adipogénesis
Por qué importan los interruptores de las células grasas
Las células grasas suelen recibir la culpa por la obesidad, pero el tejido adiposo sano es esencial para almacenar energía de forma segura y mantener el azúcar y el colesterol en sangre en equilibrio. Cuando las células grasas no pueden formarse o funcionar correctamente, la grasa se filtra hacia el hígado, los músculos y el corazón, aumentando el riesgo de diabetes y enfermedad cardíaca. Este estudio plantea una pregunta básica pero crucial: ¿cómo se activa un gen clave en el momento justo para transformar una célula inmadura en una célula grasa totalmente formada? Al descubrir esa respuesta, el trabajo arroja luz sobre por qué algunas personas son más vulnerables a las enfermedades metabólicas y cómo pequeños cambios en el ADN, lejos de los genes, pueden tener grandes efectos en la salud.
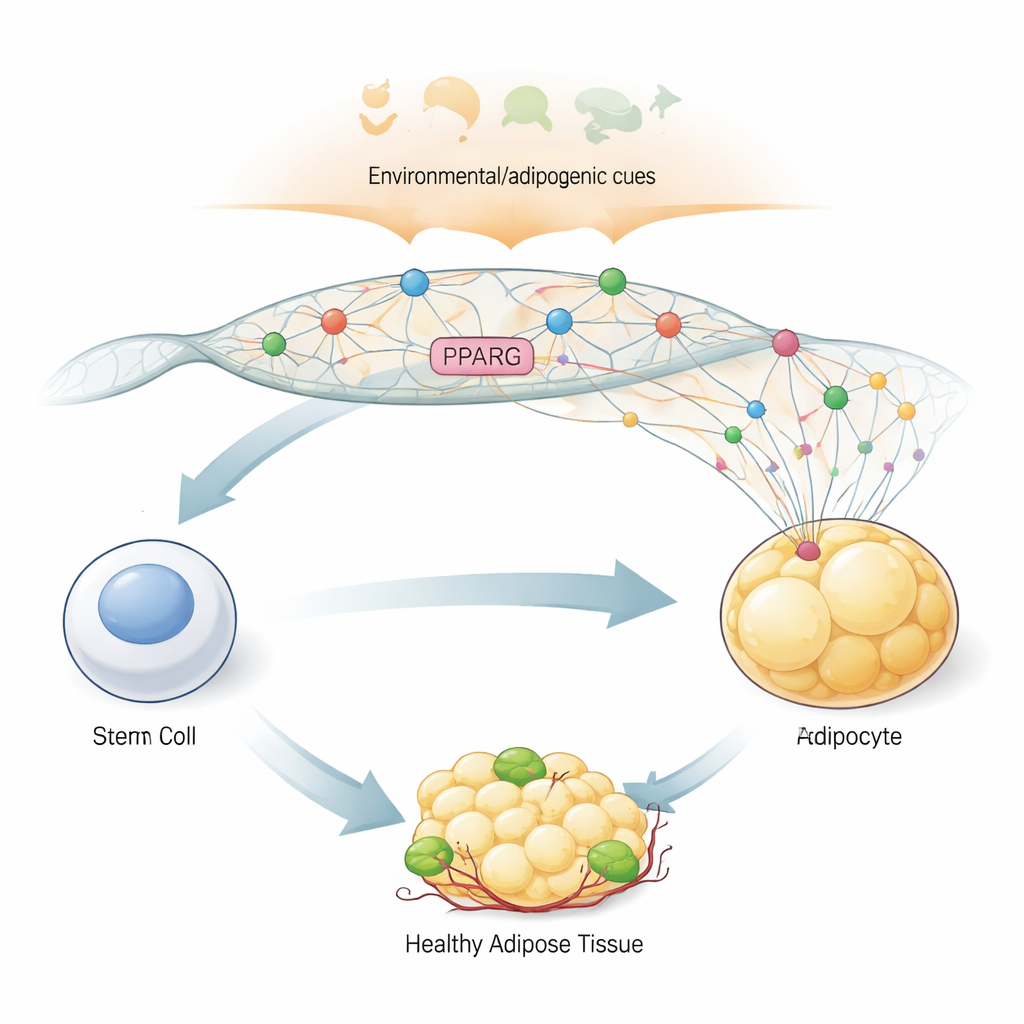
El interruptor maestro para convertirse en célula grasa
Para convertir una célula indiferenciada similar a una célula madre en una célula grasa, el organismo depende de un gen «interruptor maestro» llamado PPARG2, que produce la proteína PPARγ2. Esta proteína controla cientos de otros genes que regulan el almacenamiento de grasa, la sensibilidad a la insulina y la producción de hormonas en el tejido adiposo. Debido a su papel central, PPARG2 debe permanecer apagado en las células precursoras y después activarse de forma rápida y potente cuando el organismo envía señales adipogénicas que, en la práctica, dicen «formar células grasas ahora». Los autores utilizaron un modelo de células madre derivadas de médula ósea humana que puede inducirse a convertirse en células grasas en el laboratorio, lo que les permitió observar, paso a paso, cómo la región genómica de PPARG2 cambia de forma y actividad a medida que transcurre la diferenciación.
Un vecindario tridimensional preparado para el cambio
El gen PPARG2 se localiza dentro de un vecindario tridimensional de ADN autocontenido conocido como dominio, físicamente aislado de los genes circundantes. Incluso antes de que las células se comprometan a convertirse en adipocitos, esta región ya está «preparada»: marcas químicas en el ADN y en las proteínas circundantes señalan un conjunto de elementos reguladores, llamados potenciadores, como futuros puntos calientes regulatorios. Mediante métodos de cartografía del genoma en 3D, los investigadores encontraron que estos potenciadores ya se comunican entre sí a larga distancia, formando una comunidad estrechamente conectada alrededor de PPARG2. Cuando las células reciben señales adipogénicas, estos contactos se fortalecen, aparecen nuevas marcas de actividad y la red de potenciadores se orienta con mayor intensidad hacia el promotor de PPARG2, coincidiendo con un aumento pronunciado de la expresión de PPARG2.
Muchos colaboradores, pocas piezas prescindibles
Para evaluar la contribución de cada potenciador, el equipo usó edición genómica basada en CRISPR para eliminar nueve segmentos potenciadores individuales dispersos aguas arriba, cercanos y aguas abajo de PPARG2. En lugar de encontrar un único interruptor de encendido/apagado, descubrieron que al menos seis de estos potenciadores son esenciales para la activación completa de PPARG2 y la formación adecuada de células grasas. La eliminación de ciertos potenciadores cercanos al promotor o de fragmentos de un gran «superpotenciador» aguas abajo redujo considerablemente la actividad de PPARG2 y la acumulación de lípidos en las células resultantes. Un potenciador aguas abajo, denominado E+102, resultó especialmente crítico: su eliminación impidió casi por completo la activación de PPARG2, a pesar de que el resto del gen y otros potenciadores permanecían intactos.
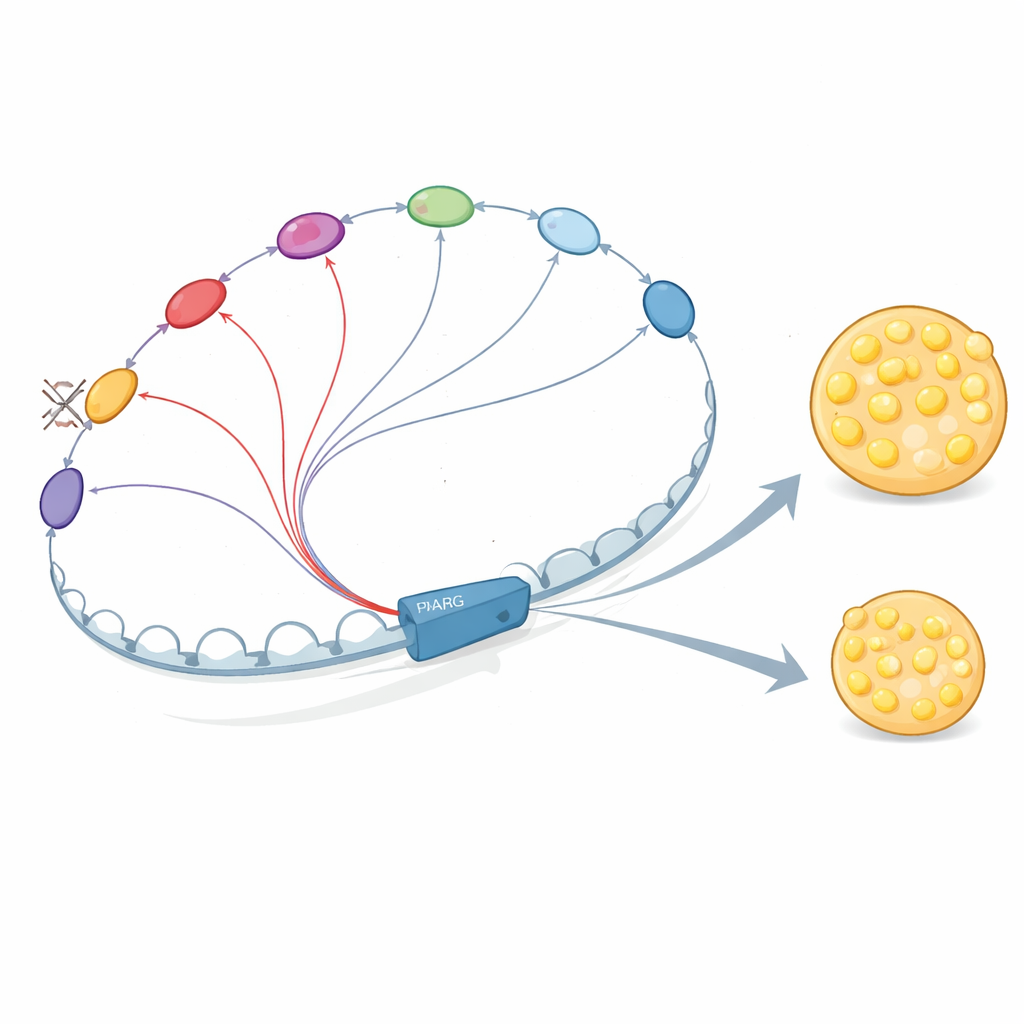
Potenciadores que se comunican y se refuerzan mutuamente
¿Por qué son tan interdependientes estos elementos de ADN? Los autores muestran que los potenciadores en el vecindario de PPARG2 no actúan de forma aislada. Reclutan proteínas reguladoras clave, incluidos factores de acción temprana como C/EBPβ y, más tarde, la propia PPARγ y C/EBPα. Estas proteínas se unen en múltiples potenciadores que mantienen contactos físicos entre sí, estabilizando la unión mutua y favoreciendo la captación del complejo Mediator, que ayuda a iniciar la transcripción. Cuando los investigadores eliminaron E+102 o un potenciador clave cercano al promotor, la unión de estos factores y del complejo Mediator disminuyó no solo en el sitio eliminado, sino también en otros potenciadores de la región, y la red de contactos 3D se debilitó. Esto respalda la imagen de que el «intercambio» entre potenciadores crea un centro cooperativo que amplifica la señal hacia PPARG2.
De las variantes del ADN al riesgo de enfermedad
Por último, el estudio vincula este intrincado sistema de control con la enfermedad metabólica humana. La mayoría de las variantes del ADN asociadas a la obesidad, los niveles de colesterol o la diabetes tipo 2 se localizan fuera de los genes, en regiones no codificantes como los potenciadores. Combinando grandes conjuntos de datos genéticos con un potente modelo de aprendizaje automático de la regulación genómica, los autores hallaron que muchas de las variantes de riesgo con mayor puntuación dentro del dominio de PPARG2 caen directamente dentro de los potenciadores más críticos que habían cartografiado, incluyendo E+102 y sitios cercanos al promotor. Se predice —y en un caso se ha demostrado— que algunas de estas variantes alteran la afinidad de unión de PPARγ u otros factores, modificando sutilmente la actividad de los potenciadores y la expresión de PPARG2. Dicho de otro modo, pequeños ajustes en esta red de potenciadores pueden empujar a las células grasas de una persona hacia un comportamiento más saludable o menos saludable.
Qué significa esto para la salud metabólica
En términos cotidianos, este trabajo revela que activar el gen clave de la célula grasa PPARG2 no es responsabilidad de un único interruptor, sino de un conjunto cuidadosamente coordinado de elementos de control del ADN que se comunican entre sí en tres dimensiones. Un potenciador especialmente importante tanto ayuda a iniciar el proceso como actúa como un objetivo principal del refuerzo positivo proporcionado por la propia proteína PPARγ, asegurando un compromiso rápido y robusto con el destino de célula grasa. Las variantes genéticas que debilitan partes de esta comunidad de potenciadores pueden reducir la activación de PPARG2, perjudicar la formación o función de las células grasas y, por tanto, contribuir a la enfermedad cardiometabólica. Comprender este sistema de control en red abre la puerta a formas más precisas de evaluar el riesgo y, potencialmente, de ajustar la biología de las células grasas para mejorar la salud metabólica.
Cita: Cetnarowska, A., Hyldahl, M., Nygård, M. et al. Extensive enhancer crosstalk controls PPARG2 activation during adipogenesis. Nat Commun 17, 3824 (2026). https://doi.org/10.1038/s41467-026-70401-7
Palabras clave: PPARG2, potenciadores, adipogénesis, regulación génica, enfermedad cardiometabólica