Clear Sky Science · sv
Omfattande interaktion mellan enhancers styr PPARG2-aktivering under adipogenes
Varför fettcellsbrytningar spelar roll
Fettceller får ofta skulden för fetma, men frisk fettvävnad är nödvändig för att lagra energi säkert och hålla blodsocker och kolesterol i balans. När fettceller inte kan bildas eller fungera korrekt läcker fett ut i levern, musklerna och hjärtat, vilket ökar risken för diabetes och hjärtsjukdom. Denna studie ställer en grundläggande men avgörande fråga: hur slås en nyckelgen på vid precis rätt tidpunkt för att omvandla en omogen cell till en fullt utvecklad fettcell? Genom att besvara den frågan belyser arbetet varför vissa människor är mer sårbara för metabola sjukdomar — och hur små DNA-förändringar långt från gener kan få stora effekter på hälsan.
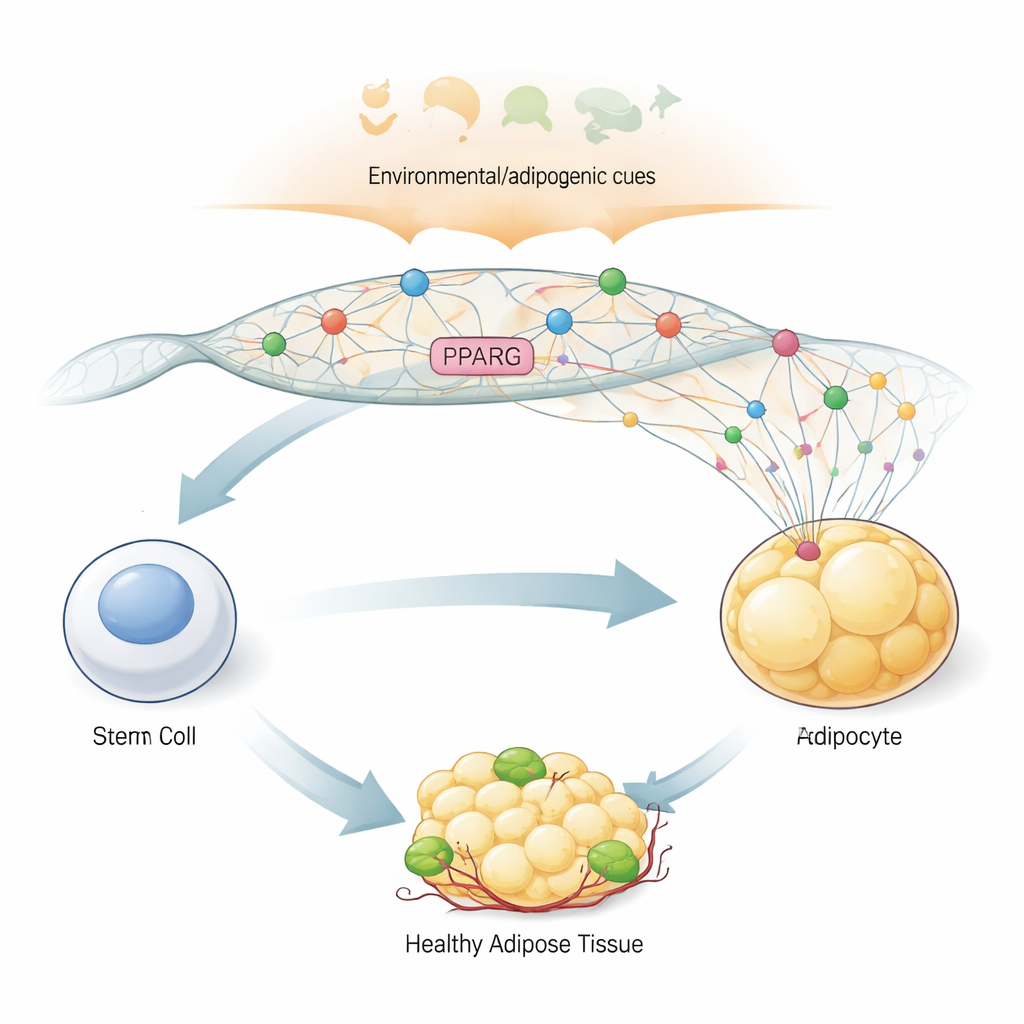
Huvudbrytaren för att bli en fettcell
För att förvandla en generisk stamlik cell till en fettcell förlitar sig kroppen på en ”huvudbrytare” gen kallad PPARG2, som kodar för proteinet PPARγ2. Detta protein styr hundratals andra gener som ansvarar för fettlagring, insulinkänslighet och hormonproduktion i fettvävnad. På grund av sin centrala roll måste PPARG2 hållas avstängd i prekursorceller och sedan slås på snabbt och kraftfullt när kroppen sänder adipogena signaler som i praktiken säger: ”bilda fettceller nu.” Författarna använde en mänsklig stamcellsmodell härledd från benmärg som kan riktas att bli fettceller i labbet, vilket gjorde det möjligt att steg för steg följa hur PPARG2-regionen i genomet förändrar form och aktivitet medan differentieringen fortskrider.
En tredimensionell stadsdel förberedd för förändring
PPARG2-genen ligger inom ett avskilt tredimensionellt DNA-område känt som en domän, fysiskt isolerat från omgivande gener. Redan innan cellerna bestämmer sig för att bli fett är den här regionen ”förprimad”: kemiska markörer på DNA och omgivande proteiner flaggar en uppsättning kontrollelement, kallade enhancers, som framtida regulatoriska knutpunkter. Med hjälp av 3D-genomkartläggningsmetoder fann forskarna att dessa enhancers redan kommunicerar med varandra över långa avstånd och bildar ett tätt kopplat nätverk kring PPARG2. När cellerna får adipogena signaler stärks dessa kontakter, nya aktivitetsmarkörer uppstår och enhancer-nätverket koncentrerar sig ännu mer mot PPARG2-promotorn, i takt med en skarp ökning av PPARG2-uttrycket.
Många hjälpande, få reserver
För att testa hur varje enhancer bidrar använde gruppen CRISPR-baserad genredigering för att ta bort nio enskilda enhancersegment spridda uppströms, nära och nedströms om PPARG2. Istället för att hitta en enda av- eller på-knapp upptäckte de att minst sex av dessa enhancers är nödvändiga för full PPARG2-aktivering och korrekt fettcellsbildning. Att ta bort vissa promoternära enhancers eller delar av en stor nedströms ”super-enhancer” dämpade kraftigt PPARG2-aktiviteten och minskade lipidackumulering i de resulterande cellerna. En nedströms enhancer, kallad E+102, var särskilt kritisk: dess borttagande hindrade nästan helt PPARG2 från att slås på, trots att resten av genen och andra enhancers förblev intakta.
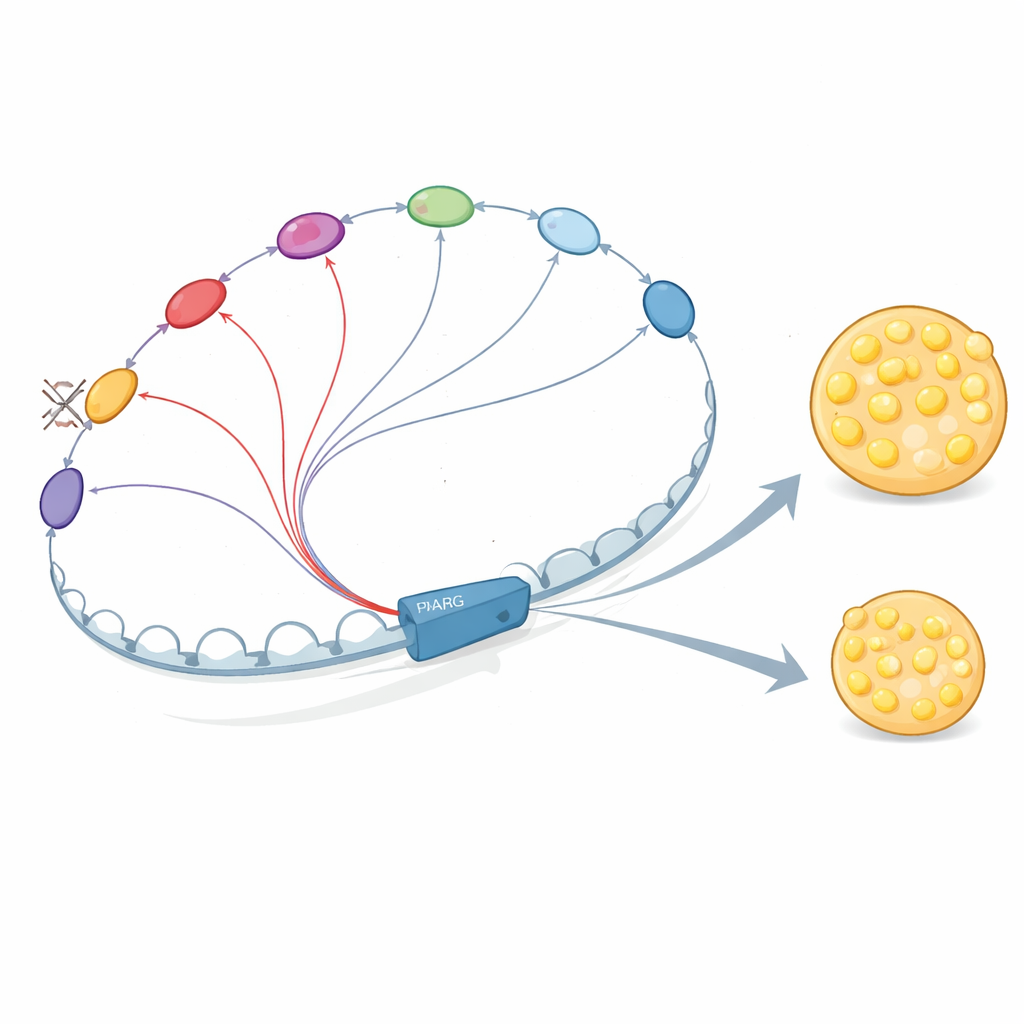
Enhancers som samtalar och förstärker varandra
Varför är dessa DNA-element så beroende av varandra? Författarna visar att enhancers i PPARG2-området inte verkar isolerat. De rekryterar nyckelregulatoriska proteiner, inklusive tidigt verkande faktorer som C/EBPβ och senare PPARγ själv samt C/EBPα. Dessa proteiner binder vid flera enhancers som fysiskt kontaktar varandra, vilket stabiliserar varandras bindning och ökar rekryteringen av Mediator-komplexet, som hjälper till att initiera transkription. När forskarna tog bort E+102 eller en viktig promoternära enhancer minskade bindningen av dessa faktorer och Mediator inte bara vid den borttagna platsen utan över andra enhancers i regionen, och det tredimensionella kontaktnätverket försvagades. Detta stöder en bild där enhancer–enhancer ”crosstalk” skapar en kooperativ nav som förstärker PPARG2-signalen.
Från DNA-varianter till sjukdomsrisk
Slutligen kopplar studien detta intrikata kontrollsystem till mänsklig metabol sjukdom. De flesta DNA-varianter som associeras med fetma, kolesterolnivåer eller typ 2-diabetes ligger utanför gener, i icke-kodande regioner som enhancers. Genom att kombinera stora genetiska dataset med en kraftfull maskininlärningsmodell för genomreglering fann författarna att många av de högst rankade riskvarianterna inom PPARG2-domänen faller direkt i de mest kritiska enhancers de kartlagt, inklusive E+102 och promoternära platser. Vissa av dessa varianter förväntas — och i ett fall visats — ändra hur väl PPARγ eller andra faktorer binder, vilket subtilt förändrar enhanceraktivitet och PPARG2-uttryck. Med andra ord kan små justeringar i detta enhancer-nätverk skjuta en persons fettceller mot mer eller mindre hälsosamt beteende.
Vad detta betyder för metabol hälsa
I vardagstermer visar detta arbete att aktiveringen av den centrala fettcellsgenen PPARG2 inte är en uppgift för en enda strömbrytare utan för ett tätt koreograferat team av DNA-kontrollelement som kommunicerar i tre dimensioner. En särskilt viktig enhancer hjälper både till att starta processen och fungerar därefter som ett huvudmål för positiv återkoppling från PPARγ-proteinet självt, vilket säkerställer ett snabbt och robust åtagande till fettcellsödet. Genetiska varianter som försvagar delar av detta enhancer-samhälle kan sänka PPARG2-aktiveringen, försämra bildning eller funktion av fettceller och därigenom bidra till kardiometabol sjukdom. Att förstå detta nätverksbaserade kontrollsystem öppnar dörren för mer precisa sätt att bedöma risk och möjligen finjustera fettcellsbiologin för att förbättra metabol hälsa.
Citering: Cetnarowska, A., Hyldahl, M., Nygård, M. et al. Extensive enhancer crosstalk controls PPARG2 activation during adipogenesis. Nat Commun 17, 3824 (2026). https://doi.org/10.1038/s41467-026-70401-7
Nyckelord: PPARG2, enhancers, adipogenes, genreglering, kardiometabolisk sjukdom