Clear Sky Science · ru
Обширное взаимодействие энхансеров контролирует активацию PPARG2 во время адипогенеза
Почему важны переключатели жировых клеток
Жировые клетки часто обвиняют в ожирении, но здоровая жировая ткань необходима для безопасного хранения энергии и поддержания баланса сахара и холестерина в крови. Когда жировые клетки не могут правильно формироваться или функционировать, жир попадает в печень, мышцы и сердце, повышая риск диабета и сердечных заболеваний. В этом исследовании ставится простой, но ключевой вопрос: как один важный ген включается в нужный момент, чтобы незрелая клетка превратилась в полноценную жировую клетку? Ответ проливает свет на то, почему некоторые люди более уязвимы к метаболическим болезням — и на то, как крошечные изменения в ДНК, расположенные далеко от генов, могут сильно влиять на здоровье.
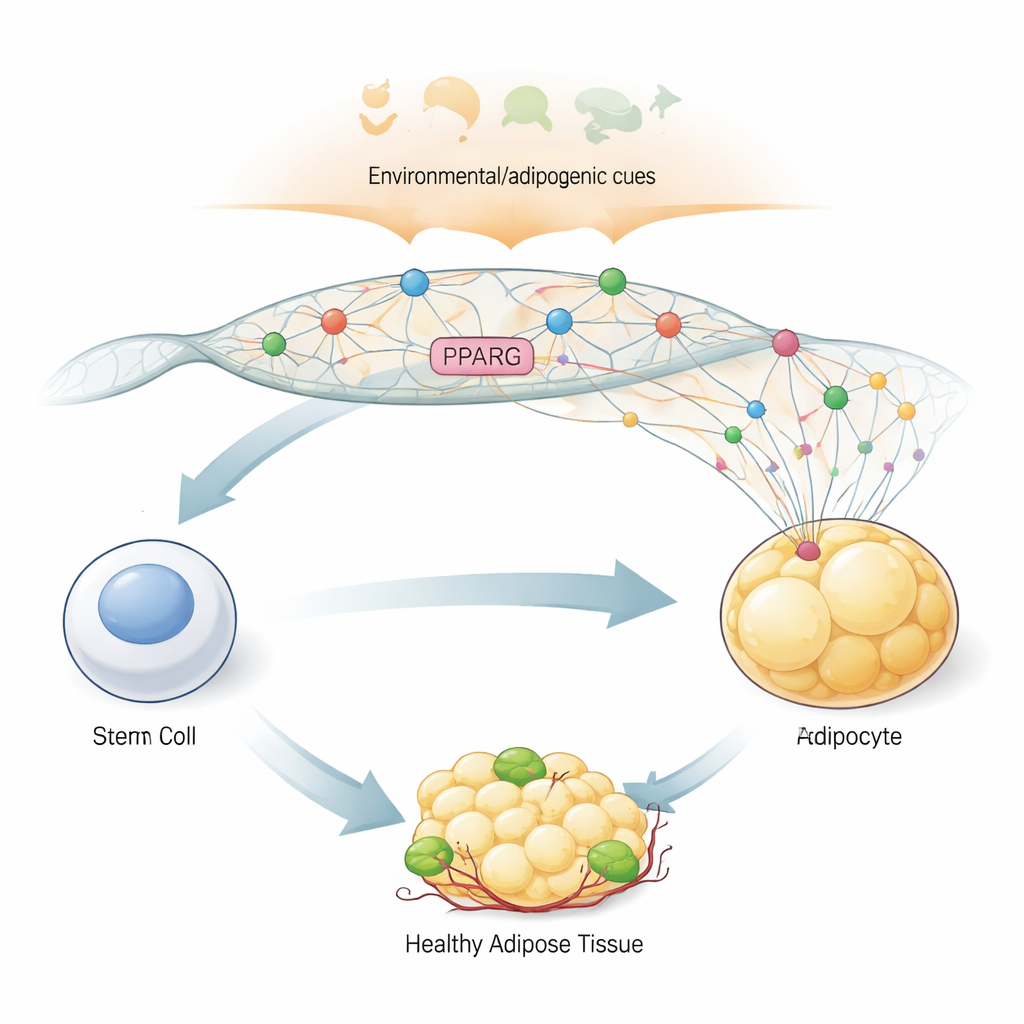
Главный переключатель превращения в жировую клетку
Чтобы превратить универсальную стволоподобную клетку в жировую, организм опирается на «главный переключатель» — ген PPARG2, который кодирует белок PPARγ2. Этот белок контролирует сотни других генов, отвечающих за накопление жира, чувствительность к инсулину и гормональную функцию жировой ткани. Из-за своей центральной роли PPARG2 должен оставаться выключенным в предшественниках, а затем включаться быстро и значительно при поступлении адипогенных сигналов, по сути говорящих: «формируйте жировые клетки сейчас». Авторы использовали модель человеческих стволовых клеток из костного мозга, которые в лаборатории можно направить в адипогенную дифференцировку, что позволило им поэтапно наблюдать, как изменяется конфигурация и активность региона генома вокруг PPARG2 в процессе дифференцировки.
3D-окрестность, заранее подготовленная к изменениям
Ген PPARG2 расположен внутри замкнутого трёхмерного участка ДНК, известного как домен, физически изолированного от соседних генов. Даже до момента, когда клетки принимают решение стать жировыми, этот участок уже «праймирован»: химические метки на ДНК и белках, её окружающих, отмечают набор регуляторных элементов — энхансеров — как будущие узлы регуляции. С помощью методов трёхмерного картирования генома исследователи обнаружили, что эти энхансеры уже взаимодействуют друг с другом на длинных расстояниях, формируя плотно связанное сообщество вокруг PPARG2. При поступлении адипогенных сигналов эти контакты укрепляются, появляются новые признаки активности, а сеть энхансеров ещё более фокусируется на промоторе PPARG2, что совпадает с резким повышением экспрессии PPARG2.
Много помощников, мало запасных
Чтобы проверить вклад каждого энхансера, команда применила редактирование генома на основе CRISPR и удаляла девять отдельных сегментов энхансеров, разбросанных вверхпо течению, рядом с геном и внизпо течению от PPARG2. Вместо простого включателя/выключателя они обнаружили, что по крайней мере шесть из этих энхансеров необходимы для полной активации PPARG2 и нормального формирования жировых клеток. Удаление некоторых промотор-близких энхансеров или участков большого нисходящего «супер-энхансера» значительно ослабляло активность PPARG2 и снижало накопление липидов в получившихся клетках. Один нисходящий энхансер, обозначенный как E+102, оказался особенно критичным: его удаление практически полностью мешало включению PPARG2, хотя остальная часть гена и другие энхансеры оставались нетронутыми.
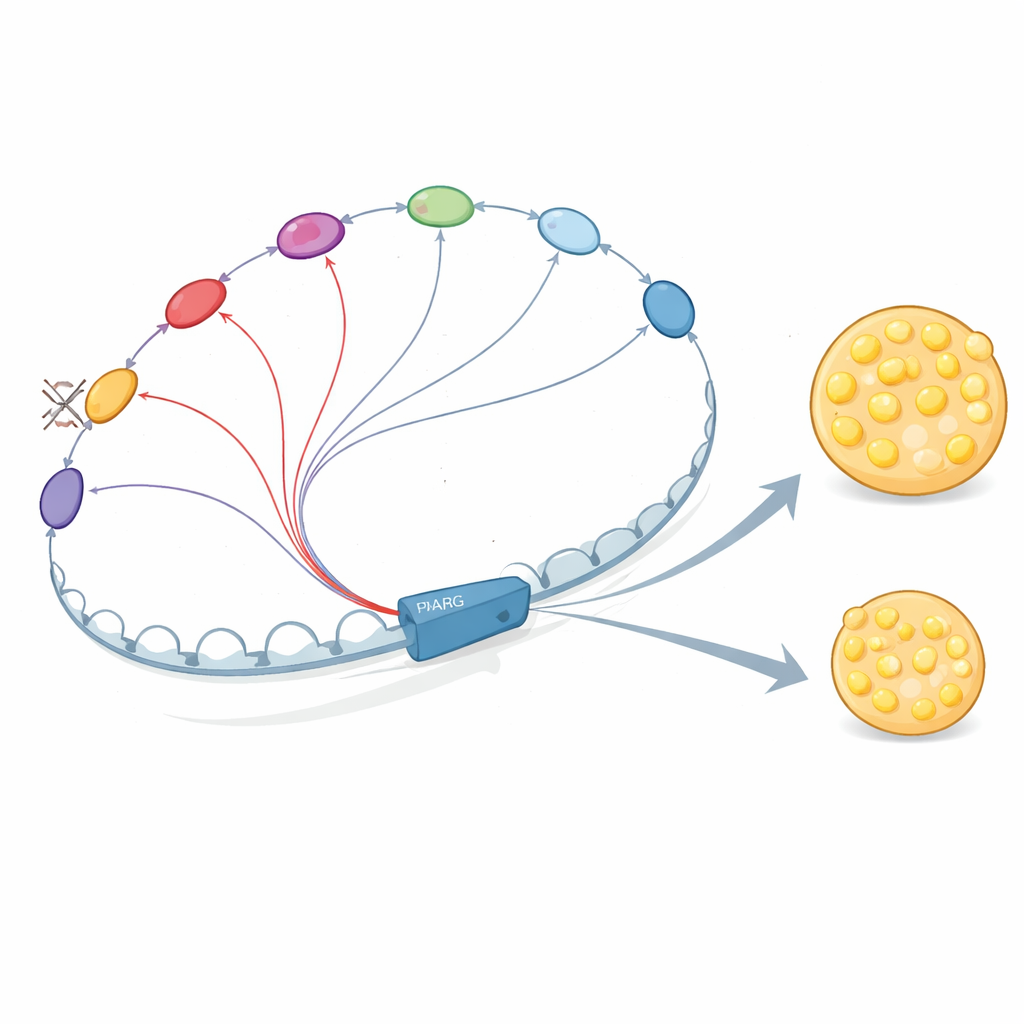
Энхансеры общаются и усиливают друг друга
Почему эти элементы ДНК настолько взаимозависимы? Авторы показывают, что энхансеры в окрестности PPARG2 не действуют изолированно. Они привлекают ключевые регуляторные белки, включая ранние факторы, такие как C/EBPβ, а затем — сам PPARγ и C/EBPα. Эти белки связываются с несколькими энхансерами, которые физически контактируют друг с другом, стабилизируя взаимное связывание и усиливая привлечение комплекса Mediator, помогающего начинать транскрипцию. Когда исследователи удаляли E+102 или важный промотор-близкий энхансер, связывание этих факторов и Mediator снижалось не только на удалённом участке, но и по всему ансамблю энхансеров региона, а трёхмерная сеть контактов ослабевала. Это подтверждает модель, в которой «перекрёстное общение» между энхансерами формирует кооперативный центр, усиливающий сигнал PPARG2.
От вариантов ДНК к риску болезни
Наконец, исследование связывает эту сложную систему контроля с человеческими метаболическими заболеваниями. Большинство вариантов ДНК, ассоциированных с ожирением, уровнем холестерина или сахарным диабетом 2-го типа, располагаются вне кодирующих участков — в некодирующих областях, таких как энхансеры. Объединив большие генетические наборы данных с мощной моделью машинного обучения регуляции генома, авторы обнаружили, что многие высокоранговые варианты риска внутри домена PPARG2 попадают прямо в наиболее критичные энхансеры, которые они картировали, включая E+102 и промотор-близкие сайты. Некоторые из этих вариантов, по прогнозам — и в одном случае экспериментально — изменяют, насколько хорошо PPARγ или другие факторы связываются, тонко меняя активность энхансера и экспрессию PPARG2. Иными словами, небольшие изменения в этой сети энхансеров могут склонить жировые клетки человека к более здоровому или менее здоровому поведению.
Что это значит для метаболического здоровья
Проще говоря, эта работа показывает, что включение ключевого гена жировых клеток PPARG2 — это не работа одного переключателя, а слаженной команды регуляторных элементов ДНК, которые взаимодействуют в трёх измерениях. Один особенно важный энхансер помогает запустить процесс и затем служит главным объектом положительной обратной связи от самого белка PPARγ, обеспечивая быстрое и надёжное закрепление судьбы клетки как жировой. Генетические варианты, ослабляющие части этого сообщества энхансеров, могут снижать активацию PPARG2, нарушать формирование или функцию жировых клеток и тем самым способствовать сердечно-метаболическим заболеваниям. Понимание этой сетевой системы управления открывает путь к более точной оценке риска и, возможно, к целевому корректированию биологии жировых клеток для улучшения метаболического здоровья.
Цитирование: Cetnarowska, A., Hyldahl, M., Nygård, M. et al. Extensive enhancer crosstalk controls PPARG2 activation during adipogenesis. Nat Commun 17, 3824 (2026). https://doi.org/10.1038/s41467-026-70401-7
Ключевые слова: PPARG2, энхансеры, адипогенез, регуляция генов, сердечно-метаболические заболевания