Clear Sky Science · pt
Extenso intercâmbio entre enhancers controla a ativação de PPARG2 durante a adipogênese
Por que os interruptores de células adiposas importam
As células adiposas costumam ser responsabilizadas pela obesidade, mas o tecido adiposo saudável é essencial para armazenar energia com segurança e manter o açúcar no sangue e o colesterol em equilíbrio. Quando as células adiposas não conseguem se formar ou funcionar adequadamente, a gordura vaza para o fígado, músculos e coração, aumentando o risco de diabetes e doenças cardíacas. Este estudo faz uma pergunta básica, porém crucial: como um gene-chave é ativado no momento certo para transformar uma célula imatura em uma célula adiposa plenamente formada? Ao responder a essa questão, o trabalho esclarece por que algumas pessoas são mais vulneráveis a doenças metabólicas — e como pequenas alterações no DNA, longe dos genes, podem ter grandes efeitos na saúde.
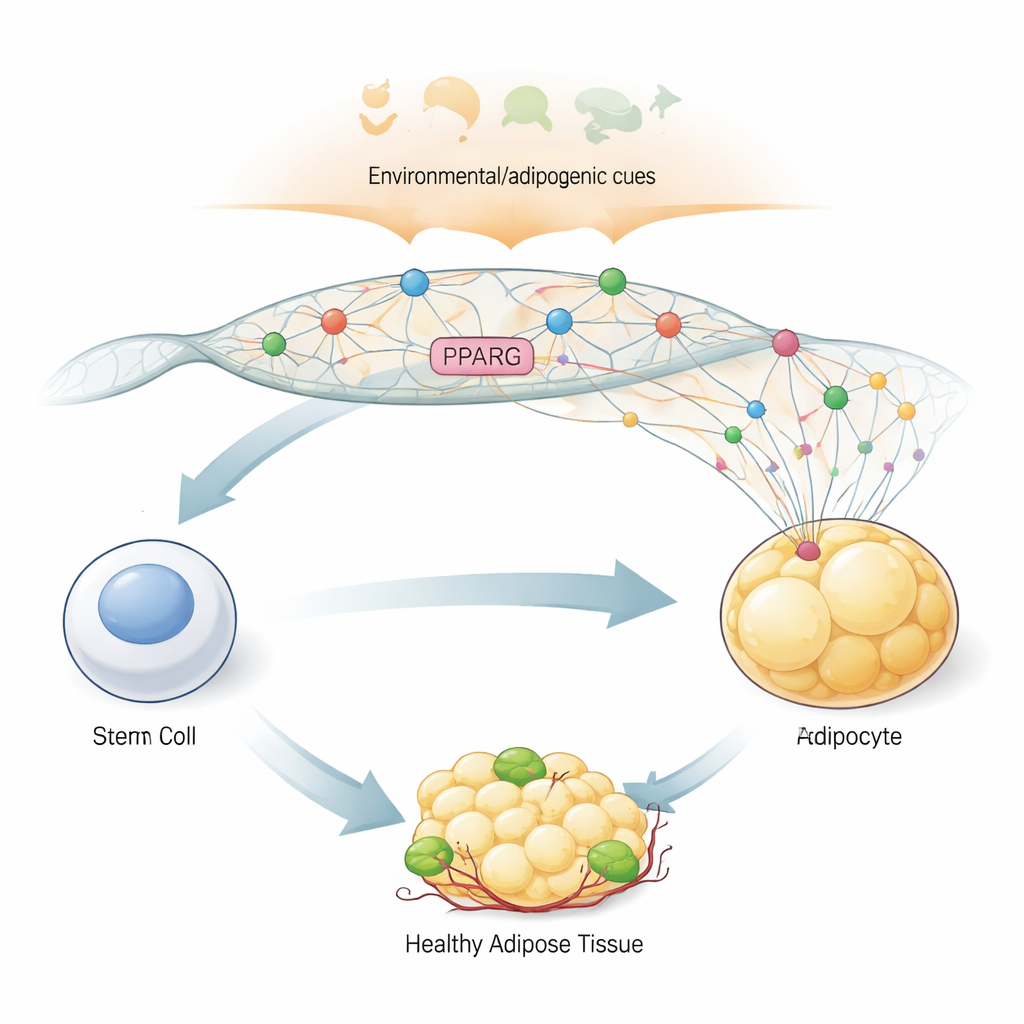
O interruptor mestre para se tornar uma célula adiposa
Para transformar uma célula genérica semelhante a uma célula-tronco em uma célula adiposa, o organismo depende de um gene “interruptor mestre” chamado PPARG2, que produz a proteína PPARγ2. Essa proteína controla centenas de outros genes envolvidos no armazenamento de gordura, sensibilidade à insulina e produção hormonal no tecido adiposo. Por seu papel central, PPARG2 precisa permanecer desligado nas células precursoras e então ligar-se rápida e fortemente quando o organismo envia sinais adipogênicos que, na prática, dizem “façam células adiposas agora”. Os autores usaram um modelo de células-tronco derivadas da medula óssea humana que pode ser direcionado a virar células adiposas em laboratório, permitindo-lhes observar, passo a passo, como a região do genoma ao redor de PPARG2 muda de forma e atividade conforme a diferenciação se desenrola.
Um bairro 3D pré-configurado para a mudança
O gene PPARG2 está situado dentro de um bairro 3D auto-contido de DNA conhecido como domínio, fisicamente isolado dos genes vizinhos. Mesmo antes das células se comprometerem com o destino adiposo, essa região já está “primed”: marcas químicas no DNA e nas proteínas circundantes sinalizam um conjunto de elementos de controle, chamados enhancers, como pontos regulatórios futuros. Usando métodos de mapeamento do genoma em 3D, os pesquisadores descobriram que esses enhancers já se comunicam entre si a longas distâncias, formando uma comunidade fortemente conectada em torno de PPARG2. Quando as células recebem sinais adipogênicos, esses contatos se fortalecem, aparecem novas marcas de atividade e a rede de enhancers se concentra ainda mais no promotor de PPARG2, coincidindo com um forte aumento na expressão de PPARG2.
Muitos ajudantes, poucos sobressalentes
Para testar como cada enhancer contribui, a equipe usou edição genômica baseada em CRISPR para deletar nove segmentos individuais de enhancer espalhados a montante, próximos e a jusante de PPARG2. Em vez de encontrar um único interruptor liga/desliga, eles descobriram que pelo menos seis desses enhancers são essenciais para a ativação completa de PPARG2 e para a formação adequada de células adiposas. Remover certos enhancers próximos ao promotor ou partes de um grande “super-enhancer” a jusante reduziu bastante a atividade de PPARG2 e diminuiu o acúmulo de lipídios nas células resultantes. Um enhancer a jusante, chamado E+102, foi especialmente crítico: sua deleção quase impediu totalmente a ativação de PPARG2, mesmo que o resto do gene e outros enhancers permanecessem intactos.
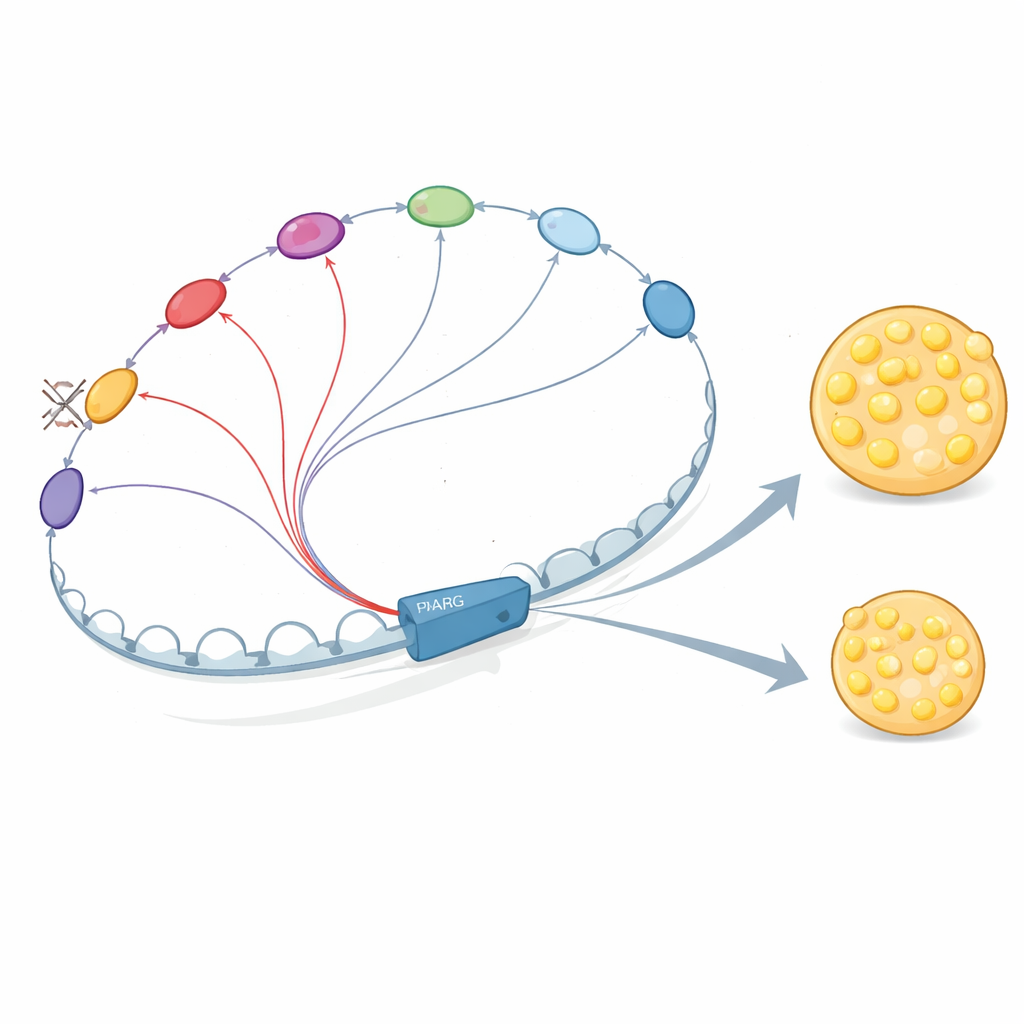
Enhancers conversando e reforçando uns aos outros
Por que esses elementos de DNA são tão interdependentes? Os autores mostram que os enhancers no bairro de PPARG2 não atuam isoladamente. Eles recrutam proteínas regulatórias-chave, incluindo fatores que atuam cedo, como C/EBPβ, e, mais tarde, o próprio PPARγ e C/EBPα. Essas proteínas se ligam em múltiplos enhancers que se contactam fisicamente, estabilizando a ligação umas das outras e aumentando o recrutamento do complexo Mediator, que ajuda a iniciar a transcrição. Quando os pesquisadores removeram E+102 ou um enhancer proximal ao promotor importante, a ligação desses fatores e do Mediator caiu não apenas no sítio deletado, mas também em outros enhancers da região, e a rede de contatos 3D enfraqueceu. Isso apoia a imagem de que o “diálogo” entre enhancers cria um núcleo cooperativo que amplifica o sinal de PPARG2.
De variantes do DNA ao risco de doença
Por fim, o estudo liga esse sistema de controle intrincado à doença metabólica humana. A maioria das variantes de DNA associadas à obesidade, níveis de colesterol ou diabetes tipo 2 está fora dos genes, em regiões não codificantes como enhancers. Ao combinar grandes conjuntos de dados genéticos com um poderoso modelo de aprendizado de máquina da regulação genômica, os autores descobriram que muitas das variantes de risco com maior pontuação dentro do domínio de PPARG2 caem diretamente dentro dos enhancers mais críticos que mapearam, incluindo E+102 e sítios próximos ao promotor. Algumas dessas variantes são previstas — e em um caso demonstrado — para alterar o quanto PPARγ ou outros fatores se ligam, modificando sutilmente a atividade do enhancer e a expressão de PPARG2. Em outras palavras, pequenos ajustes nessa rede de enhancers podem empurrar as células adiposas de uma pessoa para um comportamento mais saudável ou menos saudável.
O que isso significa para a saúde metabólica
Em termos práticos, este trabalho revela que ligar o gene chave das células adiposas, PPARG2, não é tarefa de um único interruptor, mas de uma equipe cuidadosamente coreografada de elementos de controle do DNA que se comunicam em três dimensões. Um enhancer especialmente importante tanto ajuda a iniciar o processo quanto serve como alvo principal para feedback positivo do próprio protein PPARγ, assegurando um compromisso rápido e robusto com o destino adiposo. Variantes genéticas que enfraquecem partes dessa comunidade de enhancers podem reduzir a ativação de PPARG2, prejudicar a formação ou função das células adiposas e, assim, contribuir para doenças cardiometabólicas. Entender esse sistema de controle em rede abre a porta para formas mais precisas de avaliar o risco e, potencialmente, ajustar a biologia das células adiposas para melhorar a saúde metabólica.
Citação: Cetnarowska, A., Hyldahl, M., Nygård, M. et al. Extensive enhancer crosstalk controls PPARG2 activation during adipogenesis. Nat Commun 17, 3824 (2026). https://doi.org/10.1038/s41467-026-70401-7
Palavras-chave: PPARG2, enhancers, adipogênese, regulação gênica, doença cardiometabólica