Clear Sky Science · fr
Un vaste dialogue entre enhancers contrôle l’activation de PPARG2 pendant l’adipogenèse
Pourquoi les interrupteurs des cellules graisseuses comptent
Les cellules graisseuses sont souvent pointées du doigt dans l’obésité, mais un tissu adipeux sain est essentiel pour stocker l’énergie en toute sécurité et maintenir l’équilibre de la glycémie et du cholestérol. Quand les adipocytes ne se forment pas ou ne fonctionnent pas correctement, les lipides s’accumulent dans le foie, les muscles et le cœur, augmentant le risque de diabète et de maladies cardiovasculaires. Cette étude pose une question simple mais cruciale : comment un gène clé s’active-t-il au bon moment pour transformer une cellule immature en adipocyte pleinement différencié ? En répondant à cette question, le travail éclaire pourquoi certaines personnes sont plus vulnérables aux troubles métaboliques — et comment de petites variations d’ADN, situées loin des gènes, peuvent avoir de grands effets sur la santé.
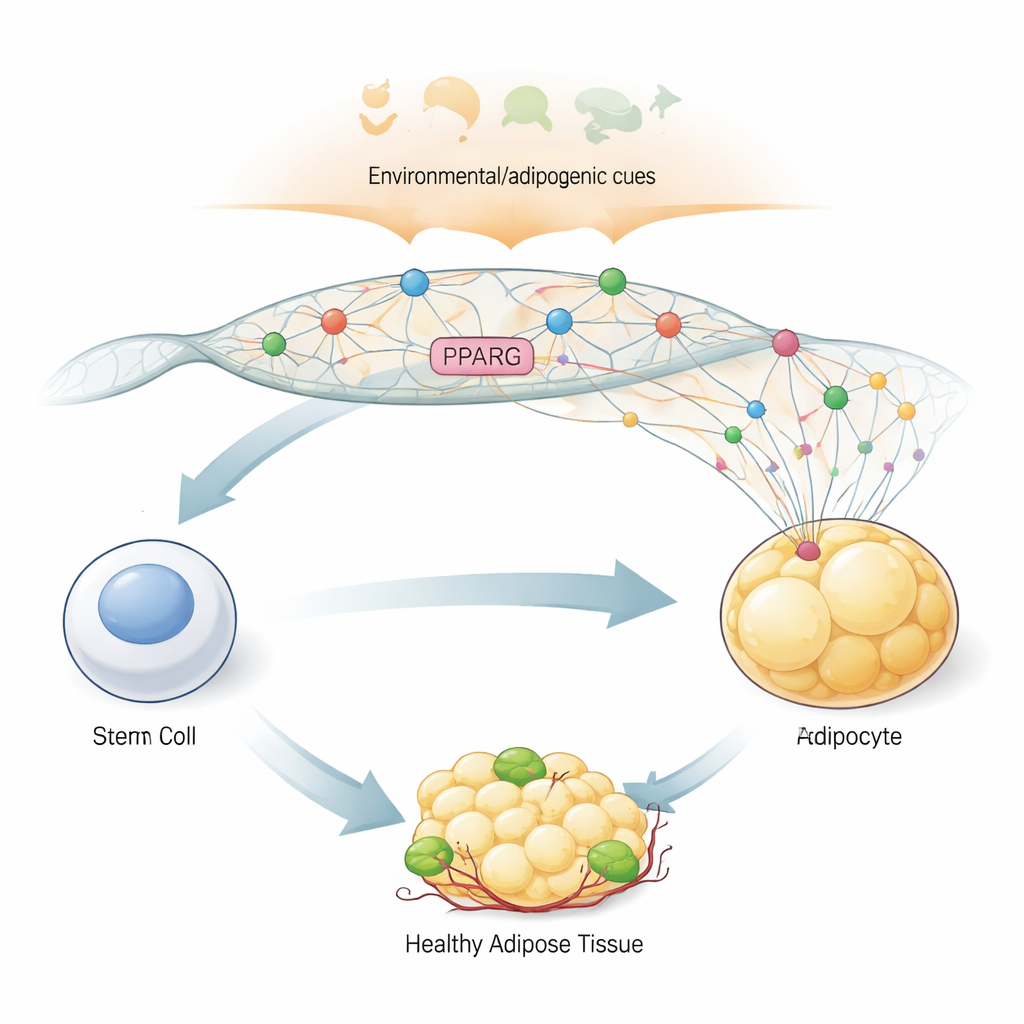
Le commutateur maître de la différenciation adipocytaire
Pour transformer une cellule souches généraliste en adipocyte, l’organisme s’appuie sur un gène « commutateur maître » nommé PPARG2, qui code pour la protéine PPARγ2. Cette protéine régule des centaines d’autres gènes impliqués dans le stockage des lipides, la sensibilité à l’insuline et la production hormonale dans le tissu adipeux. En raison de son rôle central, PPARG2 doit rester éteint dans les cellules précurseures puis s’allumer rapidement et fortement quand l’organisme envoie des signaux adipogéniques signifiant, en substance, « fabriquer des cellules graisseuses maintenant ». Les auteurs ont utilisé un modèle de cellules souches dérivées de la moelle osseuse humaine pouvant être dirigées vers la filière adipeuse en laboratoire, ce qui leur a permis d’observer, étape par étape, comment la région génomique de PPARG2 change de forme et d’activité au cours de la différenciation.
Un voisinage 3D préconfiguré pour le changement
Le gène PPARG2 se situe à l’intérieur d’un voisinage 3D autonome d’ADN connu comme un domaine, physiquement isolé des gènes voisins. Avant même que les cellules ne s’engagent dans la filière adipeuse, cette région est déjà « amorcée » : des marques chimiques sur l’ADN et les protéines avoisinantes signalent un ensemble d’éléments de contrôle, appelés enhancers, comme de futurs points chauds régulateurs. Grâce à des méthodes de cartographie 3D du génome, les chercheurs ont constaté que ces enhancers communiquent déjà entre eux sur de longues distances, formant une communauté fortement connectée autour de PPARG2. Lorsque les cellules reçoivent des signaux adipogéniques, ces contacts se renforcent, de nouvelles marques d’activité apparaissent, et le réseau d’enhancers concentre encore davantage son action sur le promoteur de PPARG2, en corrélation avec une hausse nette de l’expression de PPARG2.
Beaucoup d’aides, peu de remplaçants
Pour tester la contribution de chaque enhancer, l’équipe a utilisé l’édition du génome basée sur CRISPR pour supprimer neuf segments d’enhancer individuels répartis en amont, à proximité et en aval de PPARG2. Plutôt que de découvrir un simple interrupteur marche/arrêt, ils ont montré qu’au moins six de ces enhancers sont essentiels pour une activation complète de PPARG2 et une formation correcte des adipocytes. La suppression de certains enhancers proches du promoteur ou de portions d’un grand « super‑enhancer » en aval a fortement atténué l’activité de PPARG2 et réduit l’accumulation de lipides dans les cellules obtenues. Un enhancer en aval, nommé E+102, s’est avéré particulièrement critique : sa suppression a presque empêché PPARG2 de s’activer, malgré l’intégrité du reste du gène et des autres enhancers.
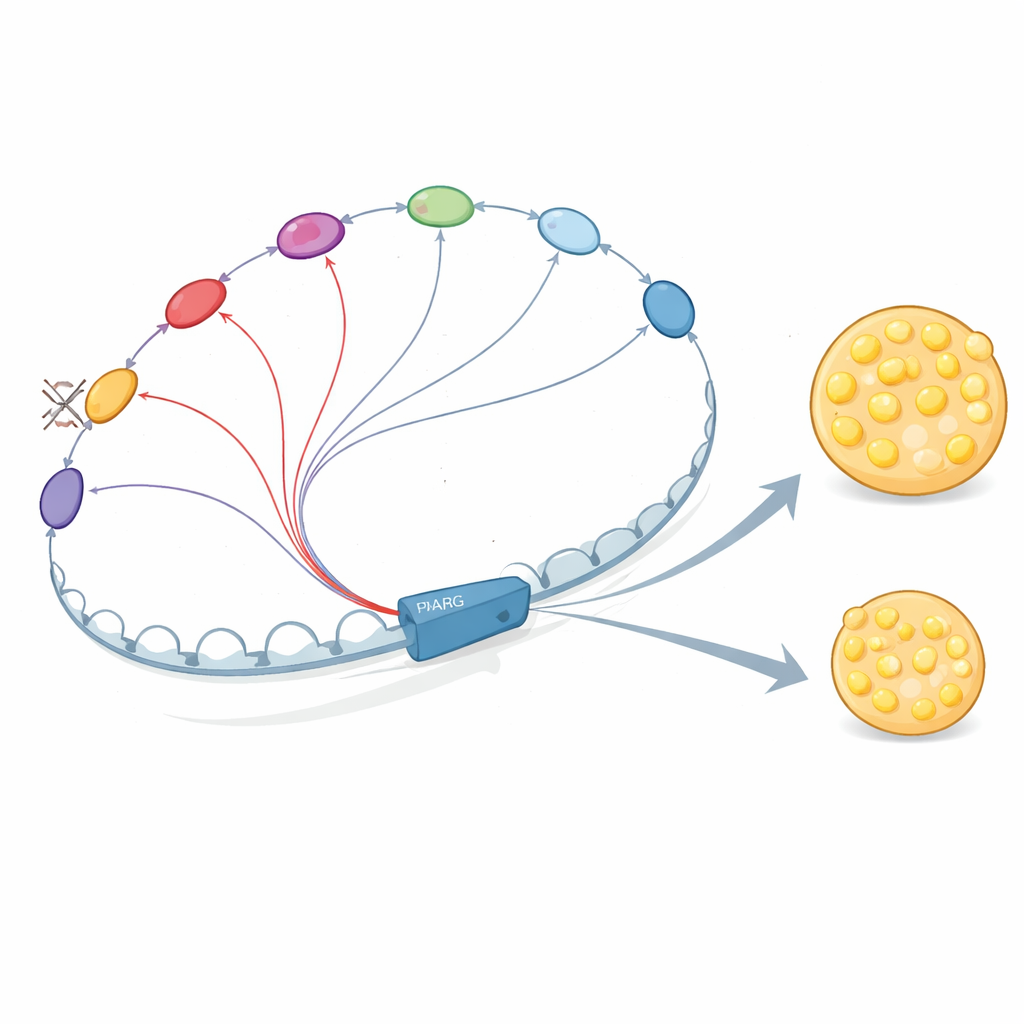
Des enhancers qui se parlent et se renforcent mutuellement
Pourquoi ces éléments d’ADN sont‑ils si interdépendants ? Les auteurs montrent que les enhancers du voisinage de PPARG2 n’agissent pas isolément. Ils recrutent des protéines régulatrices clés, incluant des facteurs d’action précoce comme C/EBPβ, puis plus tard PPARγ lui‑même et C/EBPα. Ces protéines se lient à plusieurs enhancers qui sont en contact physique les uns avec les autres, stabilisant la liaison réciproque et favorisant le recrutement du complexe Mediator, qui aide au démarrage de la transcription. Lorsque les chercheurs ont supprimé E+102 ou un enhancer crucial proche du promoteur, la liaison de ces facteurs et du Mediator a diminué non seulement au site supprimé mais aussi sur d’autres enhancers de la région, et le réseau de contacts 3D s’est affaibli. Cela soutient l’idée selon laquelle le « dialogue » enhancer–enhancer crée un noyau coopératif qui amplifie le signal PPARG2.
Des variantes d’ADN au risque de maladie
Enfin, l’étude relie ce système de contrôle complexe aux maladies métaboliques humaines. La plupart des variantes d’ADN associées à l’obésité, aux taux de cholestérol ou au diabète de type 2 se trouvent en dehors des gènes, dans des régions non codantes comme les enhancers. En combinant de grands jeux de données génétiques avec un modèle d’apprentissage automatique puissant de la régulation du génome, les auteurs ont trouvé que de nombreuses variantes de risque mieux classées à l’intérieur du domaine de PPARG2 se situent directement dans les enhancers les plus critiques qu’ils ont cartographiés, y compris E+102 et des sites proches du promoteur. Certaines de ces variantes sont prédites — et dans un cas démontré — comme modifiant l’affinité de liaison de PPARγ ou d’autres facteurs, modifiant subtilement l’activité des enhancers et l’expression de PPARG2. Autrement dit, de petites modifications de ce réseau d’enhancers peuvent orienter les adipocytes d’une personne vers un comportement plus ou moins sain.
Ce que cela signifie pour la santé métabolique
Concrètement, ce travail montre que l’activation du gène clé des adipocytes PPARG2 n’est pas l’affaire d’un seul interrupteur mais d’une équipe coordonnée d’éléments de contrôle de l’ADN qui communiquent en trois dimensions. Un enhancer particulièrement important aide à initier le processus puis sert de cible principale pour un feedback positif provenant de la protéine PPARγ elle‑même, garantissant un engagement rapide et robuste vers la destinée adipocytaire. Des variantes génétiques qui affaiblissent des parties de cette communauté d’enhancers peuvent réduire l’activation de PPARG2, compromettre la formation ou la fonction des adipocytes, et contribuer ainsi aux maladies cardiométaboliques. Comprendre ce système de contrôle en réseau ouvre la voie à des méthodes plus précises d’évaluation du risque et, potentiellement, à des interventions visant à moduler la biologie des adipocytes pour améliorer la santé métabolique.
Citation: Cetnarowska, A., Hyldahl, M., Nygård, M. et al. Extensive enhancer crosstalk controls PPARG2 activation during adipogenesis. Nat Commun 17, 3824 (2026). https://doi.org/10.1038/s41467-026-70401-7
Mots-clés: PPARG2, enhancers, adipogenèse, régulation des gènes, maladie cardiométabolique