Clear Sky Science · it
Esteso dialogo tra enhancer controlla l’attivazione di PPARG2 durante l’adipogenesi
Perché i interruttori delle cellule adipose sono importanti
Le cellule adipose vengono spesso additate per l’obesità, ma il tessuto adiposo sano è fondamentale per immagazzinare energia in modo sicuro e mantenere sotto controllo glicemia e colesterolo. Quando le cellule adipose non si formano o non funzionano correttamente, il grasso si accumula nel fegato, nei muscoli e nel cuore, aumentando il rischio di diabete e malattie cardiovascolari. Questo studio pone una domanda semplice ma cruciale: come viene attivato un gene chiave nel momento giusto per trasformare una cellula immatura in una cellula adiposa matura? Scoprire la risposta chiarisce perché alcune persone sono più vulnerabili alle malattie metaboliche — e come piccole variazioni del DNA, anche lontano dai geni, possono avere grandi effetti sulla salute.
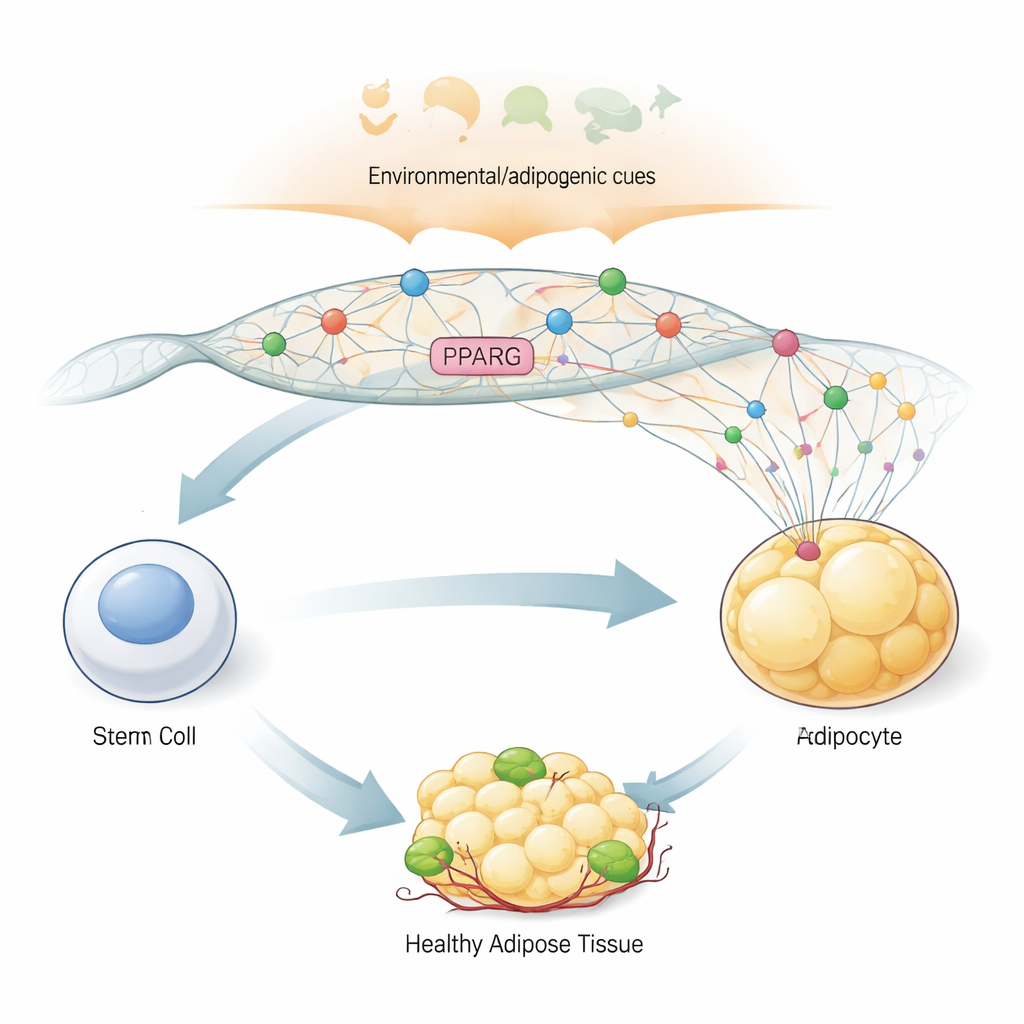
Il comando principale per diventare una cellula adiposa
Per trasformare una cellula generica simile a uno staminale in una cellula adiposa, l’organismo si affida a un gene “interruttore principale” chiamato PPARG2, che codifica la proteina PPARγ2. Questa proteina controlla centinaia di altri geni responsabili dell’immagazzinamento dei grassi, della sensibilità all’insulina e della produzione ormonale nel tessuto adiposo. Per il suo ruolo centrale, PPARG2 deve restare spento nei precursori e poi accendersi rapidamente e intensamente quando l’organismo invia segnali adipogenici che dicono, in pratica, “ora fai cellule adipose”. Gli autori hanno usato un modello di cellule staminali umane derivate dal midollo osseo che può essere indirizzato verso la linea adiposa in laboratorio, permettendo di osservare, passo dopo passo, come la regione genomica di PPARG2 cambia forma e attività durante la differenziazione.
Un quartiere 3D predisposto al cambiamento
Il gene PPARG2 si trova all’interno di un quartiere 3D autosufficiente del DNA noto come dominio, fisicamente isolato dai geni circostanti. Anche prima che le cellule si impegnino a diventare adipose, questa regione è già “primed”: modificazioni chimiche sul DNA e sulle proteine circostanti segnalano un insieme di elementi di controllo, detti enhancer, come futuri punti caldi regolatori. Utilizzando metodi di mappatura del genoma in 3D, i ricercatori hanno scoperto che questi enhancer comunicano già tra loro a lunga distanza, formando una comunità strettamente connessa attorno a PPARG2. Quando le cellule ricevono i segnali adipogenici, questi contatti si rafforzano, compaiono nuovi segni di attività e la rete di enhancer si concentra ancora di più sul promotore di PPARG2, in coincidenza con un netto aumento dell’espressione di PPARG2.
Molti aiutanti, poche riserve
Per valutare il contributo di ciascun enhancer, il gruppo ha utilizzato l’editing genomico basato su CRISPR per eliminare nove segmenti enhancer individuali dispersi a monte, vicino e a valle di PPARG2. Invece di trovare un singolo interruttore on/off, hanno scoperto che almeno sei di questi enhancer sono essenziali per la piena attivazione di PPARG2 e per la corretta formazione delle cellule adipose. Rimuovere alcuni enhancer prossimali al promotore o porzioni di un grande “super-enhancer” a valle riduceva fortemente l’attività di PPARG2 e l’accumulo lipidico nelle cellule risultanti. Un enhancer a valle, chiamato E+102, era particolarmente critico: la sua eliminazione impediva quasi completamente l’accensione di PPARG2, nonostante il resto del gene e degli altri enhancer rimanessero intatti.
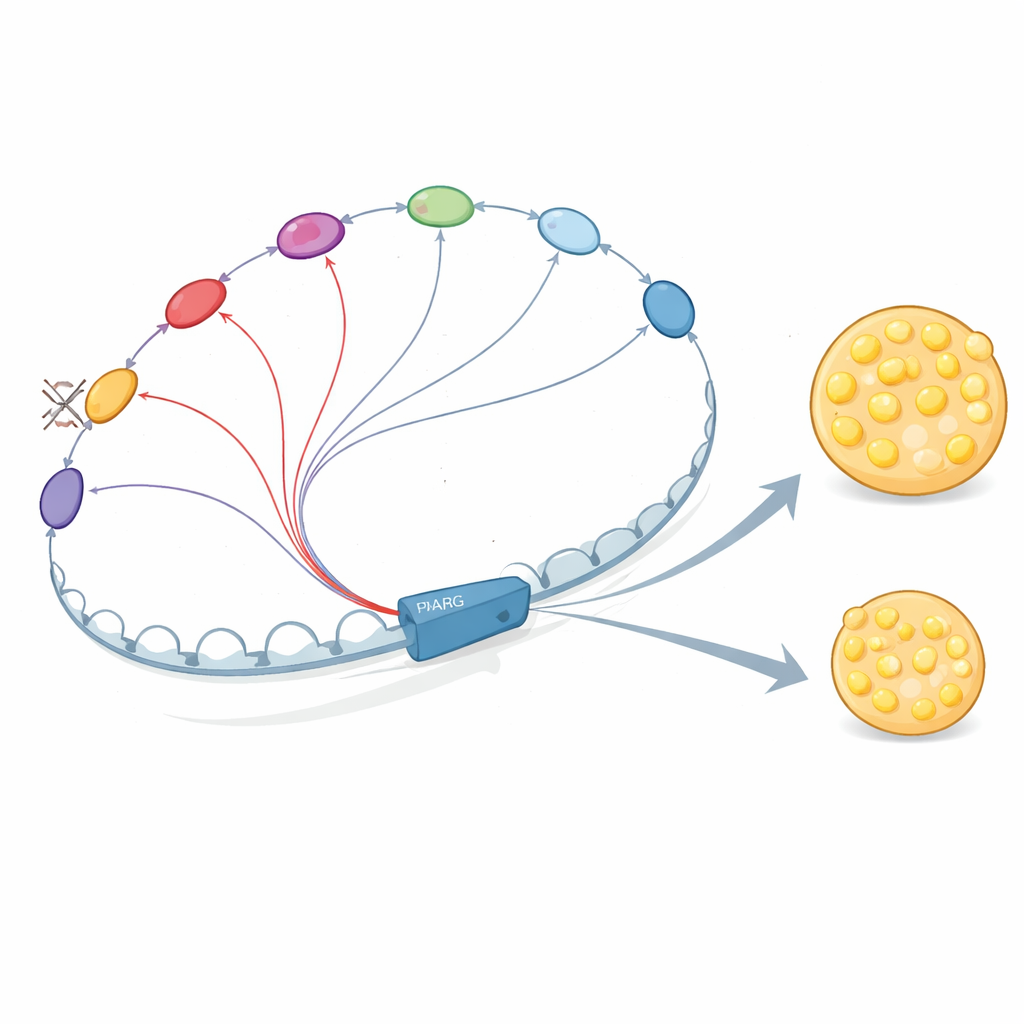
Enhancer che si parlano e si rafforzano a vicenda
Perché questi elementi del DNA sono così interdipendenti? Gli autori mostrano che gli enhancer nel quartiere di PPARG2 non agiscono isolatamente. Reclutano proteine regolatrici chiave, inclusi fattori che agiscono precocemente come C/EBPβ e, in seguito, lo stesso PPARγ e C/EBPα. Queste proteine si legano a più enhancer che entrano in contatto fisico tra loro, stabilizzando il legame reciproco e potenziando il reclutamento del complesso Mediator, che aiuta a iniziare la trascrizione. Quando i ricercatori hanno rimosso E+102 o un enhancer prossimale al promotore cruciale, il legame di questi fattori e del Mediator è diminuito non solo nel sito cancellato ma anche negli altri enhancer della regione, e la rete di contatti 3D si è indebolita. Ciò supporta l’idea che il “crosstalk” enhancer–enhancer crei un hub cooperativo che amplifica il segnale di PPARG2.
Dalle varianti del DNA al rischio di malattia
Infine, lo studio collega questo complesso sistema di controllo alle malattie metaboliche umane. La maggior parte delle varianti del DNA associate a obesità, livelli di colesterolo o diabete di tipo 2 si trova al di fuori dei geni, in regioni non codificanti come gli enhancer. Combinando ampi dataset genetici con un potente modello di machine learning della regolazione genomica, gli autori hanno scoperto che molte delle varianti di rischio meglio classificate all’interno del dominio di PPARG2 ricadono direttamente nei enhancer più critici che avevano mappato, inclusi E+102 e siti prossimali al promotore. Alcune di queste varianti sono previste — e in un caso dimostrate — alterare quanto efficacemente PPARγ o altri fattori si legano, modificando sottilmente l’attività degli enhancer e l’espressione di PPARG2. In altre parole, piccole modifiche a questa rete di enhancer possono spingere le cellule adipose di una persona verso comportamenti più o meno salutari.
Cosa significa per la salute metabolica
In termini pratici, questo lavoro rivela che attivare il gene chiave delle cellule adipose PPARG2 non è compito di un singolo interruttore, ma di una squadra strettamente coreografata di elementi di controllo del DNA che comunicano in tre dimensioni. Un enhancer particolarmente importante aiuta sia ad avviare il processo sia a fungere da bersaglio principale per il feedback positivo proveniente dalla proteina PPARγ stessa, garantendo un impegno rapido e robusto verso il destino di cellula adiposa. Le varianti genetiche che indeboliscono parti di questa comunità di enhancer possono ridurre l’attivazione di PPARG2, compromettere la formazione o la funzione delle cellule adipose e contribuire così alle malattie cardiometaboliche. Comprendere questo sistema di controllo a rete apre la strada a modi più precisi per valutare il rischio e, potenzialmente, modulare la biologia delle cellule adipose per migliorare la salute metabolica.
Citazione: Cetnarowska, A., Hyldahl, M., Nygård, M. et al. Extensive enhancer crosstalk controls PPARG2 activation during adipogenesis. Nat Commun 17, 3824 (2026). https://doi.org/10.1038/s41467-026-70401-7
Parole chiave: PPARG2, enhancer, adipogenesi, regolazione genica, malattie cardiometaboliche