Clear Sky Science · pl
Rozległa komunikacja między enhancerami kontroluje aktywację PPARG2 podczas adipogenezy
Dlaczego przełączniki w komórkach tłuszczowych są ważne
Komórki tłuszczowe bywają obwiniane za otyłość, ale zdrowa tkanka tłuszczowa jest niezbędna do bezpiecznego magazynowania energii oraz utrzymywania równowagi poziomu glukozy i cholesterolu we krwi. Gdy komórki tłuszczowe nie mogą się prawidłowo formować lub działać, tłuszcz przedostaje się do wątroby, mięśni i serca, zwiększając ryzyko cukrzycy i chorób serca. W tym badaniu zadano podstawowe, lecz kluczowe pytanie: jak jeden ważny gen zostaje włączony we właściwym momencie, aby przekształcić niedojrzałą komórkę w w pełni ukształtowaną komórkę tłuszczową? Odkrycie tej odpowiedzi wyjaśnia, dlaczego niektórzy ludzie są bardziej podatni na choroby metaboliczne — i jak drobne zmiany w DNA, położone daleko od genów, mogą mieć duży wpływ na zdrowie.
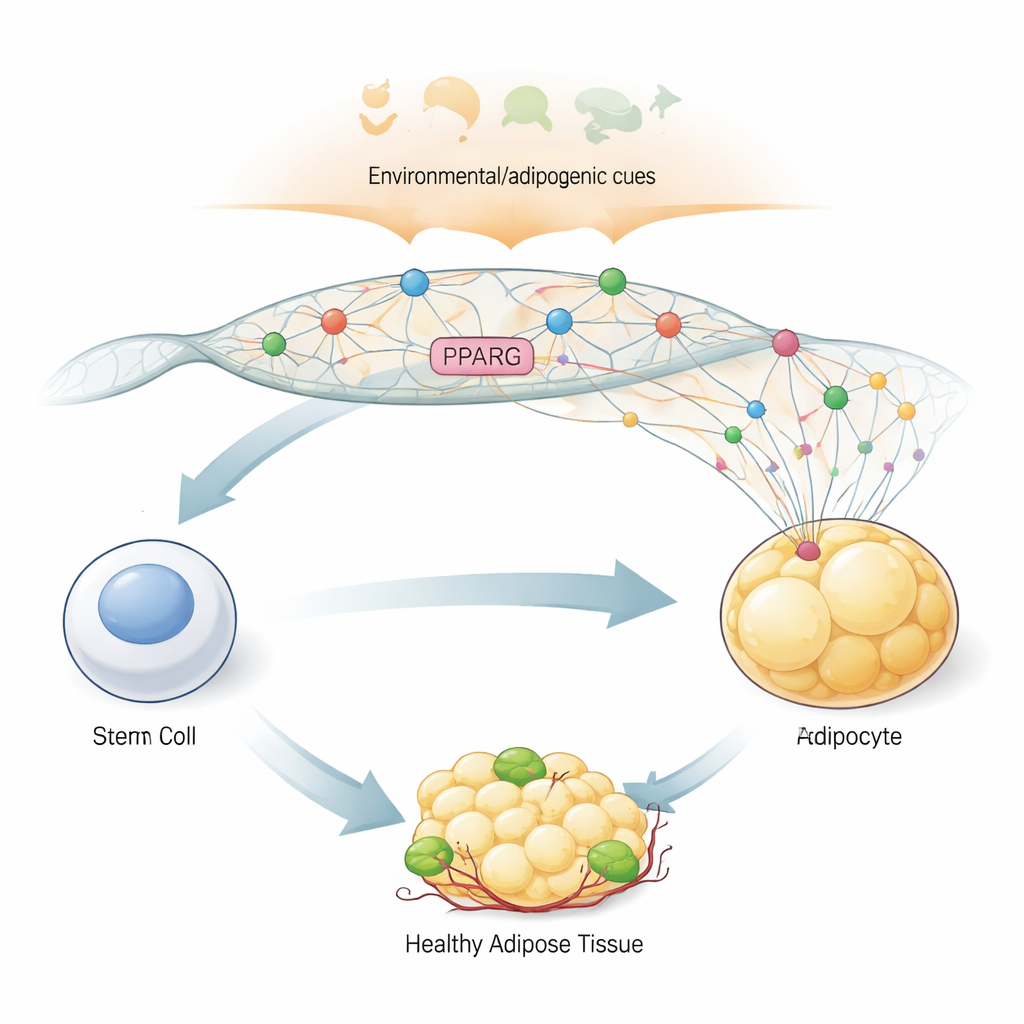
Główny przełącznik pozwalający zostać komórką tłuszczową
Aby przekształcić ogólną komórkę o cechach macierzystych w komórkę tłuszczową, organizm polega na „głównym przełączniku” — genie PPARG2, który koduje białko PPARγ2. To białko kontroluje setki innych genów odpowiedzialnych za magazynowanie tłuszczu, wrażliwość na insulinę i produkcję hormonów w tkance tłuszczowej. Ze względu na centralną rolę, PPARG2 musi pozostawać wyłączony w komórkach prekursorowych, a następnie szybko i silnie włączać się, gdy organizm wysyła sygnały adipogeniczne, które w istocie mówią: „twórz komórki tłuszczowe teraz”. Autorzy użyli modelu ludzkich komórek macierzystych pochodzących ze szpiku kostnego, które można w laboratorium nakierować na linię adipogenną, co pozwoliło im obserwować krok po kroku, jak region genomu zawierający PPARG2 zmienia kształt i aktywność w trakcie różnicowania.
Trójwymiarowe sąsiedztwo zaprogramowane na zmianę
Gen PPARG2 znajduje się w odizolowanym trójwymiarowym sąsiedztwie DNA, zwanym domeną, fizycznie oddzielonym od otaczających genów. Nawet zanim komórki zobowiążą się do bycia komórkami tłuszczowymi, ten region jest już „zaprzyjaźniony”: chemiczne oznaczenia na DNA i białkach otaczających wskazują zestaw elementów kontrolnych, zwanych enhancerami, jako przyszłe regulatoryczne punkty zapalne. Korzystając z metod mapowania 3D genomu, badacze wykryli, że te enhancery już komunikują się ze sobą na duże odległości, tworząc ciasno połączoną społeczność wokół PPARG2. Gdy komórki otrzymują sygnały adipogenne, te kontakty się wzmacniają, pojawiają się nowe znaki aktywności, a sieć enhancerów jeszcze mocniej koncentruje się na promotorze PPARG2, co zbiega się z gwałtownym wzrostem ekspresji PPARG2.
Wielu pomocników, mało zapasowych
Aby sprawdzić, jak każdy enhancer przyczynia się do regulacji, zespół użył edycji genomu opartej na CRISPR do usunięcia dziewięciu pojedynczych fragmentów enhancerów rozmieszczonych powyżej, blisko i poniżej PPARG2. Zamiast jednego przełącznika on/off odkryli, że co najmniej sześć z tych enhancerów jest niezbędnych do pełnej aktywacji PPARG2 i prawidłowego tworzenia komórek tłuszczowych. Usunięcie niektórych enhancerów bliskich promotorowi lub fragmentów dużego „super-enhancera” położonego poniżej znacząco stłumiło aktywność PPARG2 i zmniejszyło akumulację lipidów w powstałych komórkach. Jeden enhancer położony poniżej, nazwany E+102, okazał się szczególnie krytyczny: jego usunięcie niemal całkowicie uniemożliwiło włączenie PPARG2, mimo że reszta genu i pozostałe enhancery pozostały nienaruszone.
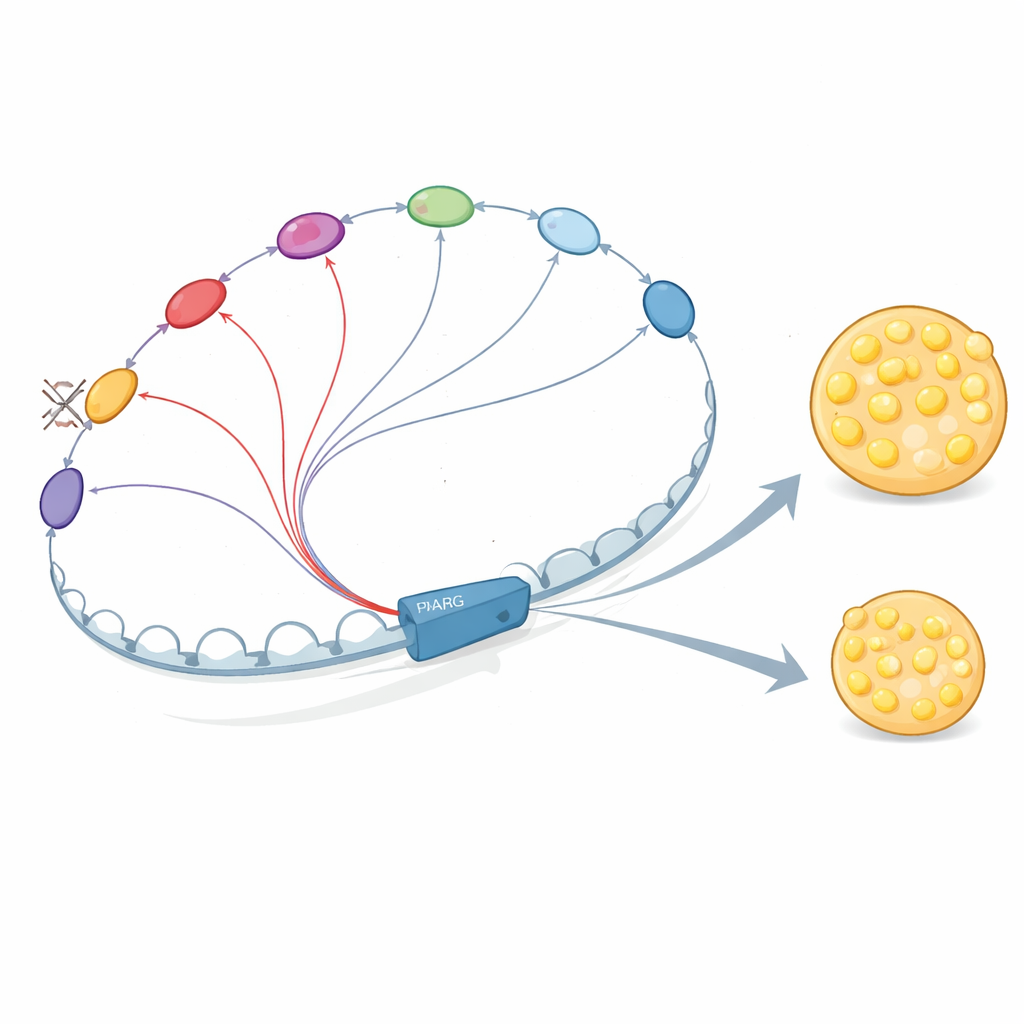
Enhancery rozmawiają ze sobą i wzmacniają nawzajem działanie
Dlaczego te elementy DNA są tak współzależne? Autorzy pokazują, że enhancery w sąsiedztwie PPARG2 nie działają w izolacji. Rekrutują kluczowe białka regulatorowe, w tym czynniki działające wcześnie, takie jak C/EBPβ, a później samego PPARγ i C/EBPα. Te białka wiążą się w wielu enhancerach, które fizycznie się kontaktują, stabilizując swoje wiązanie i zwiększając rekrutację kompleksu Mediator, który pomaga zainicjować transkrypcję. Gdy badacze usunęli E+102 lub istotny enhancer bliski promotorowi, wiązanie tych czynników i Mediatora spadło nie tylko w miejscu delecji, ale w całym regionie enhancerów, a trójwymiarowa sieć kontaktów osłabła. To wspiera obraz, w którym „rozmowy” między enhancerami tworzą kooperatywny hub wzmacniający sygnał PPARG2.
Od wariantów DNA do ryzyka chorób
Wreszcie badanie łączy ten złożony system kontroli z ludzkimi chorobami metabolicznymi. Większość wariantów DNA związanych z otyłością, poziomem cholesterolu czy cukrzycą typu 2 leży poza sekwencjami kodującymi, w obszarach niekodujących, takich jak enhancery. Łącząc duże zbiory danych genetycznych z zaawansowanym modelem uczenia maszynowego regulacji genomu, autorzy odkryli, że wiele najwyżej ocenianych wariantów ryzyka w domenie PPARG2 znajduje się bezpośrednio wewnątrz najważniejszych zmapowanych enhancerów, w tym E+102 i miejsc bliskich promotorowi. Niektóre z tych wariantów są przewidywane — i w jednym przypadku wykazano to empirycznie — że zmieniają, jak dobrze PPARγ lub inne czynniki się wiążą, subtelnie modyfikując aktywność enhancerów i ekspresję PPARG2. Innymi słowy, drobne poprawki w tej sieci enhancerów mogą przesunąć funkcjonowanie komórek tłuszczowych danej osoby w stronę zdrowszego lub mniej korzystnego fenotypu.
Co to znaczy dla zdrowia metabolicznego
Mówiąc prosto, praca ta pokazuje, że włączenie kluczowego genu komórek tłuszczowych PPARG2 nie jest zadaniem pojedynczego przełącznika, lecz starannie zaaranżowanego zespołu elementów kontrolnych DNA, które komunikują się w trzech wymiarach. Jeden szczególnie ważny enhancer pomaga zainicjować proces, a następnie pełni rolę głównego celu dodatniego sprzężenia zwrotnego od samego białka PPARγ, zapewniając szybkie i solidne zobowiązanie do losu komórki tłuszczowej. Warianty genetyczne osłabiające części tej społeczności enhancerów mogą obniżać aktywację PPARG2, upośledzać powstawanie lub funkcję komórek tłuszczowych i w ten sposób przyczyniać się do chorób kardiometabolicznych. Zrozumienie tego sieciowego systemu kontroli otwiera drogę do precyzyjniejszej oceny ryzyka i — potencjalnie — do modulowania biologii komórek tłuszczowych w celu poprawy zdrowia metabolicznego.
Cytowanie: Cetnarowska, A., Hyldahl, M., Nygård, M. et al. Extensive enhancer crosstalk controls PPARG2 activation during adipogenesis. Nat Commun 17, 3824 (2026). https://doi.org/10.1038/s41467-026-70401-7
Słowa kluczowe: PPARG2, enhancery, adipogeneza, regulacja genów, choroby kardiometaboliczne