Clear Sky Science · de
Umfangreiche Enhancer-Kommunikation steuert die Aktivierung von PPARG2 während der Adipogenese
Warum Schalter in Fettzellen wichtig sind
Fettzellen werden oft für Fettleibigkeit verantwortlich gemacht, doch gesundes Fettgewebe ist essenziell, um Energie sicher zu speichern und Blutzucker sowie Cholesterin im Gleichgewicht zu halten. Wenn Fettzellen nicht richtig entstehen oder funktionieren, verteilt sich Fett in Leber, Muskeln und Herz, was das Risiko für Diabetes und Herzkrankheiten erhöht. Diese Studie stellt eine grundlegende, aber entscheidende Frage: Wie wird ein Schlüsselgen genau zum richtigen Zeitpunkt eingeschaltet, um eine unreife Zelle in eine ausdifferenzierte Fettzelle zu verwandeln? Die Antwort darauf erklärt, warum manche Menschen anfälliger für Stoffwechselerkrankungen sind — und wie winzige DNA-Veränderungen weit entfernt von Genen große Auswirkungen auf die Gesundheit haben können.
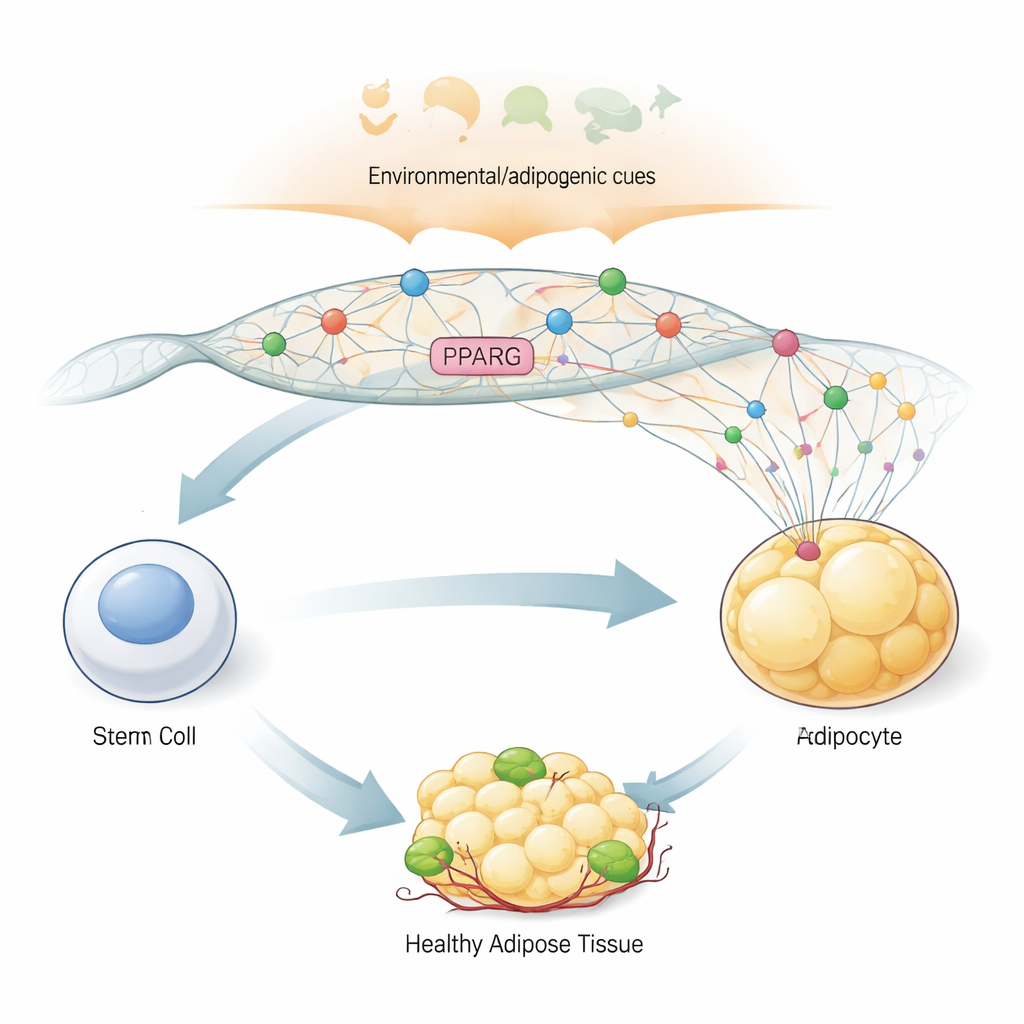
Der Hauptschalter für die Fettzellbildung
Um eine allgemein stemmungsähnliche Zelle in eine Fettzelle zu verwandeln, verlässt sich der Körper auf ein „Master“-Gen namens PPARG2, das das Protein PPARγ2 produziert. Dieses Protein steuert Hunderte anderer Gene, die für Fettspeicherung, Insulinsensitivität und Hormonproduktion im Fettgewebe verantwortlich sind. Wegen seiner zentralen Rolle muss PPARG2 in Vorläuferzellen ausgeschaltet bleiben und dann schnell und stark aktiviert werden, wenn adipogene Signale ausgesandt werden, die sozusagen „jetzt Fettzellen bilden“ bedeuten. Die Autoren verwendeten ein aus menschlichem Knochenmark stammendes Stammzellmodell, das im Labor in Fettzellen gelenkt werden kann, und konnten so Schritt für Schritt beobachten, wie sich die PPARG2-Region des Genoms während der Differenzierung in Form und Aktivität verändert.
Eine dreidimensionale Nachbarschaft, die Veränderung vorprogrammiert
Das PPARG2-Gen liegt in einer abgeschlossenen 3D-DNA-Nachbarschaft, einer sogenannten Domäne, physikalisch von benachbarten Genen isoliert. Schon bevor die Zellen sich zur Fettzelllinie verpflichten, ist diese Region „vorbereitet“: Chemische Markierungen an der DNA und den umgebenden Proteinen markieren eine Reihe von Kontrollelementen, sogenannte Enhancer, als zukünftige regulatorische Hotspots. Mithilfe von 3D-Genomkartierungsmethoden fanden die Forscher heraus, dass diese Enhancer bereits über weite Distanzen miteinander kommunizieren und eine eng vernetzte Gemeinschaft um PPARG2 bilden. Wenn die Zellen adipogene Signale erhalten, verstärken sich diese Kontakte, es erscheinen neue Aktivitätsmarken und das Enhancer-Netzwerk fokussiert sich noch stärker auf den PPARG2-Promotor, was mit einem markanten Anstieg der PPARG2-Expression zusammenfällt.
Viele Helfer, wenige Reserven
Um zu prüfen, wie jeder Enhancer beiträgt, nutzte das Team CRISPR-basierte Genomeditierung, um neun einzelne Enhancer-Segmente zu löschen, die stromaufwärts, in der Nähe und stromabwärts von PPARG2 verteilt sind. Anstatt eines einzelnen Ein-/Ausschalters entdeckten sie, dass mindestens sechs dieser Enhancer für die vollständige Aktivierung von PPARG2 und die korrekte Fettzellbildung unerlässlich sind. Das Entfernen bestimmter promotor-naher Enhancer oder Teile eines großen stromabwärts gelegenen „Super-Enhancers“ schwächte die PPARG2-Aktivität deutlich ab und reduzierte die Lipidakkumulation in den resultierenden Zellen. Ein downstream liegender Enhancer, genannt E+102, war besonders kritisch: Seine Deletion verhinderte fast vollständig das Anlaufen von PPARG2, obwohl der Rest des Gens und andere Enhancer intakt blieben.
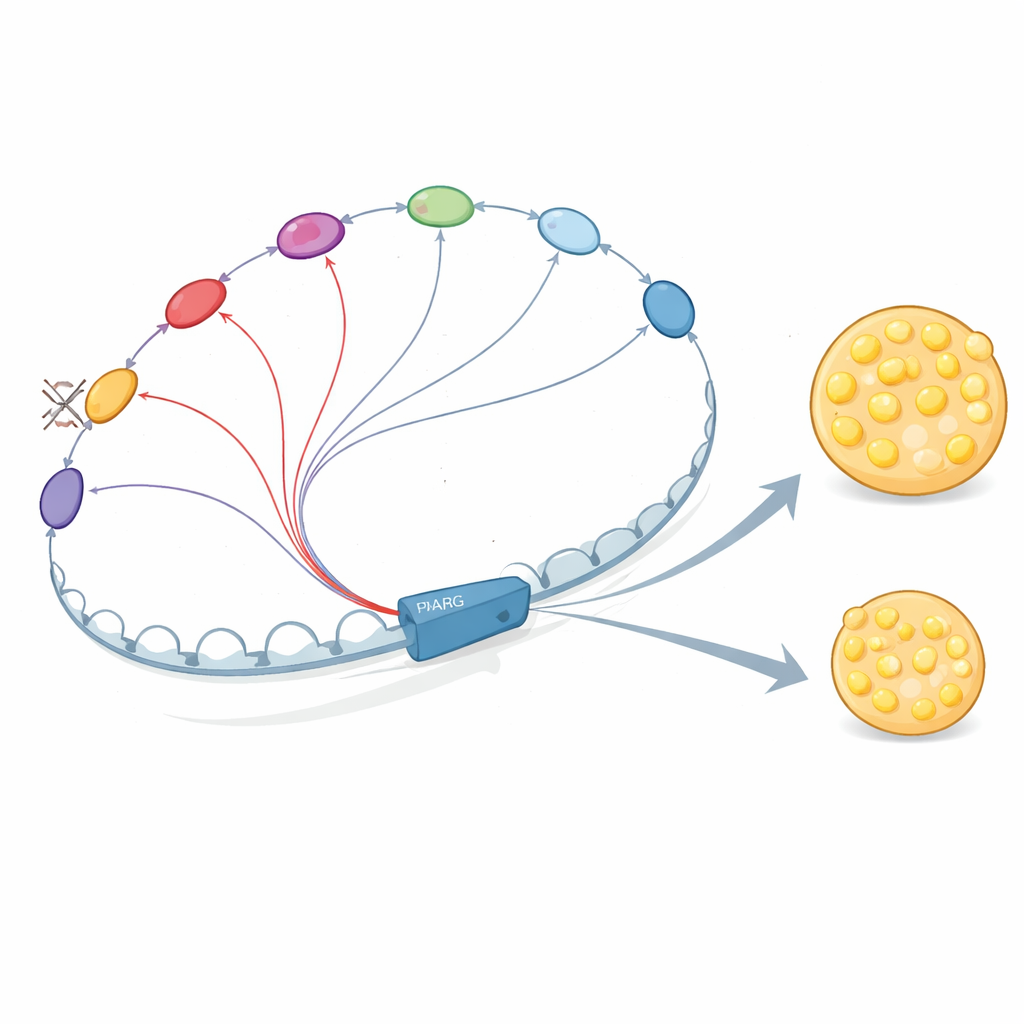
Enhancer im Dialog und in gegenseitiger Verstärkung
Warum sind diese DNA-Elemente so voneinander abhängig? Die Autoren zeigen, dass Enhancer in der PPARG2-Nachbarschaft nicht isoliert wirken. Sie rekrutieren Schlüsselregulatoren, darunter früh wirkende Faktoren wie C/EBPβ und später PPARγ selbst sowie C/EBPα. Diese Proteine binden an mehrere Enhancer, die physisch miteinander in Kontakt stehen, stabilisieren gegenseitig ihre Bindung und fördern die Rekrutierung des Mediator-Komplexes, der die Transkriptionsinitiierung unterstützt. Wenn die Forscher E+102 oder einen wichtigen promotor-nahen Enhancer entfernten, fielen die Bindungen dieser Faktoren und des Mediator-Komplexes nicht nur an der gelöschten Stelle, sondern auch an anderen Enhancern der Region ab, und das 3D-Kontaktnetzwerk schwächte sich. Das stützt das Bild, dass Enhancer–Enhancer-„Crosstalk“ einen kooperativen Hub bildet, der das PPARG2-Signal verstärkt.
Von DNA-Varianten zum Krankheitsrisiko
Schließlich verbinden die Autorinnen und Autoren dieses komplexe Kontrollsystem mit menschlichen Stoffwechselerkrankungen. Die meisten DNA-Varianten, die mit Adipositas, Cholesterinwerten oder Typ-2-Diabetes assoziiert sind, liegen außerhalb von Genen, in nichtkodierenden Regionen wie Enhancern. Durch die Kombination großer genetischer Datensätze mit einem leistungsstarken Machine-Learning-Modell der Genomregulation fanden die Forschenden heraus, dass viele hoch bewertete Risiko-Varianten innerhalb der PPARG2-Domäne direkt in die kritischsten Enhancer fallen, die sie kartiert hatten, einschließlich E+102 und promotor-naher Stellen. Einige dieser Varianten werden vorhergesagt — und in einem Fall gezeigt —, die Bindung von PPARγ oder anderen Faktoren zu verändern, wodurch die Enhancer-Aktivität und die PPARG2-Expression subtil moduliert werden. Mit anderen Worten: Kleine Veränderungen in diesem Enhancer-Netzwerk können die Fettzellfunktion einer Person in Richtung gesünder oder weniger gesund verschieben.
Was das für die metabolische Gesundheit bedeutet
Anschaulich zeigt diese Arbeit, dass das Einschalten des Schlüsselgens für Fettzellen, PPARG2, nicht die Aufgabe eines einzelnen Schalters ist, sondern eines eng aufeinander abgestimmten Teams von DNA-Kontrollelementen, die in drei Dimensionen miteinander kommunizieren. Ein besonders wichtiger Enhancer trägt sowohl zum Start des Prozesses bei als auch als zentrales Ziel für positives Feedback durch das PPARγ-Protein selbst, womit eine schnelle und robuste Festlegung auf das Fettzellschicksal sichergestellt wird. Genetische Varianten, die Teile dieser Enhancer-Gemeinschaft schwächen, können die PPARG2-Aktivierung vermindern, die Fettzellbildung oder -funktion beeinträchtigen und so zu kardiometabolischen Erkrankungen beitragen. Das Verständnis dieses vernetzten Kontrollsystems eröffnet Wege zu präziseren Risikobewertungen und möglicherweise zur gezielten Beeinflussung der Fettzellbiologie zur Verbesserung der metabolischen Gesundheit.
Zitation: Cetnarowska, A., Hyldahl, M., Nygård, M. et al. Extensive enhancer crosstalk controls PPARG2 activation during adipogenesis. Nat Commun 17, 3824 (2026). https://doi.org/10.1038/s41467-026-70401-7
Schlüsselwörter: PPARG2, Enhancer, Adipogenese, Genregulation, kardiometabolische Erkrankung