Clear Sky Science · ar
تواصل موسع بين المحسّنات يتحكم في تفعيل PPARG2 أثناء تكون الخلايا الدهنية
لماذا تهم محولات الخلايا الدهنية
غالبًا ما تُلام الخلايا الدهنية على السمنة، لكن الأنسجة الدهنية الصحية ضرورية لتخزين الطاقة بأمان والحفاظ على توازن سكر الدم والكوليسترول. عندما لا تستطيع الخلايا الدهنية أن تتكوّن أو تعمل بشكل صحيح، يتسرب الدهن إلى الكبد والعضلات والقلب، ما يزيد خطر الإصابة بالسكري وأمراض القلب. تطرح هذه الدراسة سؤالًا أساسيًا لكنه حاسم: كيف يُشغّل جين واحد في التوقيت الملائم لتحويل خلية غير ناضجة إلى خلية دهنية مكتملة؟ ومن خلال كشف هذا الجواب، تسلّط الدراسة الضوء على سبب تعرض بعض الأشخاص لخطر أعلى للإصابة بأمراض أيضية — وكيف يمكن لتغييرات صغيرة في الحمض النووي بعيدة عن الجينات أن تُحدث تأثيرات كبيرة على الصحة.
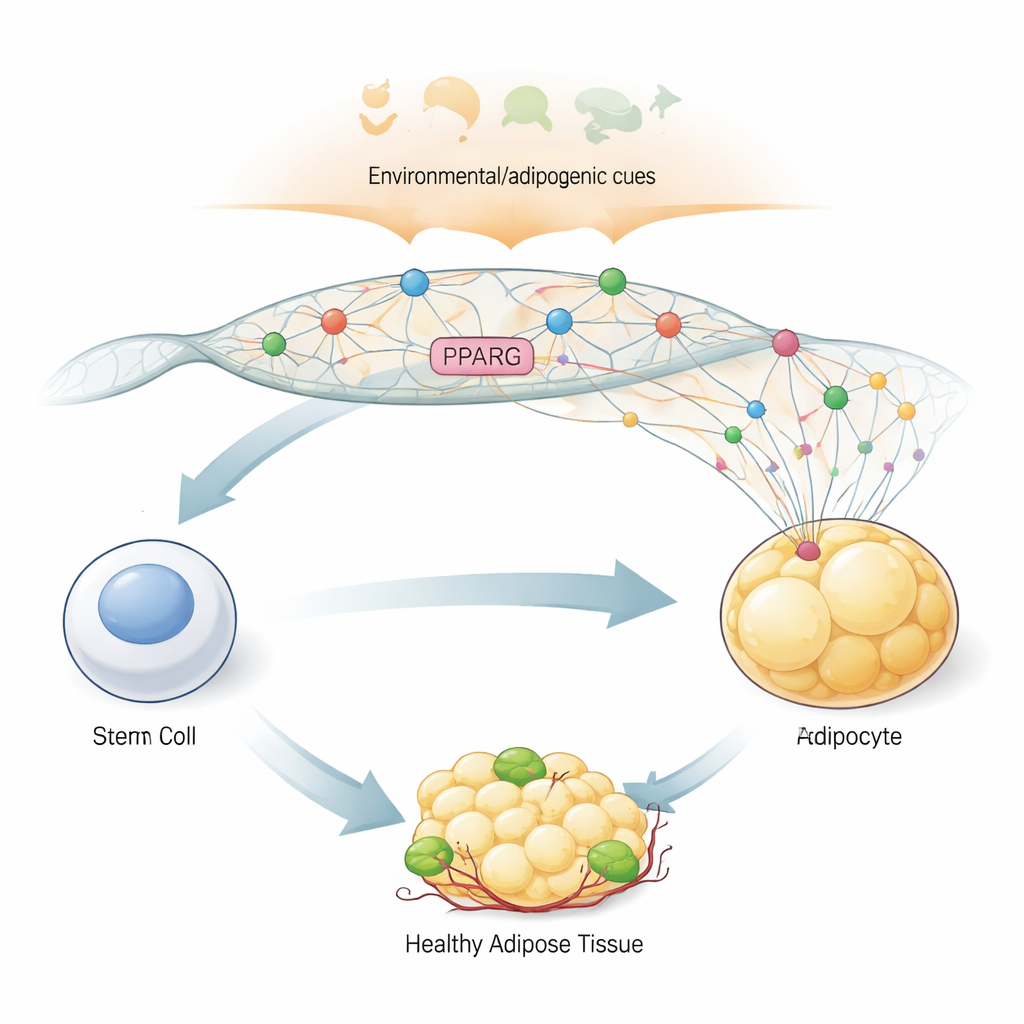
المفتاح الرئيسي لتكوين خلية دهنية
لتحويل خلية شبيهة بالخلايا الجذعية إلى خلية دهنية، يعتمد الجسم على جين «مفتاح رئيسي» يسمى PPARG2، الذي يُنتج البروتين PPARγ2. يتحكم هذا البروتين في مئات الجينات الأخرى المسؤولة عن تخزين الدهن، والحساسية للإنسولين، وإنتاج الهرمونات في الأنسجة الدهنية. وبفضل دوره المحوري، يجب أن يبقى PPARG2 مطفأً في الخلايا السابقة ثم يُشغّل بسرعة وقوة عندما تطلق الجسم إشارات تكوّن الخلايا الدهنية التي تقول، بعبارة مجازية، «كوّنوا خلايا دهنية الآن». استخدم المؤلفون نموذج خلايا جذعية مشتقّة من نخاع العظم البشري يمكن توجيهها نحو الخلايا الدهنية في المختبر، مما سمح لهم بمراقبة خطوة بخطوة كيف يتغير شكل ونشاط منطقة PPARG2 في الجينوم أثناء التمايز.
حي ثلاثي الأبعاد مهيأ للتغيير
يجلس جين PPARG2 داخل حي ثلاثي الأبعاد معزول من الحمض النووي يُعرف باسم نطاق، معزولًا ماديًا عن الجينات المحيطة. حتى قبل أن تلتزم الخلايا بأن تصبح دهنية، يكون هذا النطاق مُعَدًا بالفعل: علامات كيميائية على الحمض النووي والبروتينات المحيطة تشير إلى مجموعة من عناصر التحكم، تُسمى المحسّنات، بوصفها نقاط تنظيم مستقبلية. باستخدام أساليب رسم خرائط الجينوم ثلاثي الأبعاد، وجد الباحثون أن هذه المحسّنات تتواصل بالفعل مع بعضها عبر مسافات طويلة، وتشكل مجتمعًا مترابطًا حول PPARG2. عندما تتلقى الخلايا إشارات تكوّن الخلايا الدهنية، تقوى هذه الاتصالات، وتظهر علامات نشاط جديدة، ويركز شبكة المحسّنات تركيزًا أكبر على مروّج PPARG2، بالتزامن مع ارتفاع حاد في تعبير PPARG2.
مساعدون كثيرون وقليل من البدائل
لاختبار مساهمة كل محسّن، استخدم الفريق تحرير الجينوم المبني على CRISPR لحذف تسعة مقاطع محسّن فردية متفرقة أعلاه، وقريبًا من، وتحت PPARG2. بدلًا من العثور على مفتاح واحد للتشغيل/الإيقاف، اكتشفوا أن ما لا يقل عن ستة من هذه المحسّنات ضرورية للتفعيل الكامل لـ PPARG2 وتكوين الخلايا الدهنية السليم. أدت إزالة بعض المحسّنات القريبة من المروّج أو أجزاء من «المحسّن الفائق» الكبير الموجود أسفل الجين إلى تقليل نشاط PPARG2 بشكل كبير وتقليل تراكم الدهون في الخلايا الناتجة. كان أحد المحسّنات السفلية، المسمى E+102، حاسمًا بشكل خاص: فحذفه كاد أن يمنع تشغيل PPARG2 تمامًا، بالرغم من بقاء بقية الجين والمحسّنات الأخرى سليمة.
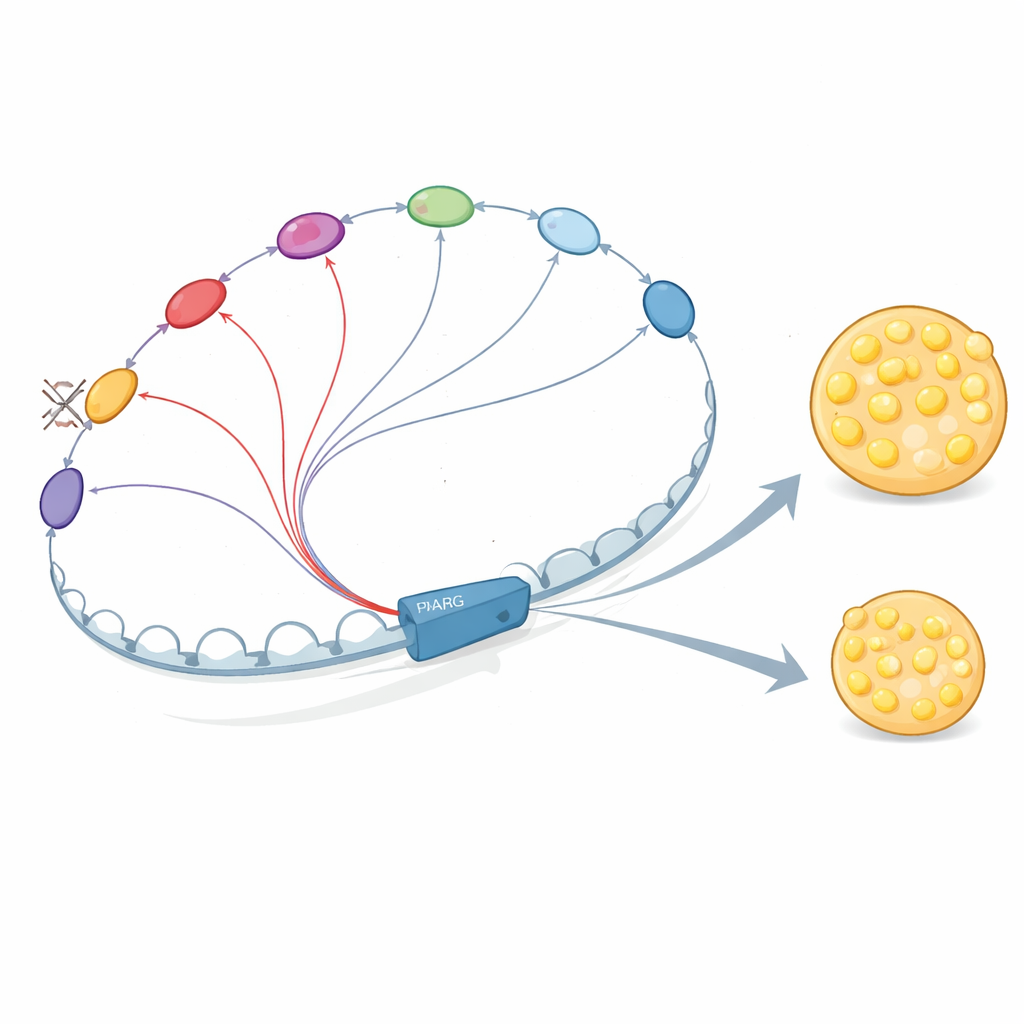
المحسّنات تتواصل وتعزّز بعضها البعض
لماذا تُعد هذه العناصر من الحمض النووي مترابطة إلى هذا الحد؟ يُظهر المؤلفون أن المحسّنات في حي PPARG2 لا تعمل بمعزل عن بعضها. إنها تُجنّد بروتينات تنظيمية رئيسية، بما في ذلك عوامِل مبكرة الفعل مثل C/EBPβ ولاحقًا PPARγ نفسه وC/EBPα. ترتبط هذه البروتينات بعدة محسنّات تتصل ماديًا ببعضها، مما يُثبّت ارتباطها ويعزّز استقطاب مركب Mediator، الذي يساعد على بدء النسخ. عندما أزال الباحثون E+102 أو محسّنًا رئيسيًا قريبًا من المروّج، انخفض ارتباط هذه العوامل ومركب Mediator ليس فقط في الموقع المحذوف بل عبر محسنّات أخرى في النطاق، وضعُفت شبكة الاتصال الثلاثية الأبعاد. وهذا يدعم تصورًا تقوم فيه «المحادثة» بين المحسّنات بخلق محور تعاوني يضخّم إشارة PPARG2.
من متغيرات الحمض النووي إلى خطر المرض
أخيرًا، تربط الدراسة هذا النظام الرقابي المعقّد بالأمراض الأيضية البشرية. تقع معظم متغيرات الحمض النووي المرتبطة بالسمنة أو مستويات الكوليسترول أو داء السكري من النوع 2 خارج الجينات، في مناطق غير مشفّرة مثل المحسّنات. بدمج مجموعات بيانات جينية كبيرة مع نموذج قوي للتعلّم الآلي حول تنظيم الجينوم، وجد المؤلفون أن العديد من المتغيرات الأعلى تصنيفًا داخل نطاق PPARG2 تقع مباشرة داخل أهم المحسّنات التي رسموها، بما في ذلك E+102 ومواقع قريبة من المروّج. البعض من هذه المتغيرات متوقع — وفي حالة واحدة مبين — أن يغيّر مدى ارتباط PPARγ أو عوامل أخرى، مغيرةً بنعومة نشاط المحسّن وتعبير PPARG2. بعبارة أخرى، قد تُدفع تعديلات صغيرة على شبكة المحسّنات هذه بخلايا الدهن لدى الشخص نحو سلوكٍ أكثر صحة أو أقل صحة.
ما الذي يعنيه هذا للصحة الأيضية
بعبارات يومية، تُظهر هذه الدراسة أن تشغيل جين الخلايا الدهنية الرئيسي PPARG2 ليس مهمة مفتاح واحد بل فريق مُنسق من عناصر التحكم في الحمض النووي التي تتواصل ثلاثيًا. يساعد محسّن واحد مهم بشكل خاص في بدء العملية ثم يعمل كهدف رئيسي للتغذية الراجعة الإيجابية من بروتين PPARγ نفسه، ما يضمن التزامًا سريعًا وقويًا بمصير الخلية الدهنية. قد تُضعف المتغيرات الجينية التي تضعف أجزاء من هذا المجتمع المحسّنات تنشيط PPARG2، وتعيق تكوين الخلايا الدهنية أو وظائفها، وبالتالي تساهم في الأمراض القلبية والتمثيل الغذائي. إن فهم هذا النظام الرقابي المتشابك يفتح الباب أمام طرق أكثر دقة لتقييم المخاطر وربما ضبط بيولوجيا الخلايا الدهنية لتحسين الصحة الأيضية.
الاستشهاد: Cetnarowska, A., Hyldahl, M., Nygård, M. et al. Extensive enhancer crosstalk controls PPARG2 activation during adipogenesis. Nat Commun 17, 3824 (2026). https://doi.org/10.1038/s41467-026-70401-7
الكلمات المفتاحية: PPARG2, المحسّنات, تكوّن الخلايا الدهنية, تنظيم الجينات, أمراض القلب والتمثيل الغذائي