Clear Sky Science · tr
TMBIM6, Parkinson hastalığında IRE1α yolunu düzenleyerek dopaminerjik nöronların hayatta kalmasını artırıyor
Bu araştırma Parkinson’lu kişiler için neden önemli
Parkinson hastalığı, dopamin üreten kilit beyin hücrelerinin yavaşça ölmesiyle pürüzsüz hareketi elinden alır. Bu çalışma, bu savunmasız nöronların protein katlanma mekanizması içindeki strese karşı koymasına yardımcı olan TMBIM6 adlı yerleşik bir koruyucu proteini ortaya koyuyor. TMBIM6’yı artırmanın nöronları canlı tutabileceğini ve hayvan modellerinde hareketi iyileştirebileceğini göstererek, çalışmanın dopamin yerine koymanın ötesinde yeni bir terapötik yaklaşım sunduğu anlaşılıyor.
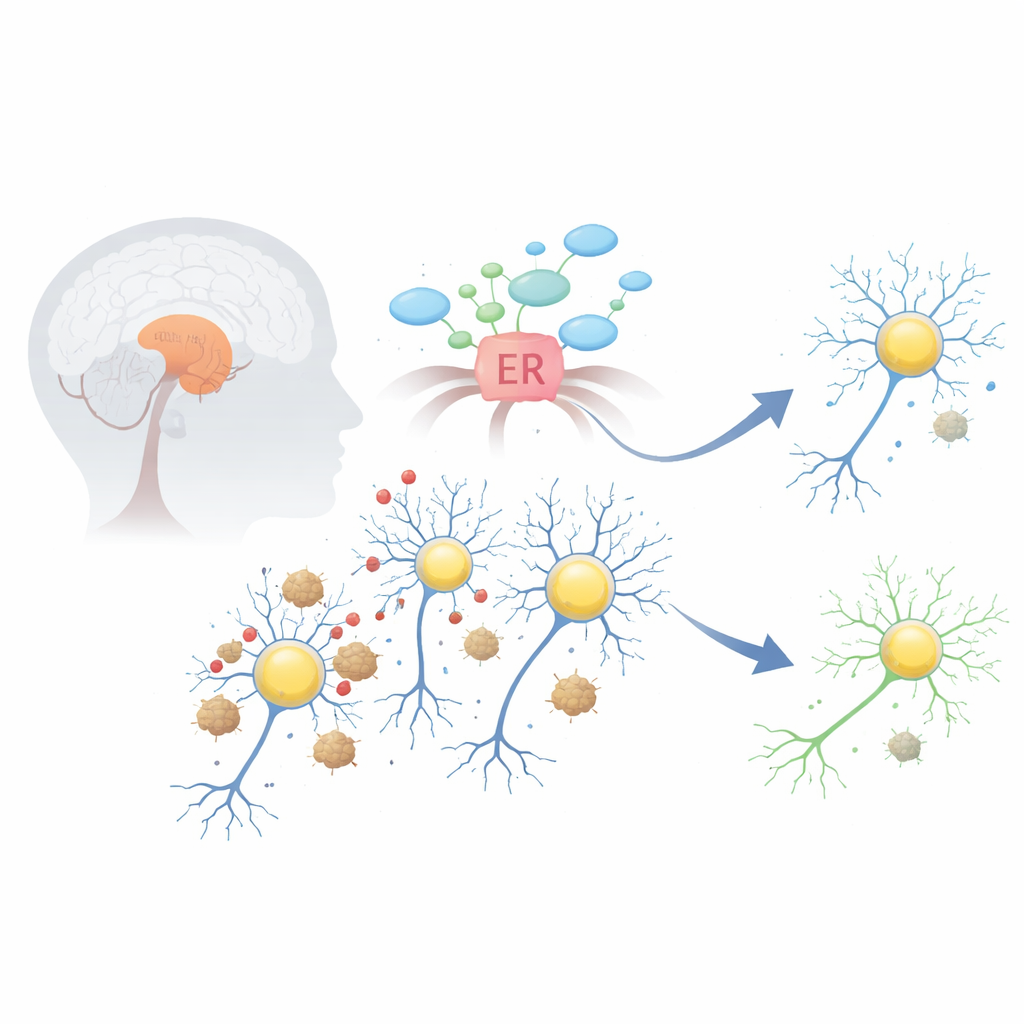
Dopamin üreten beyin hücreleri içindeki sorun
Parkinson hastalığında alpha-sinüklein adlı bir protein yanlış katlanıp yapışkan kümeler halinde toplanabilir ve Lewy cisimcikleri olarak bilinen yapıların oluşmasına yol açar. Bu kümeler, orta beyin bölgesindeki substantia nigra’da yer alan dopamin üreten nöronlarda bir dizi hayati sistemi bozuyor. Erken ve en zararlı etkilerden biri, hücrenin proteinleri katlayan ve işleyen fabrikası olan endoplazmik retikulumda (ER) stres oluşmasıdır. Bu kompartıman bunaldığında, başlangıçta yardımcı olabilecek ama uzun süre açık kalırsa hücreleri kendi kendini yok etmeye itecek bir acil durum programı olan açılmamış protein yanıtını (UPR) devreye sokar.
Doğal bir kalkan: TMBIM6 güvenlik anahtarı
TMBIM6 proteini endoplazmik retikulum zarında yer alır ve normalde IRE1α adlı anahtar bir stres algılayıcısına fren görevi görür. Araştırmacılar önce TMBIM6’nın Parkinson’da önemli olabilecek doğru yerde bulunup bulunmadığını sorguladılar. Büyük gen ifadesi veritabanlarını kullanarak, TMBIM6’nın insan orta beyninde ve dopamin nöronları açısından zengin diğer bölgelerde yüksek düzeyde ifade edildiğini buldular. Kültürdeki hücrelerde ve 6-hidroksidopamin, rotenon veya alpha-sinüklein fibrilleri gibi Parkinson benzeri toksinlere maruz bırakılmış fare nöronlarında TMBIM6 düzeyleri erken dönemde yükseldi; bu da hücrelerin bu faktörü strese hızlı bir savunma yanıtı olarak açtığını düşündürüyor.
Kırılgan nöronlarda korumanın başarısız olduğu durumlar
Bu belirgin savunmaya rağmen, Parkinson’da dopamin nöronları hâlâ ölür. Nedenini anlamak için ekip, Parkinson’lu kişilerin beyin dokusu ve tek hücre genetik verilerini inceledi. Genel olarak, hastalıklı orta beyin dokusunda TMBIM6 proteini kontrollerden daha yüksekti, ancak daha ayrıntılı bakış önemli bir ayrıntıyı ortaya koydu: en hassas olduğu bilinen dopamin nöronu alt tipinde TMBIM6 ifadesi, daha dirençli nöronlara göre aslında daha düşüktü. Aynı zamanda TMBIM6 ile diğer stres yanıtı genleri arasındaki normal sıkı koordinasyon bozulmuştu. Bu bulgular birlikte, bazı beyin hücrelerinin TMBIM6’yı artırdığı halde en korumaya ihtiyaç duyan nöronların bu güvenlik anahtarını kaybedebileceğini, böylece kronik stres ve ölüm sinyallerine açık kaldıklarını göstermektedir.
Hücrelerde ve sineklerde nedenselliği kanıtlama
TMBIM6’nın gerçekten hayatta kalmayı etkileyip etkilemediğini test etmek için araştırmacılar bu proteinin düzeylerini birkaç laboratuvar modelinde artırıp azalttılar. Dopamin benzeri fare hücrelerinde TMBIM6’yı azalttıklarında, bu hücreler toksik alpha-sinüklein fibrillerine ve Parkinson’ı taklit eden kimyasal toksinlere karşı çok daha duyarlı hale geldi. Hücreler mitokondriyal işlev kaybı, kaspaz-3 gibi infazcı enzimlerin daha yüksek düzeyde aktivasyonu ve hücre içeriklerinin daha fazla sızması—programlı hücre ölümünün belirteçleri—gösterdi. TMBIM6 eşdeğerini daha az üretecek şekilde genetik olarak değiştirilmiş meyve sineklerinde benzer sonuçlar gözlendi: göz ve beyindeki dopamin nöronlarını kaybettiler ve özellikle rotenon pestisidine maruz kaldıklarında daha ağır hareket sorunları geliştirdiler.
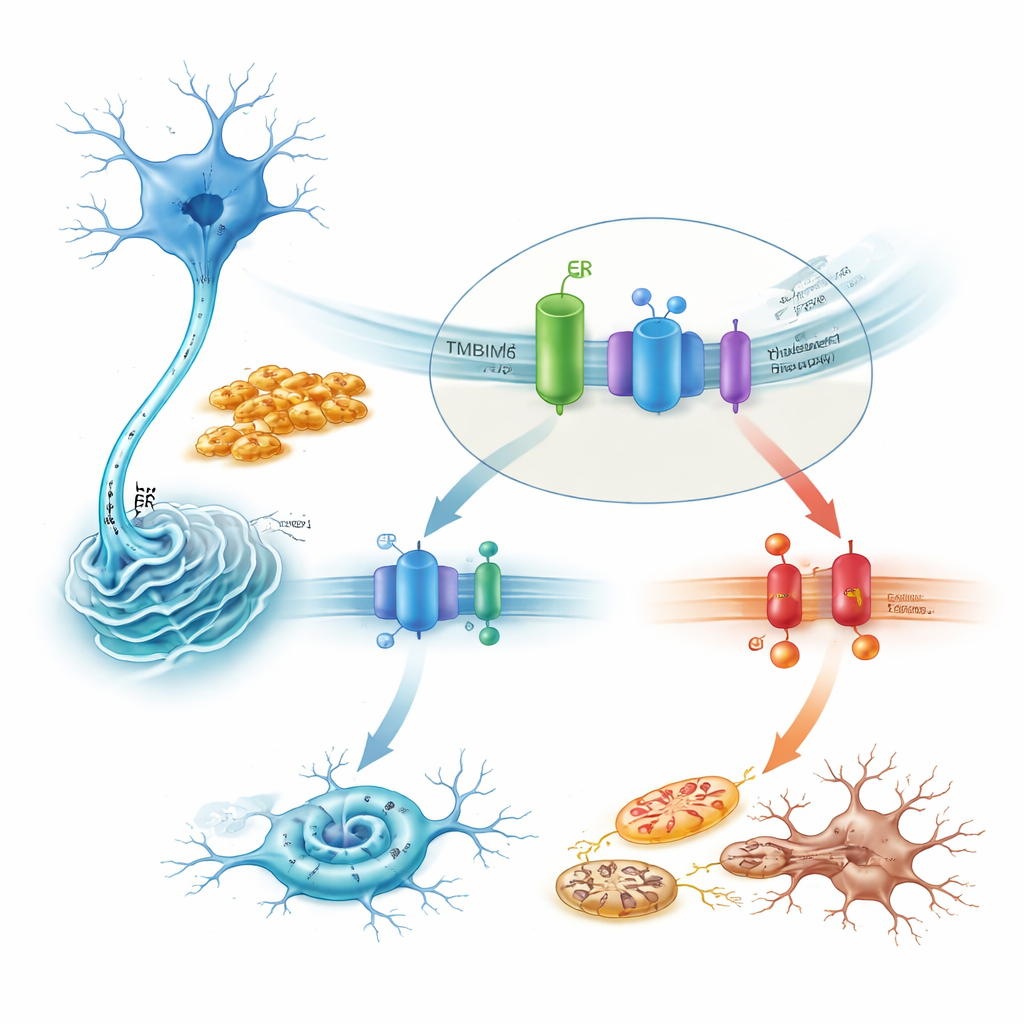
TMBIM6’nın öldürücü bir stres yolunu nasıl dizginlediği
Mekanizmaya yakından bakıldığında, çalışma TMBIM6’nın dinlenme koşullarında fiziksel olarak IRE1α ile ilişki kurduğunu gösteriyor. Toksik alpha-sinüklein fibrilleri bu ortaklığı bozarak IRE1α’nın güçlü bir şekilde açılmasına izin veriyor. TMBIM6 eksikliğindeki hücrelerde bu aktivasyon abartılıyor; XBP1 haberci RNA’sının artan kesilmesi ve IRE1α’nın başka bir hedefinin bozulmasıyla gösterildiği gibi. IRE1α’yı ilaçlarla bloke etmek veya genini susturmak, TMBIM6 eksik olduğunda görülen artmış hücre ölümünü büyük ölçüde geri aldı. Aşağıda zararlı yol, stres kinazı JNK, pro-ölüm proteini BAX ve kaspazlar aracılığıyla ilerleyerek apoptozu tetikliyor. Buna karşılık TMBIM6’yı fazla eksprese etmek IRE1α aktivitesini bastırdı, bu ölüm sinyallerini azalttı ve mitokondrileri korudu; alpha-sinüklein birikiminin miktarını değiştirmedi—bu da TMBIM6’nın kümelerin kendisine değil hücrenin stresle başa çıkma mekanizmasına etki ettiğini gösteriyor.
Farelerde gen-terapisine benzeyen bir yaklaşımı test etmek
Terapötik potansiyeli araştırmak için yazarlar, insan TMBIM6’yı farelerin substantia nigra’sına doğrudan teslim etmek amacıyla zararsız bir adeno-ilişkili virüs (AAV) kullandılar. İki hafta sonra, dopamin yolunu standart bir Parkinson toksini olan 6-hidroksidopamin ile zedelediler. Sadece bir işaretçi gen alan kontrol fareleri belirgin motor sorunlar geliştirdi: etkilenen ön bacağı daha az kullanma ve bir kiriş testinde dengesizlik. Ancak TMBIM6 taşıyan virüsle önceden tedavi edilen fareler belirgin şekilde daha iyi performans gösterdi; daha az hata yaptılar ve görevleri daha hızlı tamamladılar. Kültürdeki primer nöronlarda da aynı AAV yapı toksinler veya alpha-sinüklein fibrillerinin tetiklediği hücre ölümü ve kaspaz aktivasyonunu hafifletti; bu da TMBIM6 düzeylerini artırmanın nöron direncini güçlendirdiği savını destekliyor.
Gelecekteki tedaviler için bunun anlamı
Bu bulgular TMBIM6’yı, tehlikeli bir stres algılayıcısı olan IRE1α’yı kontrol altında tutarak ve mitokondri başarısızlığı ile apoptoza yol açan olaylar zincirini önleyerek dopamin nöronlarının koruyucusu olarak resmediyor. Hastalığın erken döneminde hücreler TMBIM6’yı bir başa çıkma stratejisi olarak yükseltir gibi görünse de, en risk altındaki nöronlarda sistem nihayetinde çöker ve denge kronik stres ve hücre ölümüne kayar. TMBIM6’yı onarmak veya güçlendirmek—işlevini artıran ilaçlar veya burada test edilen AAV benzeri gen terapileri yoluyla—Parkinson hastalığında mevcut tedavilerin çoğunlukla dopamini yerine koymaya odaklanmasının ötesinde nöron kaybını yavaşlatma veya önleme yolu sunabilir.
Atıf: Ahumada-Montalva, P., Muñoz-Carvajal, F., Bórquez-Macaya, S. et al. TMBIM6 enhances dopaminergic neuron survival by modulating the IRE1a pathway in Parkinson’s disease. Cell Death Dis 17, 385 (2026). https://doi.org/10.1038/s41419-025-08391-5
Anahtar kelimeler: Parkinson hastalığı, dopaminerjik nöronlar, endoplazmik retikulum stresi, IRE1α yolu, nöroproteksiyon