Clear Sky Science · ar
يُحسّن TMBIM6 بقاء الخلايا العصبية الدوبامينية عبر تعديل مسار IRE1α في مرض باركنسون
لماذا يهم هذا البحث للأشخاص المصابين بمرض باركنسون
يسلب مرض باركنسون من المصابين الحركة السلسة لأن خلايا دماغية رئيسية تُنتج الدوبامين تموت ببطء. يكشف هذا البحث عن بروتين وقائي داخلي يُسمى TMBIM6 يساعد هذه الخلايا العصبية الضعيفة على التعامل مع الإجهاد داخل آلية طي البروتين. من خلال إظهار كيف أن تعزيز TMBIM6 يمكن أن يبقي الخلايا العصبية على قيد الحياة ويحسّن الحركة في نماذج حيوانية، يشير العمل إلى نهج علاجي جديد يتجاوز مجرد استبدال الدوبامين.
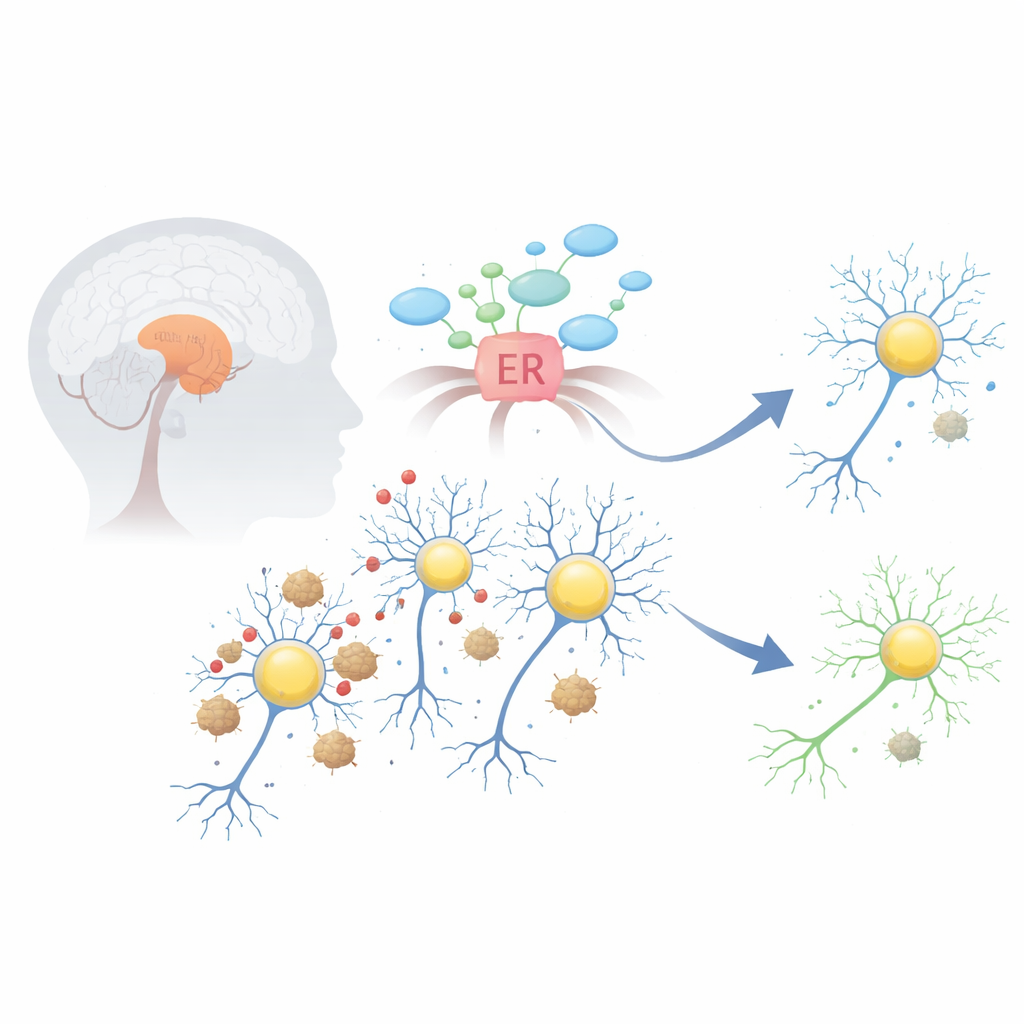
المشكلة داخل الخلايا المنتجة للدوبامين
في مرض باركنسون، يمكن أن يطرأ طي خاطئ على بروتين يُدعى ألفا-سينوكلين ويتكدس ليكوّن تجمعات لزجة تُعرف بأجسام لوي. تعمل هذه التكتلات على تعطيل عدة أنظمة حيوية داخل الخلايا المنتجة للدوبامين في منطقة منتصف الدماغ المعروفة بالمادة السوداء. أحد التأثيرات المبكرة والأكثر ضرراً هو الإجهاد في الشبكة الإندوبلازمية، مصنع الخلية لطي ومعالجة البروتينات. عندما تغمر هذه الحجرة بالعمل تفَعّل برنامج طوارئ يُسمى استجابة البروتين غير المطوي، والذي قد يساعد مبدئياً لكنه، إذا استمر لفترة طويلة، يبدأ بدفع الخلايا نحو الانتحار الخلوي.
درع طبيعي: مفتاح الأمان TMBIM6
يتوضع بروتين TMBIM6 في غشاء الشبكة الإندوبلازمية ويعمل عادةً كفرامل على جهاز استشعار الإجهاد الرئيسي المسمى IRE1α. سأل الباحثون أولاً ما إذا كان TMBIM6 موجوداً في الموضع الصحيح ليكون مهماً في باركنسون. باستخدام قواعد بيانات تعبير الجينات الكبيرة، وجدوا أن TMBIM6 مُعبر عنه بكثافة في منتصف الدماغ البشري ومناطق أخرى غنية بخلايا الدوبامين. في خلايا مزروعة وعصبونات فأر تعرضت لسموم شبيهة بباركنسون—مثل 6-هيدروكزيدوبامين، الروتينون، أو ألياف ألفا-سينوكلين—ارتفعت مستويات TMBIM6 مبكراً، مما يشير إلى أن الخلايا تُشغّل هذا العامل كاستجابة دفاعية سريعة للإجهاد.
عندما يفشل الحماية في الخلايا الضعيفة
رغم هذا الدفاع الظاهري، تستمر خلايا الدوبامين في الموت في مرض باركنسون. لفهم السبب، فحص الفريق أنسجة دماغية وبيانات جينية خلوية أحادية من أشخاص أصيبوا بالمرض. بشكل عام، كان بروتين TMBIM6 أعلى في نسيج منتصف الدماغ المصاب مقارنة بالضوابط، لكن نظرة أكثر تفصيلاً كشفت تحوّلاً حاسماً: داخل النوع الفرعي نفسه من خلايا الدوبامين المعروفة بالأكثر عرضة للخطر، كان تعبير TMBIM6 فعلياً أقل مقارنة بالخلايا الأكثر مقاومة. في الوقت نفسه، تعرّض التنسيق المعتاد بين TMBIM6 وجينات الاستجابة للإجهاد الأخرى للاضطراب. تقترح هذه النتائج معاً أنه بينما ترفع بعض خلايا الدماغ TMBIM6، فإن الخلايا العصبية التي في أمسّ الحاجة إلى الحماية قد تفقد مفتاح الأمان هذا، مما يتركها عرضة للإجهاد المزمن وإشارات الموت.
إثبات السبب والنتيجة في الخلايا والذباب
لاختبار ما إذا كان TMBIM6 يؤثر فعلاً على البقاء، عدّل الباحثون مستوياته صعوداً وهبوطاً في عدة نماذج مخبرية. عندما قلّلوا TMBIM6 في خلايا فأر شبيهة بالدوبامين، أصبحت تلك الخلايا أكثر حساسية بكثير لألياف ألفا-سينوكلين السامة وللسموم الكيميائية التي تحاكي باركنسون. أظهرت الخلايا فقداناً أكبر لوظيفة الميتوكوندريا، وتنشيطاً أعلى لإنزيمات القتل مثل كاسبيز-3، وتسرباً أكبر لمحتويات الخلية—علامات مميزة للموت المبرمج للخلايا. ظهرت نتائج مماثلة في ذباب الفاكهة المصمم لإنتاج كمية أقل من المعادل لـ TMBIM6: فقدوا خلايا دوبامين في العين والدماغ وطوروا مشاكل حركية أسوأ، خصوصاً عند تعرضهم لمبيد الحشرات الروتينون.
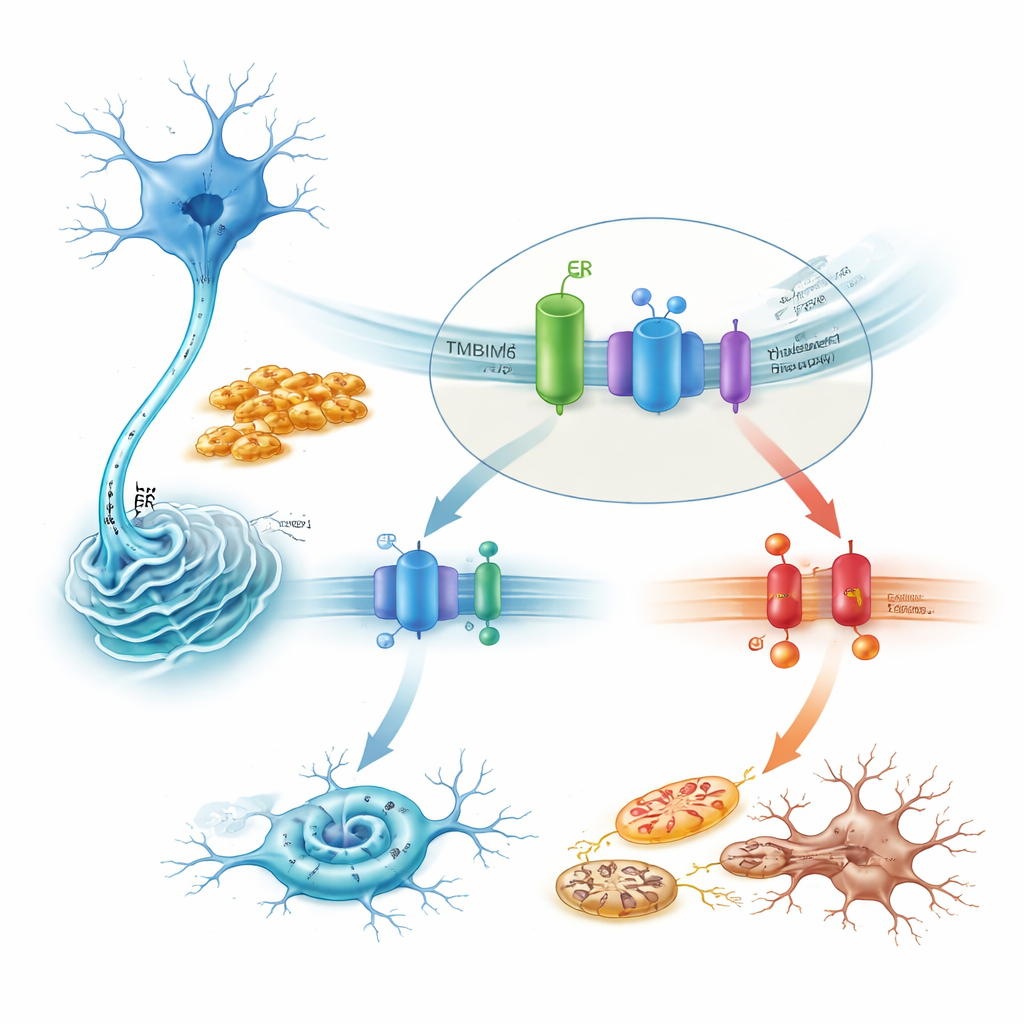
كيف يروي TMBIM6 مسار إجهاديًا قاتلاً
بالتركيز على الآلية، تُظهر الدراسة أن TMBIM6 يرتبط بدنيا مع IRE1α في الظروف الراحة. تزعزع ألياف ألفا-سينوكلين السامة هذه الشراكة، محررة IRE1α للتفعيل القوي. في الخلايا الناقصة لـ TMBIM6، يصبح هذا التفعيل مبالغاً فيه، كما يتضح بزيادة اقتطاع الرنا الناقل الخاص بـ XBP1 وتحلل هدف آخر لـ IRE1α. حجب IRE1α بالأدوية أو بإسكات جينِه أعاد إلى حد بعيد الإنقاذ من زيادة موت الخلايا التي رُصدت عند غياب TMBIM6. أسفل السلسلة، سار المسار الضار عبر كيناز الإجهاد JNK، والبروتين المسبب للموت BAX، والكاسبيزات، مكوِّناً سلسلة تدفع نحو الاستماتة. بالمقابل، قلّل الإفراط في التعبير عن TMBIM6 نشاط IRE1α، وخفّض إشارات الموت هذه، وحمى الميتوكوندريا، دون تغيير مقدار تجمّع ألفا-سينوكلين—مما يشير إلى أن TMBIM6 يؤثر على معالجة الخلايا للإجهاد بدلاً من التأثير على التجمعات نفسها.
اختبار نهج شبيه بالعلاج الجيني في الفئران
لاستكشاف الإمكانات العلاجية، استخدم المؤلفون فيروساً غدياً مرتبطاً آمنًا (AAV) لتوصيل الجين البشري TMBIM6 مباشرةً إلى المادة السوداء في الفئران. بعد أسبوعين، ألحَقوا ضرراً بمسار الدوبامين باستخدام سم باركنسون القياسي، 6-هيدروكزيدوبامين. الفئران الضابطة التي تلقت جين علامة فقط طورت مشكلات حركية واضحة: انخفاض استخدام الطرف الأمامي المتأثر وتراجع التوازن في اختبار الشعاع. أما الفئران التي عولجت مسبقاً بالفيروس الحامل لـ TMBIM6 فقد أدت أداءً أفضل بشكل ملحوظ، مرتكبة أخطاء أقل وكاملةً المهام بسرعة أكبر. في الخلايا الأولية المزروعة، خفف نفس ناقل AAV موت الخلايا وتنشيط الكاسبيز الناتج عن السموم أو ألياف ألفا-سينوكلين، مما يعزز الحجة بأن رفع مستويات TMBIM6 يعزز مرونة الخلايا العصبية.
ماذا قد يعني هذا للعلاجات المستقبلية
ترسم هذه النتائج معاً صورة TMBIM6 كحارس لخلايا الدوبامين يعمل عن طريق إبقاء حساس إجهاد خطير، IRE1α، تحت السيطرة ومنع سلسلة من الأحداث التي تؤدي إلى فشل الميتوكوندريا والاستماتة. في المراحل المبكرة من المرض، يبدو أن الخلايا ترفع TMBIM6 كاستراتيجية تكيّف، لكن في الخلايا العصبية الأكثر عرضة ينهار النظام في النهاية، مائلًا الميزان نحو الإجهاد المزمن وموت الخلايا. قد يوفر استعادة أو تضخيم TMBIM6—عبر أدوية تعزز وظيفته أو عبر علاجات جينية شبيهة بـ AAV المختبرة هنا—سبيلًا لإبطاء أو منع فقدان الخلايا العصبية في مرض باركنسون، مكملاً العلاجات الحالية التي تركز أساساً على استبدال الدوبامين بدلاً من حماية الخلايا المنتجة له.
الاستشهاد: Ahumada-Montalva, P., Muñoz-Carvajal, F., Bórquez-Macaya, S. et al. TMBIM6 enhances dopaminergic neuron survival by modulating the IRE1a pathway in Parkinson’s disease. Cell Death Dis 17, 385 (2026). https://doi.org/10.1038/s41419-025-08391-5
الكلمات المفتاحية: مرض باركنسون, الخلايا العصبية الدوبامينية, إجهاد الشبكة الإندوبلازمية, مسار IRE1α, الحماية العصبية