Clear Sky Science · fr
TMBIM6 améliore la survie des neurones dopaminergiques en modulant la voie IRE1α dans la maladie de Parkinson
Pourquoi cette recherche importe pour les personnes atteintes de Parkinson
La maladie de Parkinson prive les personnes de mouvements fluides parce que des cellules cérébrales clés productrices de dopamine meurent progressivement. Cette étude met au jour une protéine protectrice intrinsèque, appelée TMBIM6, qui aide ces neurones vulnérables à faire face au stress dans leur machinerie de repliement des protéines. En montrant comment l’augmentation de TMBIM6 peut préserver les neurones et améliorer les mouvements chez des modèles animaux, le travail ouvre une piste thérapeutique nouvelle au-delà du simple remplacement de la dopamine.
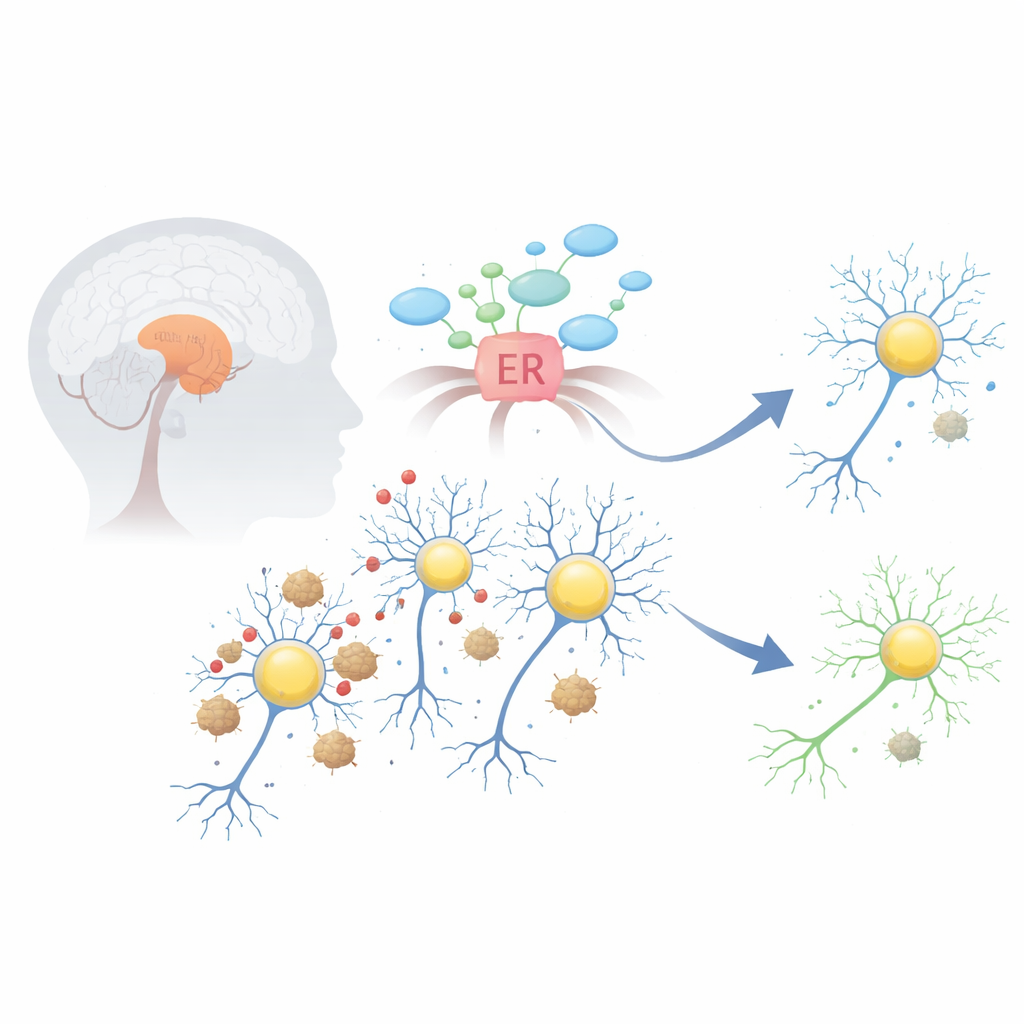
Le problème à l’intérieur des cellules productrices de dopamine
Dans la maladie de Parkinson, une protéine nommée alpha-synucléine peut se replier de façon incorrecte et s’agglomérer en agrégats collants, formant des structures appelées corps de Lewy. Ces amas perturbent plusieurs systèmes vitaux au sein des neurones producteurs de dopamine d’une région du mésencéphale appelée la substance noire. Un des effets précoces et les plus délétères est le stress du réticulum endoplasmique, la « usine » cellulaire de repliement et de traitement des protéines. Lorsque cette compartimentation est débordée, elle active un programme d’urgence nommé réponse aux protéines mal repliées, qui peut d’abord aider mais, si elle reste activée trop longtemps, pousse les cellules vers l’autodestruction.
Un bouclier naturel : l’interrupteur de sécurité TMBIM6
La protéine TMBIM6 est située dans la membrane du réticulum endoplasmique et agit normalement comme un frein sur un capteur de stress clé appelé IRE1α. Les chercheurs ont d’abord vérifié si TMBIM6 est présente au bon endroit pour jouer un rôle dans la maladie de Parkinson. En utilisant de larges bases de données d’expression génique, ils ont constaté que TMBIM6 est fortement exprimée dans le mésencéphale humain et d’autres régions riches en neurones dopaminergiques. Dans des cellules en culture et des neurones de souris exposés à des toxines de type Parkinson — comme la 6-hydroxydopamine, le rotenone ou des fibrilles d’alpha-synucléine — les niveaux de TMBIM6 ont augmenté précocement, suggérant que les cellules activent ce facteur comme réponse défensive rapide au stress.
Quand la protection échoue dans les neurones vulnérables
Malgré cette défense apparente, les neurones dopaminergiques continuent de mourir dans la maladie de Parkinson. Pour comprendre pourquoi, l’équipe a examiné des tissus cérébraux et des données génétiques monocellulaires de personnes ayant eu la maladie. Globalement, la protéine TMBIM6 était plus élevée dans le tissu mésencéphalique malade que dans les témoins, mais un examen plus fin révèle un tournant crucial : au sein du sous-type même de neurones dopaminergiques connu pour être le plus vulnérable, l’expression de TMBIM6 était en réalité plus faible que dans les neurones plus résistants. Parallèlement, la coordination habituelle entre TMBIM6 et d’autres gènes de réponse au stress était perturbée. Ensemble, ces observations suggèrent que si certaines cellules cérébrales augmentent TMBIM6, les neurones qui ont le plus besoin de protection peuvent perdre cet interrupteur de sécurité, les laissant exposés à un stress chronique et à des signaux de mort.
Prouver la cause et l’effet dans des cellules et des mouches
Pour tester si TMBIM6 influence réellement la survie, les chercheurs ont modulé ses niveaux à la hausse et à la baisse dans plusieurs modèles expérimentaux. Lorsqu’ils ont réduit TMBIM6 dans des cellules murines de type dopaminergique, ces cellules sont devenues beaucoup plus sensibles aux fibrilles toxiques d’alpha-synucléine et aux toxiques chimiques imitant la maladie de Parkinson. Les cellules présentaient une perte plus marquée de la fonction mitochondriale, une activation accrue d’enzymes exécutrices comme la caspase-3, et davantage de fuite de contenu cellulaire — signes typiques de mort cellulaire programmée. Des résultats similaires sont apparus chez la drosophile génétiquement modifiée pour produire moins d’équivalent de TMBIM6 : elle perdait des neurones dopaminergiques dans l’œil et le cerveau et développait des troubles moteurs plus graves, en particulier lorsqu’elle était exposée au pesticide rotenone.
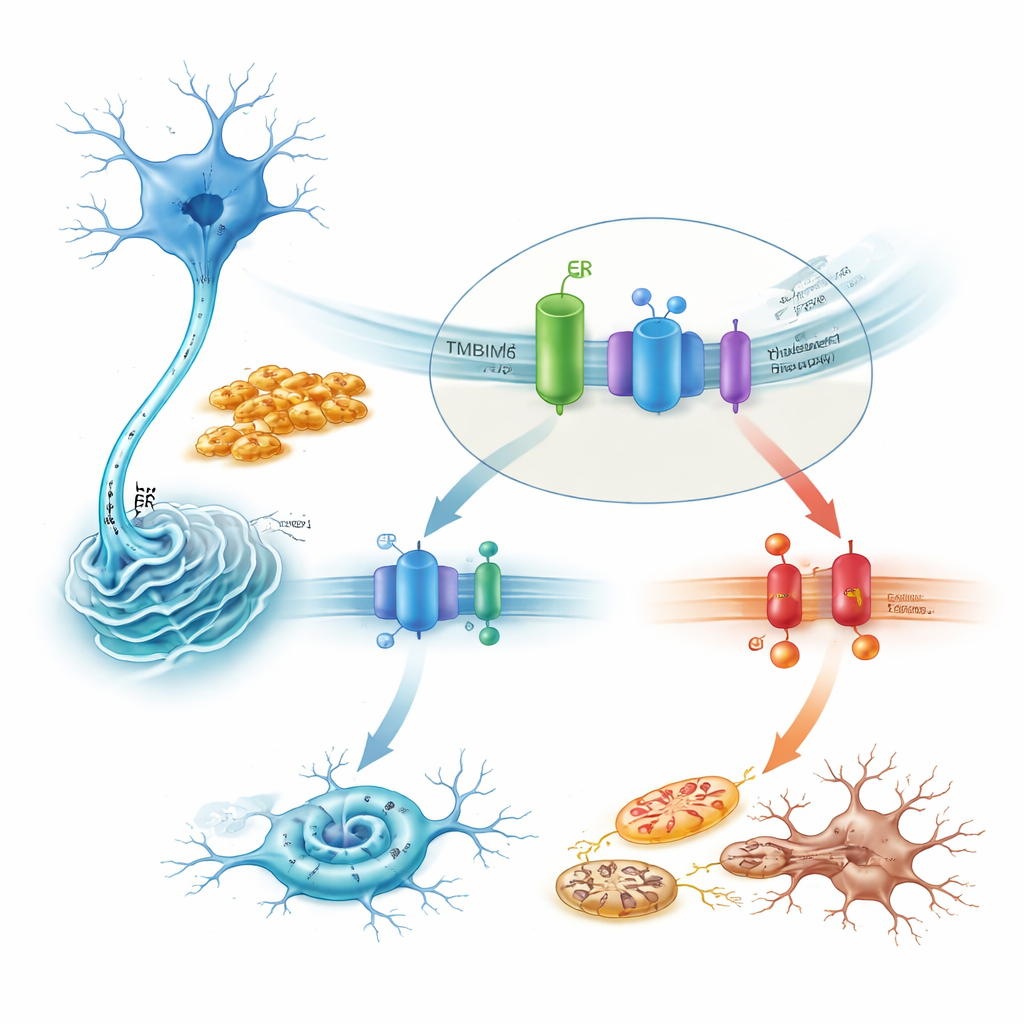
Comment TMBIM6 canalise une voie de stress mortelle
En s’attachant au mécanisme, l’étude montre que TMBIM6 s’associe physiquement à IRE1α dans des conditions de repos. Les fibrilles toxiques d’alpha-synucléine perturbent ce partenariat, libérant IRE1α pour qu’il s’active fortement. Dans les cellules déficientes en TMBIM6, cette activation devient exagérée, comme le montrent un épissage accru de l’ARNm de XBP1 et la dégradation d’une autre cible d’IRE1α. Bloquer IRE1α avec des médicaments ou en réduisant l’expression de son gène a en grande partie sauvé la surmortalité observée en l’absence de TMBIM6. En aval, la voie nocive passait par la kinase de stress JNK, la protéine pro-mort BAX et les caspases, formant une chaîne conduisant à l’apoptose. Inversement, la surexpression de TMBIM6 a atténué l’activité d’IRE1α, réduit ces signaux de mort et protégé les mitochondries, sans modifier la quantité d’agrégats d’alpha-synucléine — ce qui indique que TMBIM6 agit sur la gestion cellulaire du stress plutôt que sur les agrégats eux-mêmes.
Tester une approche de type thérapie génique chez la souris
Pour explorer le potentiel thérapeutique, les auteurs ont utilisé un adénovirus associé inoffensif (AAV) pour délivrer la TMBIM6 humaine directement dans la substance noire des souris. Deux semaines plus tard, ils ont lésé la voie dopaminergique avec une toxine standard du modèle de Parkinson, la 6-hydroxydopamine. Les souris témoins ayant reçu uniquement un gène marqueur ont présenté des troubles moteurs évidents : diminution de l’utilisation du membre antérieur affecté et équilibre détérioré sur une poutre. Les souris prétraitées par le virus portant TMBIM6 ont en revanche obtenu de bien meilleurs résultats, faisant moins d’impairs et accomplissant les tâches plus rapidement. Dans des neurones primaires en culture, le même vecteur AAV a atténué la mort cellulaire et l’activation des caspases déclenchées par des toxines ou des fibrilles d’alpha-synucléine, renforçant l’idée que l’augmentation des niveaux de TMBIM6 améliore la résilience neuronale.
Ce que cela pourrait signifier pour les traitements futurs
Ensemble, ces résultats présentent TMBIM6 comme un gardien des neurones dopaminergiques qui agit en maintenant sous contrôle un capteur de stress dangereux, IRE1α, et en empêchant une cascade d’événements menant à une défaillance mitochondriale et à l’apoptose. Aux premiers stades de la maladie, les cellules semblent augmenter TMBIM6 comme stratégie d’adaptation, mais dans les neurones les plus à risque le système finit par céder, faisant basculer l’équilibre vers le stress chronique et la mort cellulaire. Restaurer ou amplifier TMBIM6 — par des médicaments qui renforcent sa fonction ou par des thérapies géniques comme l’approche AAV testée ici — pourrait offrir un moyen de ralentir ou prévenir la perte neuronale dans la maladie de Parkinson, en complément des traitements actuels qui remplacent surtout la dopamine plutôt que de protéger les cellules qui la produisent.
Citation: Ahumada-Montalva, P., Muñoz-Carvajal, F., Bórquez-Macaya, S. et al. TMBIM6 enhances dopaminergic neuron survival by modulating the IRE1a pathway in Parkinson’s disease. Cell Death Dis 17, 385 (2026). https://doi.org/10.1038/s41419-025-08391-5
Mots-clés: Maladie de Parkinson, neurones dopaminergiques, stress du réticulum endoplasmique, voie IRE1α, neuroprotection