Clear Sky Science · pl
TMBIM6 zwiększa przeżywalność neuronów dopaminergicznych poprzez modulację szlaku IRE1α w chorobie Parkinsona
Dlaczego te badania mają znaczenie dla osób z chorobą Parkinsona
Choroba Parkinsona odbiera ludziom płynność ruchu, ponieważ kluczowe komórki mózgowe produkujące dopaminę stopniowo obumierają. To badanie ujawnia wewnętrzny białkowy mechanizm ochronny, zwany TMBIM6, który pomaga tym wrażliwym neuronów radzić sobie ze stresem wewnątrz ich aparatu do składania białek. Pokazując, że zwiększenie poziomu TMBIM6 może ratować neurony i poprawiać ruch u modeli zwierzęcych, praca wskazuje nowe podejście terapeutyczne wykraczające poza samo uzupełnianie dopaminy.
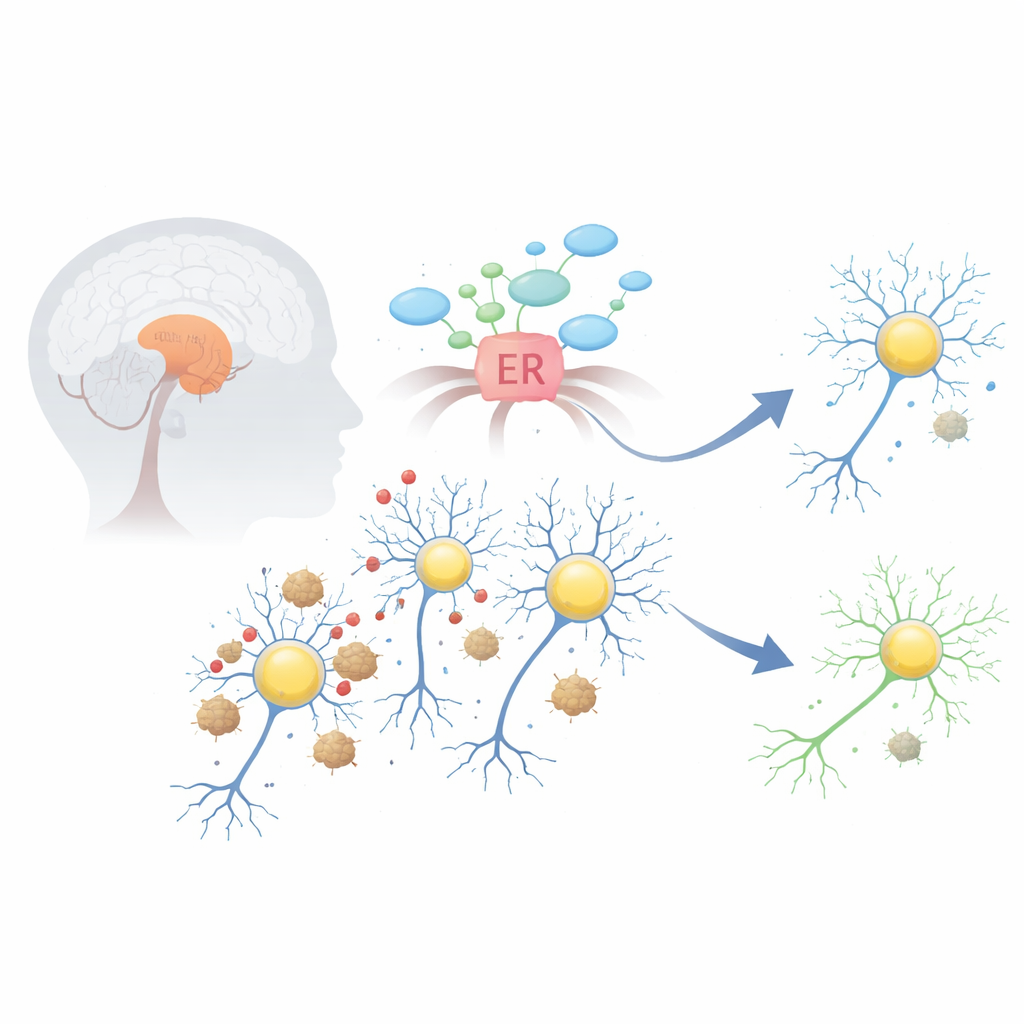
Problem wewnątrz komórek wytwarzających dopaminę
W chorobie Parkinsona białko alfa-synukleina może nieprawidłowo się fałdować i tworzyć lepkie agregaty, tworzące struktury znane jako ciała Lewy’ego. Te skupiska zaburzają kilka kluczowych układów w neuronach produkujących dopaminę w obszarze śródmózgowia zwanym istotą czarną. Jednym z najwcześniejszych i najbardziej szkodliwych skutków jest stres retikulum endoplazmatycznego — fabryki komórkowej odpowiedzialnej za fałdowanie i przetwarzanie białek. Gdy to przedział jest przeciążony, uruchamia awaryjny program zwany odpowiedzią na złożone białka (UPR), który na początku może pomagać, ale jeśli pozostanie aktywny zbyt długo, zaczyna skłaniać komórki do samozniszczenia.
Naturalna tarcza: przełącznik bezpieczeństwa TMBIM6
Białko TMBIM6 znajduje się w błonie retikulum endoplazmatycznego i zazwyczaj działa jak hamulec dla kluczowego czujnika stresu zwanego IRE1α. Badacze najpierw sprawdzili, czy TMBIM6 występuje w odpowiednim miejscu, by mieć znaczenie w chorobie Parkinsona. Korzystając z dużych baz danych ekspresji genów, stwierdzili, że TMBIM6 jest silnie eksprymowany w ludzkim śródmózgowiu oraz w innych rejonach bogatych w neurony dopaminergiczne. W hodowlach komórkowych i neuronach mysich wystawionych na toksyny przypominające Parkinsona — takie jak 6-hydroksydopamina, rotenon czy włókna alfa-synukleiny — poziomy TMBIM6 wzrastały już we wczesnym etapie, co sugeruje, że komórki uruchamiają ten czynnik jako szybką odpowiedź obronną na stres.
Kiedy ochrona zawodzi w najbardziej wrażliwych neuronach
Mimo tej pozornej obrony neurony dopaminergiczne nadal giną w chorobie Parkinsona. Aby zrozumieć dlaczego, zespół przeanalizował tkankę mózgową i dane jednoczkowej ekspresji genów od osób z Parkinsonem. Ogólnie białko TMBIM6 było wyższe w chorej tkance śródmózgowia niż w kontrolach, ale dokładniejsza analiza ujawniła kluczowy zwrot akcji: w podtypie neuronów dopaminergicznych uznawanych za najbardziej wrażliwe ekspresja TMBIM6 była w rzeczywistości niższa niż w neuronach bardziej odpornych. Jednocześnie zaburzeniu uległa zwykła ścisła koordynacja między TMBIM6 a innymi genami odpowiedzi na stres. Te obserwacje sugerują, że choć niektóre komórki zwiększają TMBIM6, neurony najbardziej potrzebujące ochrony mogą utracić ten przełącznik bezpieczeństwa, pozostając narażone na chroniczny stres i sygnały śmierci.
Dowód przyczynowości w komórkach i muszkach owocowych
Aby sprawdzić, czy TMBIM6 rzeczywiście wpływa na przeżywalność, badacze regulowali jego poziomy w wielu modelach laboratoryjnych. Gdy obniżono TMBIM6 w komórkach mysich przypominających neurony dopaminergiczne, komórki te stały się znacznie bardziej wrażliwe na toksyczne włókna alfa-synukleiny oraz na chemiczne toksyny naśladujące Parkinsona. Komórki wykazywały większą utratę funkcji mitochondriów, silniejszą aktywację enzymów egzekucyjnych, takich jak kaspaza-3, oraz większe wycieki zawartości komórkowej — cechy charakterystyczne zaprogramowanej śmierci komórki. Podobne wyniki zaobserwowano u muszek owocowych zaprojektowanych tak, by produkować mniej odpowiednika TMBIM6: traciły neurony dopaminergiczne w oku i mózgu oraz rozwijały gorsze problemy z ruchem, zwłaszcza po narażeniu na pestycyd rotenon.
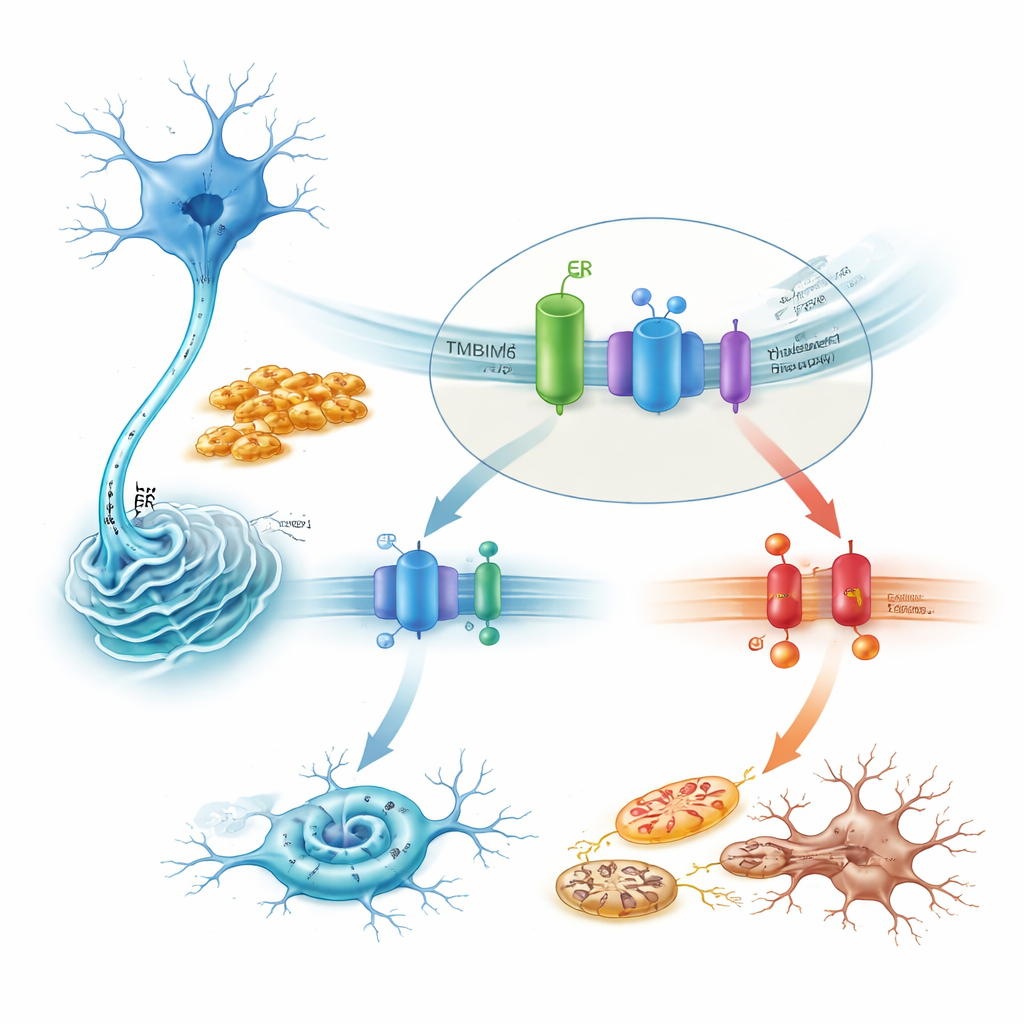
Jak TMBIM6 ujarzmia zabójczy szlak stresowy
Pogłębiając mechanizm, badanie pokazuje, że TMBIM6 fizycznie łączy się z IRE1α w warunkach spoczynkowych. Toksyczne włókna alfa-synukleiny przerywają to partnerstwo, uwalniając IRE1α do silnej aktywacji. W komórkach deficytowych w TMBIM6 ta aktywacja staje się przesadna, co ilustruje zwiększone składanie (splicing) mRNA dla XBP1 i degradacja innego celu IRE1α. Zablokowanie IRE1α za pomocą leków lub wyciszenie jego genu w dużej mierze ratowało zwiększoną śmierć komórek obserwowaną przy braku TMBIM6. W dół strumienia szkodliwy szlak przebiegał przez kinazę stresową JNK, prozapalne białko BAX i kaspazy, tworząc łańcuch prowadzący do apoptozy. Natomiast nadekspresja TMBIM6 tłumiła aktywność IRE1α, zmniejszała te sygnały śmierci i chroniła mitochondria, nie zmieniając stopnia agregacji alfa-synukleiny — co wskazuje, że TMBIM6 działa na mechanizmy radzenia sobie ze stresem komórkowym, a nie na same skupiska białkowe.
Test podejścia przypominającego terapię genową u myszy
Aby zbadać potencjał terapeutyczny, autorzy użyli bezpiecznego wirusa adeno-związanego (AAV) do dostarczenia ludzkiego TMBIM6 bezpośrednio do istoty czarnej myszy. Dwa tygodnie później uszkodzili szlak dopaminowy standardową toksyną Parkinsona, 6-hydroksydopaminą. Myszy kontrolne, które otrzymały jedynie marker, rozwinęły wyraźne zaburzenia motoryczne: ograniczone użycie kończyny przedniej po stronie uszkodzenia i gorszą równowagę na belce. Myszy uprzednio leczone wirusem niosącym TMBIM6 radziły sobie jednak istotnie lepiej, popełniając mniej błędów i szybciej wykonując zadania. W hodowlach neuronów pierwotnych ten sam konstruktu AAV łagodził śmierć komórek i aktywację kaspaz wywołaną przez toksyny lub włókna alfa-synukleiny, co wzmacnia argument, że zwiększenie poziomu TMBIM6 poprawia odporność neuronów.
Co to może znaczyć dla przyszłych terapii
W sumie te odkrycia przedstawiają TMBIM6 jako strażnika neuronów dopaminergicznych, który działa przez utrzymywanie niebezpiecznego czujnika stresu IRE1α pod kontrolą i zapobieganie kaskadzie prowadzącej do niewydolności mitochondriów i apoptozy. We wczesnej chorobie komórki wydają się podnosić poziom TMBIM6 jako strategię radzenia sobie, ale w najbardziej zagrożonych neuronach system ostatecznie zawodzi, przesuwając równowagę w stronę chronicznego stresu i śmierci komórek. Przywracanie lub wzmacnianie TMBIM6 — poprzez leki poprawiające jego funkcję lub terapie genowe podobne do podejścia AAV opisanego tutaj — mogłoby stanowić sposób na spowolnienie lub zapobieganie utracie neuronów w chorobie Parkinsona, uzupełniając obecne leczenie, które głównie zastępuje dopaminę zamiast chronić komórki ją produkujące.
Cytowanie: Ahumada-Montalva, P., Muñoz-Carvajal, F., Bórquez-Macaya, S. et al. TMBIM6 enhances dopaminergic neuron survival by modulating the IRE1a pathway in Parkinson’s disease. Cell Death Dis 17, 385 (2026). https://doi.org/10.1038/s41419-025-08391-5
Słowa kluczowe: choroba Parkinsona, neurony dopaminergiczne, stres retikulum endoplazmatycznego, szlak IRE1α, neuroprotekcja