Clear Sky Science · nl
TMBIM6 versterkt het overleven van dopaminerge neuronen door modulatie van de IRE1α-route bij de ziekte van Parkinson
Waarom dit onderzoek belangrijk is voor mensen met Parkinson
De ziekte van Parkinson berooft mensen van vloeiende bewegingen doordat cruciale hersencellen die dopamine produceren geleidelijk afsterven. Deze studie onthult een ingebouwd beschermend eiwit, TMBIM6, dat deze kwetsbare neuronen helpt omgaan met stress in hun eiwitvouwmachines. Doordat wordt aangetoond dat het verhogen van TMBIM6 neuronen kan doen overleven en bewegingen kan verbeteren in diermodellen, wijst dit werk op een nieuwe therapeutische invalshoek die verder gaat dan louter het vervangen van dopamine.
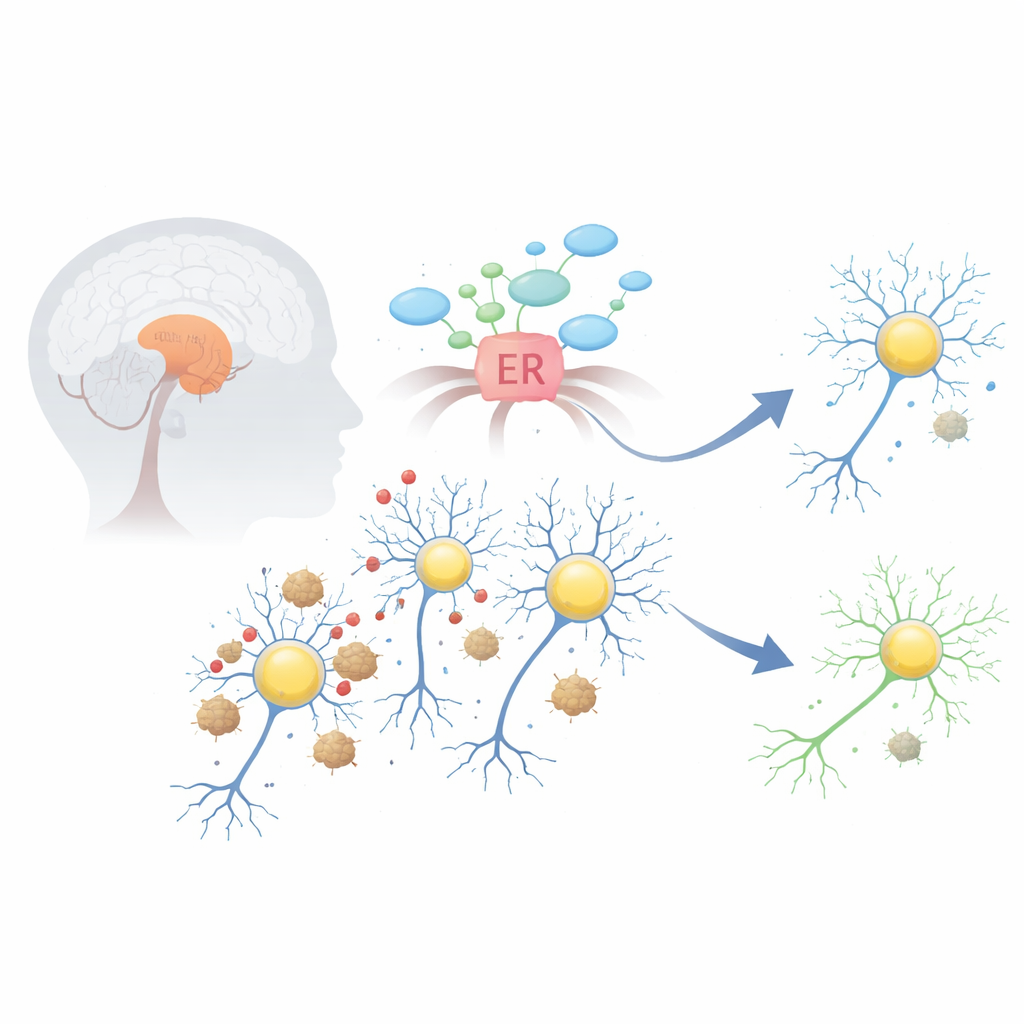
De problemen binnen dopamine-producerende hersencellen
Bij de ziekte van Parkinson kan een eiwit genaamd alfa-synucleïne verkeerd vouwen en samenklonteren tot plakkerige aggregaten, die Lewy-lichaampjes worden genoemd. Deze klonten verstoren verschillende vitale systemen binnen dopamine-producerende neuronen in een middenhersengebied dat de substantia nigra heet. Een van de vroegste en meest schadelijke effecten is stress in het endoplasmatisch reticulum, de celfabriek voor het vouwen en verwerken van eiwitten. Wanneer dit compartiment overweldigd raakt, schakelt het een noodprogramma in dat de unfolded protein response wordt genoemd, wat aanvankelijk kan helpen, maar bij langdurige activatie cellen naar zelfvernietiging kan duwen.
Een natuurlijke schild: de TMBIM6-veiligheidsschakelaar
Het eiwit TMBIM6 bevindt zich in het membraan van het endoplasmatisch reticulum en werkt normaal gesproken als een rem op een belangrijke stresssensor genaamd IRE1α. De onderzoekers vroegen eerst of TMBIM6 op de juiste plaats aanwezig is om van belang te zijn bij Parkinson. Met behulp van grote genexpressie-databases vonden ze dat TMBIM6 sterk tot expressie komt in het menselijke middenbrein en andere regio’s rijk aan dopaminerge neuronen. In gekweekte cellen en muisneuronen die werden blootgesteld aan Parkinson-achtige toxines — zoals 6-hydroxydopamine, rotenon of alfa-synucleïne-fibrillen — namen de TMBIM6-niveaus vroeg toe, wat suggereert dat cellen deze factor snel inschakelen als verdedigingsmechanisme tegen stress.
Wanneer bescherming faalt in kwetsbare neuronen
Ondanks deze schijnbare verdediging sterven dopaminerge neuronen toch bij de ziekte van Parkinson. Om te begrijpen waarom onderzocht het team hersenweefsel en single-cell genetische gegevens van mensen met Parkinson. Over het geheel genomen was het TMBIM6-eiwit hoger in ziek middenbreinweefsel dan in controles, maar een gedetailleerdere analyse liet een cruciale wending zien: binnen het subtype dopaminerge neuronen dat het meest kwetsbaar is, was de TMBIM6-expressie juist lager dan in meer resistente neuronen. Tegelijkertijd was de normale nauwe coördinatie tussen TMBIM6 en andere stress-responsgenen verstoord. Samen suggereren deze bevindingen dat hoewel sommige hersencellen TMBIM6 opvoeren, de neuronen die de meeste bescherming nodig hebben deze veiligheidsschakelaar kunnen verliezen, waardoor ze blootstaan aan chronische stress en signalen die tot celdood leiden.
Oorzakelijk bewijs in cellen en vliegen
Om te testen of TMBIM6 inderdaad de overleving beïnvloedt, reguleerden de onderzoekers de niveaus omhoog en omlaag in verschillende laboratoriummodellen. Toen ze TMBIM6 verlaagden in dopamine-achtige muiscellen, werden deze cellen veel gevoeliger voor toxische alfa-synucleïne-fibrillen en voor chemische toxines die Parkinson nabootsen. De cellen vertoonden grotere mitochondriale disfunctie, sterkere activatie van uitvoerende enzymen zoals caspase-3 en meer lekkage van celinhoud — kenmerken van geprogrammeerde celdood. Vergelijkbare resultaten werden gezien in fruitvliegen die minder van het TMBIM6-equivalent produceerden: ze verloren dopaminerge neuronen in oog en hersenen en ontwikkelden ernstiger bewegingsstoornissen, vooral bij blootstelling aan het pesticide rotenon.
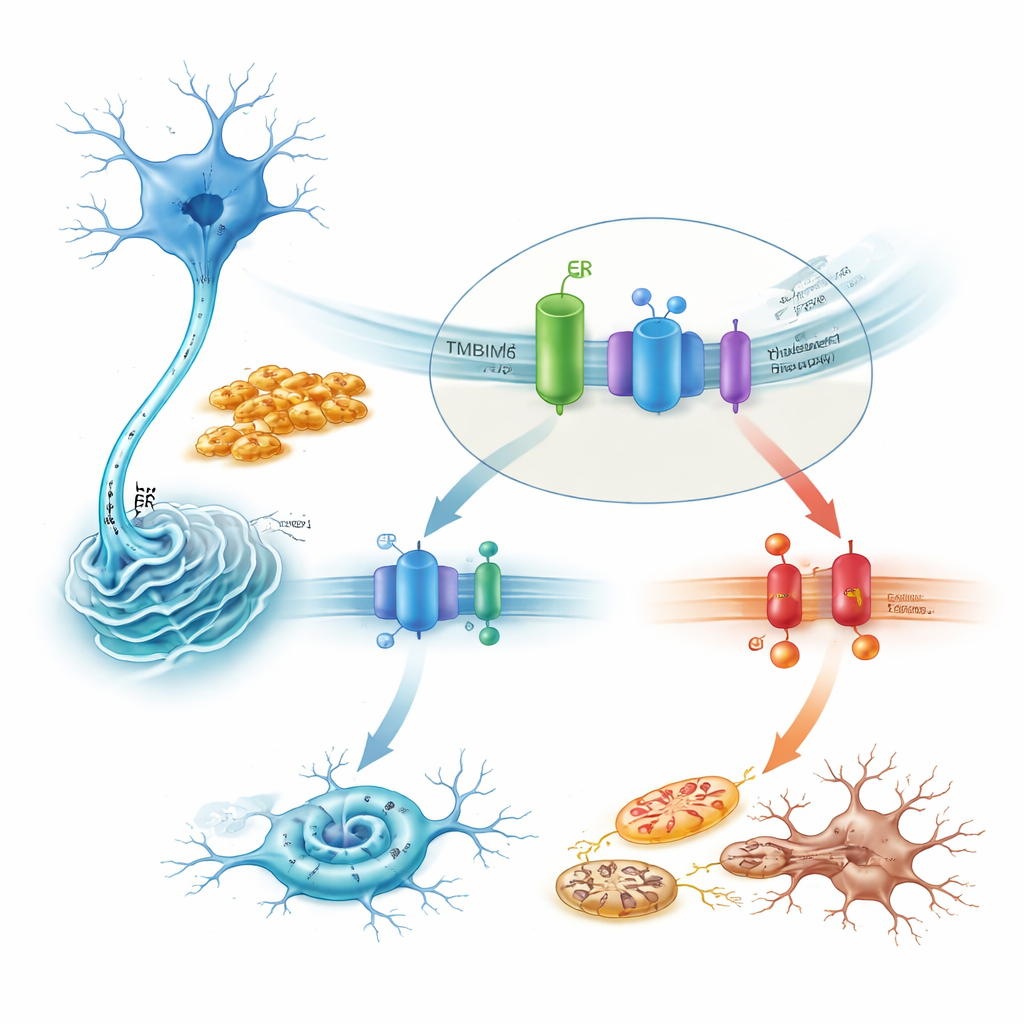
Hoe TMBIM6 een dodelijke stressroute temt
Bij nadere bestudering van het mechanisme laat de studie zien dat TMBIM6 onder rustcondities fysiek samenhangt met IRE1α. Toxische alfa-synucleïne-fibrillen verstoren deze interactie, waardoor IRE1α vrij komt om sterk te activeren. In TMBIM6-deficiënte cellen wordt die activatie overdreven, zoals blijkt uit toegenomen splicing van het mRNA voor XBP1 en degradatie van een ander IRE1α-doeleiwit. Het blokkeren van IRE1α met medicijnen of door het stilleggen van het gen herstelde grotendeels de verhoogde celdood die werd gezien bij gebrek aan TMBIM6. Stroomafwaarts liep de schadelijke route via de stresskinase JNK, het pro-dood eiwit BAX en caspases, en vormde zo een keten die apoptose aandrijft. Omgekeerd dempte overexpressie van TMBIM6 de IRE1α-activiteit, verminderde deze doodssignalen en beschermde de mitochondriën, zonder de mate van alfa-synucleïne-aggregatie te veranderen — wat aangeeft dat TMBIM6 werkt op de stressafhandeling van de cel en niet op de klonten zelf.
Een gentherapie-achtige aanpak testen bij muizen
Om het therapeutische potentieel te verkennen, gebruikten de auteurs een onschadelijk adeno-geassocieerd virus (AAV) om humane TMBIM6 rechtstreeks in de substantia nigra van muizen af te leveren. Twee weken later beschadigden ze de dopaminergische baan met een standaard Parkinson-toxine, 6-hydroxydopamine. Controlemuizen die alleen een marker-gen ontvingen ontwikkelden duidelijke motorische problemen: verminderd gebruik van de aangedane voorpoot en slechtere balans op een balktest. Muizen die vooraf werden behandeld met het virus dat TMBIM6 droeg, presteerden aanzienlijk beter, maakten minder misstappen en volbrachten de taken sneller. In primaire gecultiveerde neuronen verlichtte hetzelfde AAV-construct ook de celdood en caspase-activatie veroorzaakt door toxines of alfa-synucleïne-fibrillen, wat de stelling versterkt dat het verhogen van TMBIM6-nevels de veerkracht van neuronen vergroot.
Wat dit kan betekenen voor toekomstige behandelingen
Alles bij elkaar schetsen deze bevindingen TMBIM6 als een beschermer van dopaminerge neuronen die werkt door een gevaarlijke stresssensor, IRE1α, onder controle te houden en een cascade van gebeurtenissen die leiden tot mitochondriale uitval en apoptose te voorkomen. In een vroeg stadium van de ziekte lijken cellen TMBIM6 op te voeren als een copingstrategie, maar in de meest risicovolle neuronen faalt het systeem uiteindelijk, waardoor de balans doorslaat naar chronische stress en celdood. Het herstellen of versterken van TMBIM6 — via geneesmiddelen die de functie verbeteren of gentherapieën zoals de hier onderzochte AAV-benadering — zou een manier kunnen bieden om het verlies van neuronen bij de ziekte van Parkinson te vertragen of te voorkomen, als aanvulling op huidige behandelingen die vooral dopamine vervangen in plaats van de cellen die het maken te beschermen.
Bronvermelding: Ahumada-Montalva, P., Muñoz-Carvajal, F., Bórquez-Macaya, S. et al. TMBIM6 enhances dopaminergic neuron survival by modulating the IRE1a pathway in Parkinson’s disease. Cell Death Dis 17, 385 (2026). https://doi.org/10.1038/s41419-025-08391-5
Trefwoorden: Ziekte van Parkinson, dopaminerge neuronen, endoplasmatisch reticulum stress, IRE1α-route, neuroprotectie