Clear Sky Science · he
TMBIM6 משפר את שימור תאי העצב הדופמינרגיים על‑ידי ויסות מסלול IRE1α במחלת פרקינסון
למה המחקר הזה חשוב לאנשים עם פרקינסון
מחלת פרקינסון גוזלת מהאנשים את היכולת לזוז בצורה חלקה מכיוון שתאים מוחיים מרכזיים שמייצרים דופמין מתים בהדרגה. המחקר חושף חלבון מגן פנימי, הנקרא TMBIM6, שעוזר לנוירונים הרגישים האלה להתמודד עם מתח בתוך מנגנון קיפול החלבונים שלהם. בהדגמה שגידול ברמות TMBIM6 יכול לשמור על תאים חיים ולשפר תנועה במודלים חייתיים, העבודה מציעה אפיק טיפולי חדש שמעבר להחלפת דופמין בלבד.
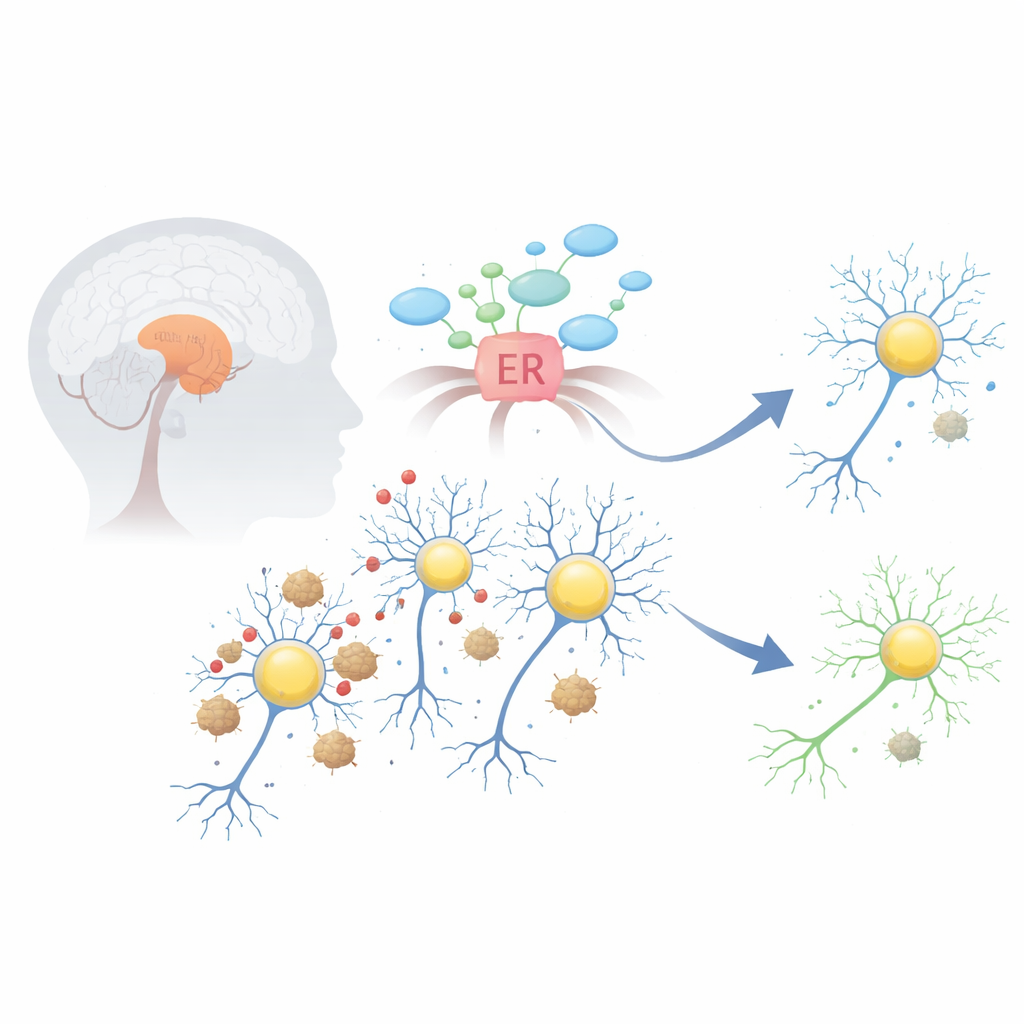
הבעיה בתוך התאים המייצרי דופמין
במחלת פרקינסון חלבון בשם אלפא‑סינוקלאין עלול לקפל בצורה לא תקינה ולהתגבש לצברי דביקים, הנקראים גופי לווי. הצבירים האלה משבשים כמה מערכות חיוניות בתוך נוירונים המייצרים דופמין באיזור שטוקה בשם הסובסטנטיה ניגרה. אחד ההשפעות המוקדמות וההרסניות ביותר הוא מתח ברטיקולום האנדופלזמי — המפעל בתא לקיפול ועיבוד חלבונים. כאשר המרחב הזה מוצף, הוא מפעיל תכנית חירום שנקראת תגובת החלבון הלא‑מקופל (UPR), שמתחילה כסיוע אך אם נשארת מופעלת זמן רב מדי יכולה לדחוף את התאים לכיוון השמדה עצמית.
מגן טבעי: מתג הבטיחות TMBIM6
החלבון TMBIM6 נמצא בממברנת הרטיקולום האנדופלזמי ופועל בדרך כלל כמעצור על חיישן מתח מרכזי הנקרא IRE1α. החוקרים שאלו תחילה האם TMBIM6 נמצא במקום הנכון כדי להיות משמעותי בפרקינסון. באמצעות מאגרי ביטוי גנים רחבים הם מצאו ש‑TMBIM6 מבוטא ברמות גבוהות במוח האמצעי האנושי ובאזורים אחרים עשירים לנוירוני דופמין. בתאים בתרבית וניורונים של עכברים שנחשפו לרעלים בדמיון לפרקינסון — כגון 6‑הידרוקסידופמין, רוטנון או סיבי אלפא‑סינוקלאין — רמות TMBIM6 עלו מוקדם, מה שמרמז שהתאים מפעילים את הגורם הזה כמענה מהיר להגנה מפני מתח.
כשמנגנון ההגנה נכשל בתאים הפגיעים
למרות ההגנה הנראית, נוירוני דופמין עדיין מתים במחלת פרקינסון. כדי להבין מדוע, הצוות בחן רקמות מוח ונתוני ריצוף תא‑יחיד מאנשים שחלו בפרקינסון. באופן כללי, רמות החלבון TMBIM6 היו גבוהות יותר ברקמת המוח האמצעי החולה לעומת ביקורות, אך מבט מפורט יותר חשף תפנית קריטית: בתוך תת‑סוג הניורונים הדופמינרגיים הידוע כפגיע ביותר, הביטוי של TMBIM6 היה נמוך יותר מזה שבתאים עמידים יותר. בו‑זמנית, התיאום הצפוף הרגיל בין TMBIM6 וגנים אחרים המשיבים למתח נשבר. יחד, הממצאים מציעים שבזמן שחלק מהתאים מגדילים את TMBIM6, הנוירונים שזקוקים להגנה יותר מכל עלולים לאבד את מתג הבטיחות הזה, מה שמשאיר אותם חשופים למתח כרוני ולאותות מוות.
הוכחת סיבה ותוצאה בתאים ובזבובי פרי
כדי לבדוק האם TMBIM6 באמת משפיע על הישרדות, החוקרים שיננו את רמותיו מעלה ומטה בכמה מודלים מעבדתיים. כאשר הם הקטינו את TMBIM6 בתאי עכבר דמויי דופמין, תאים אלה הפכו לרגישים הרבה יותר לסיבי אלפא‑סינוקלאין רעילים ולרעלים כימיים המדמים פרקינסון. בתאים נצפו פגיעה מורחבת בתפקוד המיטוכונדריה, הפעלה מוגברת של אנזימי ביצוע כמו קסקאז‑3 ודליפה רבה יותר של תכולת התא — מאפיינים של מוות תאי מתוכנת. תוצאות דומות הופיעו בזבובי פרי מהונדסים שמייצרים פחות המקבילה ל‑TMBIM6: הם איבדו נוירוני דופמין בעין ובמוח ופיתחו בעיות תנועה חמורות יותר, במיוחד בעת חשיפה לחומר ההדברה רוטנון.
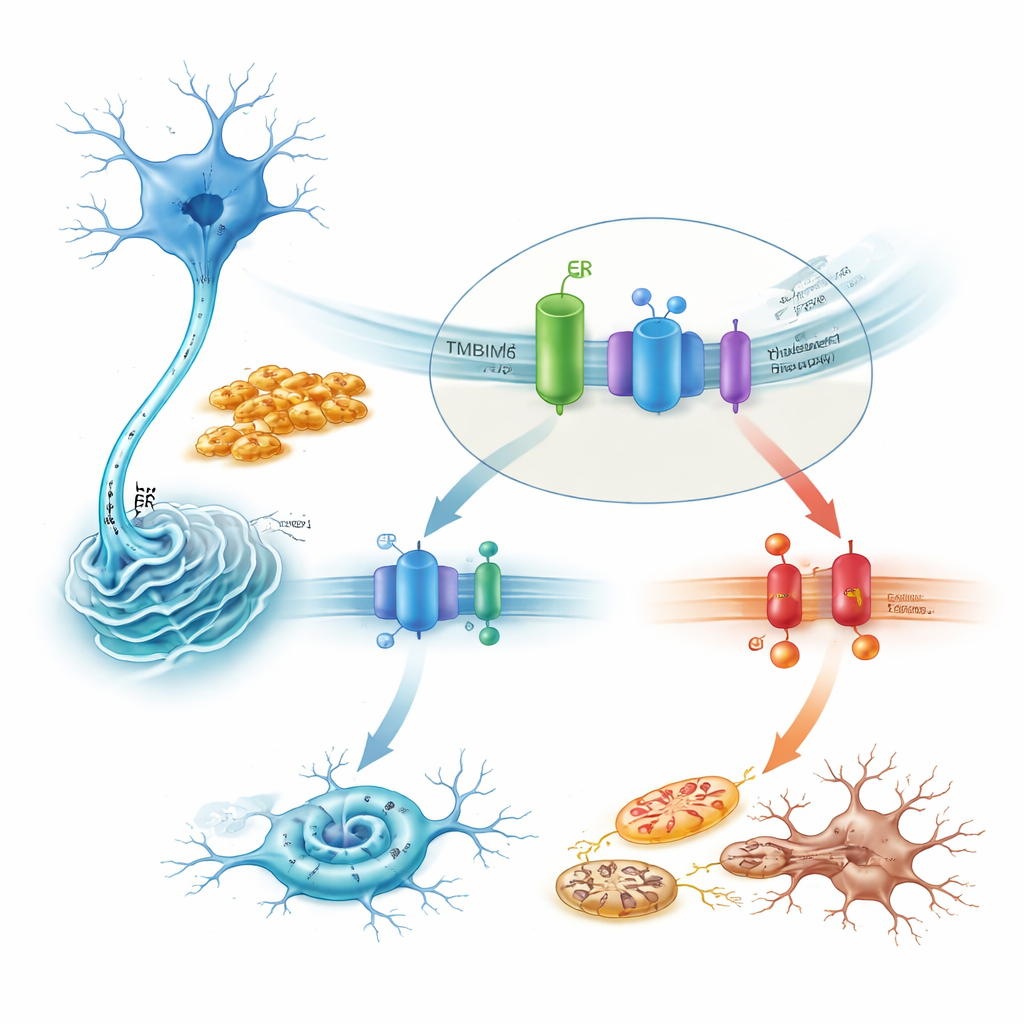
כיצד TMBIM6 מרסן מסלול מתח קטלני
בהתמקדות במנגנון, המחקר מראה ש‑TMBIM6 מקושר פיזית ל‑IRE1α במצב מנוחה. סיבי אלפא‑סינוקלאין רעילים משבשים את השותפות הזו ומשחררים את IRE1α להיפעל בחוזקה. בתאים חסרי TMBIM6 ההפעלה הזו מוגברת עוד יותר, כפי שנמדד על ידי עלייה בחיתוך (splicing) של ה‑mRNA של XBP1 ודעיכה של מטרה אחרת של IRE1α. חסימת IRE1α בתרופות או השתקה של הגן שלה הצילו במידה רבה את הגידול במוות התאי שנצפה בהיעדר TMBIM6. בהמשך, המסלול המזיק עבר דרך קינאז הלחץ JNK, חלבון הקידום־מוות BAX וקסקאזים, ויצר שרשרת שמניעה אפופטוזה. לעומת זאת, הבעה מופרזת של TMBIM6 הדכאה את פעילות IRE1α, הפחיתה את אותות המוות האלה והגנה על המיטוכונדריה, מבלי לשנות כמה אלפא‑סינוקלאין התגבש — דבר שמצביע ש‑TMBIM6 פועל על הטיפול הלחצני של התא ולא על הצברים עצמם.
ניסיון בגישה דמוית‑גנטית בעכברים
כדי לבחון פוטנציאל טיפולי, המחברים השתמשו בנגיף אדנואסוציאטיבי (AAV) בלתי מזיק כדי למסור את TMBIM6 האנושי ישירות לסובסטנטיה ניגרה של עכברים. שבועיים לאחר מכן הם פגעו במסלול הדופמינרגי עם רעל פרקינסון סטנדרטי, 6‑הידרוקסידופמין. עכברים ביקורת שקיבלו רק גן סימון פיתחו הפרעות מוטוריות ברורות: שימוש מוקטן בגפה הקדמית המושפעת ואיזון גרוע במבחן קרש. לעומת זאת, עכברים שקיבלו מראש את הנגיף הנושא את TMBIM6 הופיעו בצורה משמעותית טובה יותר, ביצעו פחות טעויות וסיימו את המשימות במהירות רבה יותר. בתרביות נוירונים ראשוניות, אותו מבנה AAV הקל על מוות תאי והפעלה של קסקאזים שנגרמו על ידי רעלים או סיבי אלפא‑סינוקלאין, וחיזק את הטענה שגידול ברמות TMBIM6 משפר את עמידות הנוירונים.
מה המשמעות האפשרית לטיפולים עתידיים
ביחד, הממצאים מציירים את TMBIM6 כשומר על נוירוני הדופמין הפועל בכך שמחזיק את חיישן המתח המסוכן IRE1α תחת שליטה ומונע מפל של אירועים המובילים לכישלון מיטוכונדריאלי ואפופטוזה. במחלה המוקדמת, נראה שהתאים מגדילים את TMBIM6 כאסטרטגיית התמודדות, אך בנוירונים הנמצאים בסיכון הגבוה ביותר המנגנון בסופו של דבר קורקב, ומשנה את המאזן לכיוון מתח כרוני ומוות תאי. שיקום או הגברה של TMBIM6 — באמצעות תרופות שמגבירות את תפקודו או טיפולי גנים כגון גישת ה‑AAV הנבדקה כאן — עשויים להציע דרך להאט או למנוע אובדן נוירונים בפרקינסון, ולשלים את הטיפולים הנוכחיים שמתמקדים בעיקר בהחלפת דופמין במקום בהגנה על התאים שמייצרים אותו.
ציטוט: Ahumada-Montalva, P., Muñoz-Carvajal, F., Bórquez-Macaya, S. et al. TMBIM6 enhances dopaminergic neuron survival by modulating the IRE1a pathway in Parkinson’s disease. Cell Death Dis 17, 385 (2026). https://doi.org/10.1038/s41419-025-08391-5
מילות מפתח: מחלת פרקינסון, תאי עצב דופמינרגיים, מתח ברטיקולום האנדופלזמי, מסלול IRE1α, הגנה נוירונית