Clear Sky Science · it
TMBIM6 migliora la sopravvivenza dei neuroni dopaminergici modulando la via IRE1α nella malattia di Parkinson
Perché questa ricerca è importante per le persone con Parkinson
La malattia di Parkinson priva le persone di movimenti fluidi perché cellule cerebrali chiave che producono dopamina muoiono lentamente. Questo studio rivela una proteina protettiva intrinseca, chiamata TMBIM6, che aiuta questi neuroni vulnerabili a gestire lo stress all’interno della loro macchina per il ripiegamento delle proteine. Dimostrando come l’aumento di TMBIM6 possa mantenere i neuroni in vita e migliorare il movimento in modelli animali, il lavoro indica una nuova direzione terapeutica oltre alla semplice sostituzione della dopamina.
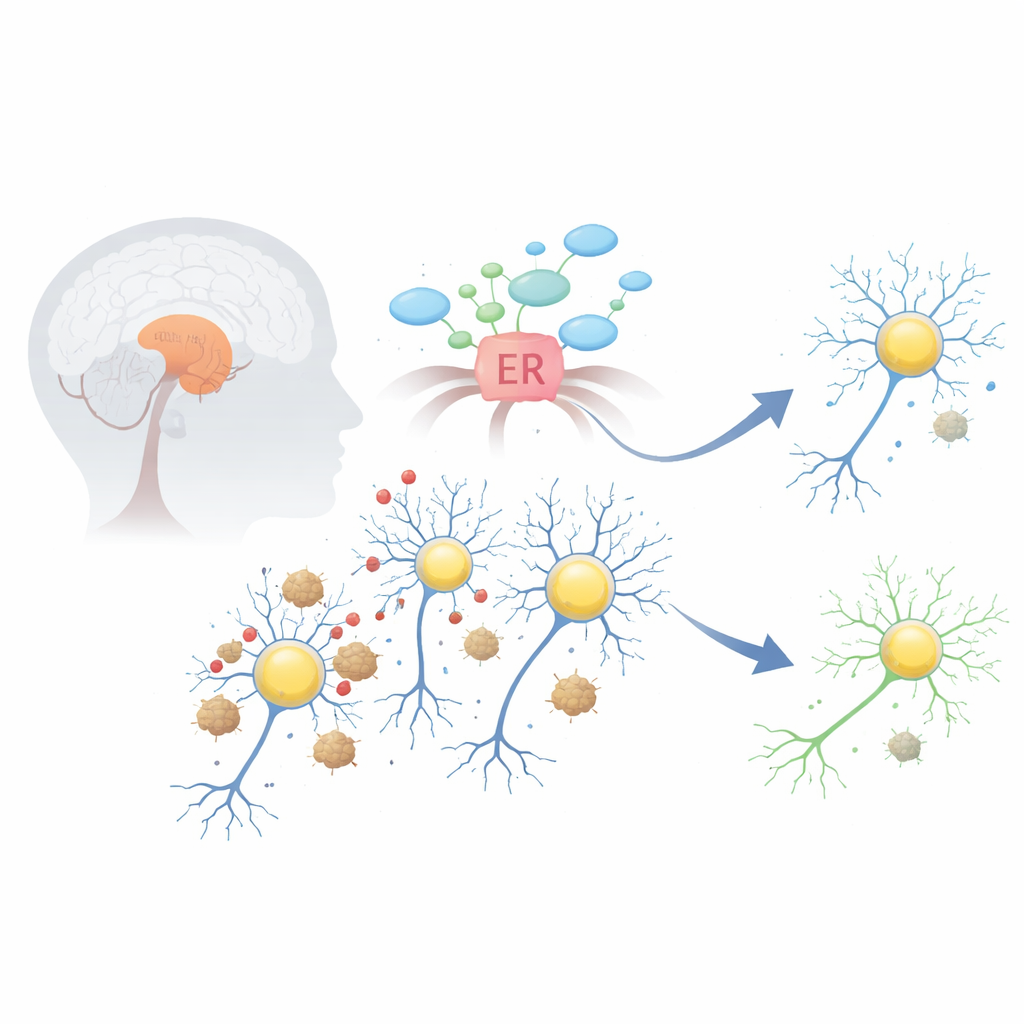
I problemi all’interno delle cellule che producono dopamina
Nella malattia di Parkinson, una proteina chiamata alfa-sinucleina può malripiegarsi e aggregarsi in ammassi appiccicosi, formando strutture note come corpi di Lewy. Questi aggregati disturbano diversi sistemi vitali all’interno dei neuroni produttori di dopamina in una regione del mesencefalo chiamata substantia nigra. Uno degli effetti precoci e più dannosi è lo stress del reticolo endoplasmatico, la «fabbrica» cellulare per il ripiegamento e il processamento delle proteine. Quando questo compartimento è sopraffatto, attiva un programma d’emergenza chiamato risposta allo stress da proteine malripiegate (unfolded protein response), che può inizialmente aiutare ma, se rimane attivo troppo a lungo, spinge le cellule verso l’autodistruzione.
Uno scudo naturale: l’interruttore di sicurezza TMBIM6
La proteina TMBIM6 si trova nella membrana del reticolo endoplasmatico e normalmente agisce come freno su un sensore chiave dello stress chiamato IRE1α. I ricercatori hanno prima verificato se TMBIM6 fosse presente nel luogo giusto per avere rilevanza nel Parkinson. Utilizzando ampi database di espressione genica, hanno scoperto che TMBIM6 è altamente espresso nel mesencefalo umano e in altre regioni ricche di neuroni dopaminergici. In colture cellulari e neuroni murini esposti a tossine che imitano il Parkinson — come 6-idrossidopamina, rotenone o fibrille di alfa-sinucleina — i livelli di TMBIM6 aumentavano precocemente, suggerendo che le cellule attivano questo fattore come risposta difensiva rapida allo stress.
Quando la protezione fallisce nei neuroni vulnerabili
Nonostante questa apparente difesa, i neuroni dopaminergici continuano a morire nella malattia di Parkinson. Per capire il motivo, il gruppo ha esaminato tessuto cerebrale e dati genetici a singola cellula di persone affette da Parkinson. Complessivamente, la proteina TMBIM6 era più alta nel tessuto mesencefalico malato rispetto ai controlli, ma un’analisi più dettagliata ha rivelato un colpo di scena cruciale: nel sottotipo di neuroni dopaminergici noto per essere più vulnerabile, l’espressione di TMBIM6 era in realtà più bassa rispetto ai neuroni più resistenti. Allo stesso tempo, la coordinazione solita tra TMBIM6 e altri geni della risposta allo stress risultava disturbata. Questi risultati suggeriscono che, mentre alcune cellule aumentano TMBIM6, i neuroni che più necessitano protezione possono perdere questo interruttore di sicurezza, lasciandoli esposti a stress cronico e segnali di morte.
Dimostrare causa ed effetto in cellule e moscerini
Per verificare se TMBIM6 influenzi davvero la sopravvivenza, i ricercatori hanno modulato i suoi livelli in vari modelli di laboratorio. Quando hanno ridotto TMBIM6 in cellule murine simili a neuroni dopaminergici, queste cellule sono diventate molto più sensibili alle fibrille tossiche di alfa-sinucleina e alle tossine chimiche che imitano il Parkinson. Le cellule mostravano una maggiore perdita della funzione mitocondriale, una maggiore attivazione di enzimi esecutori come la caspasi-3 e più perdita di contenuti cellulari — segni distintivi della morte cellulare programmata. Risultati simili sono comparsi nei moscerini della frutta ingegnerizzati per esprimere meno l’equivalente di TMBIM6: persero neuroni dopaminergici nell’occhio e nel cervello e svilupparono problemi di movimento peggiori, soprattutto quando esposti al pesticida rotenone.
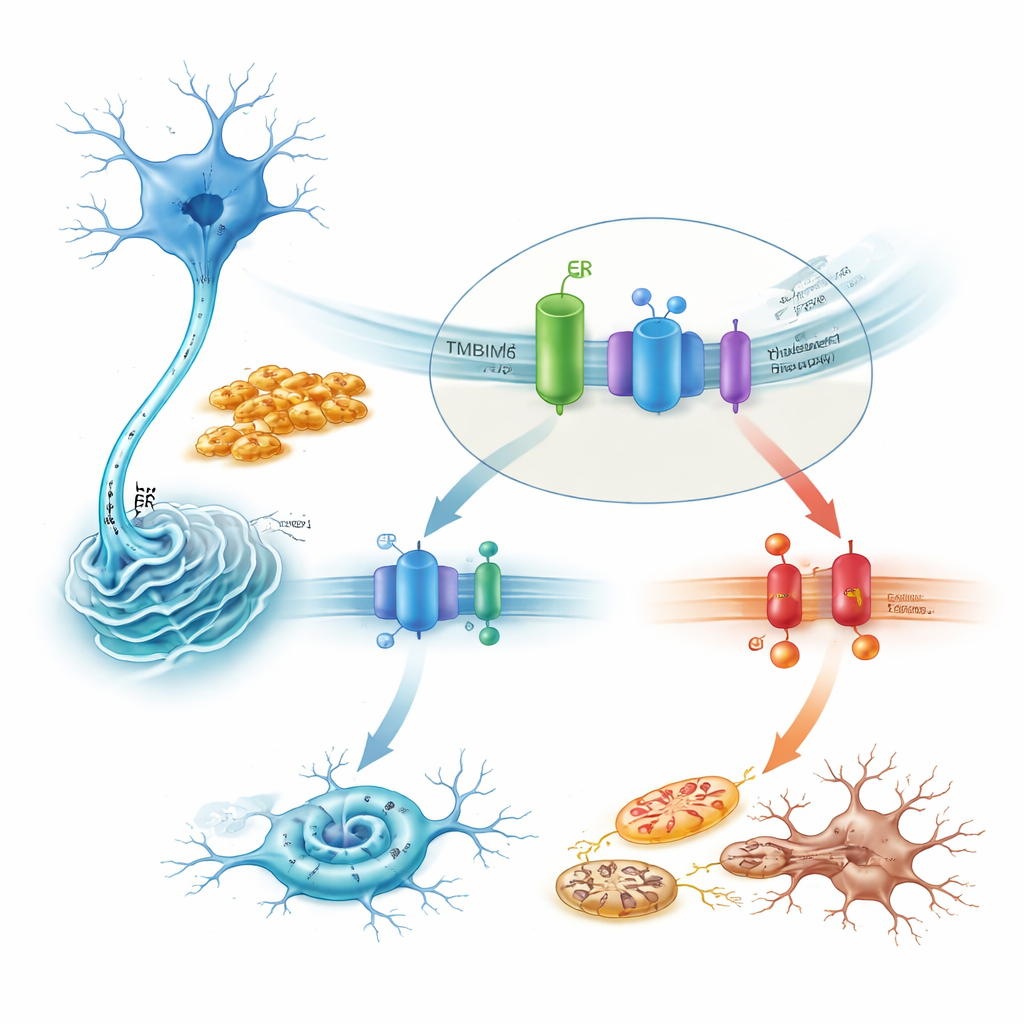
Come TMBIM6 controlla una via di stress letale
Approfondendo il meccanismo, lo studio mostra che TMBIM6 si associa fisicamente con IRE1α in condizioni di riposo. Le fibrille tossiche di alfa-sinucleina disturbano questa associazione, liberando IRE1α per un’attivazione intensa. Nelle cellule carenti di TMBIM6, questa attivazione diventa esagerata, come dimostrato dall’aumentato splicing dell’RNA messaggero per XBP1 e dal decadimento di un altro bersaglio di IRE1α. Bloccare IRE1α con farmaci o silenziandone il gene ha in gran parte salvato la maggiore morte cellulare osservata quando TMBIM6 mancava. A valle, la via dannosa passava attraverso la chinasi di stress JNK, la proteina pro-morte BAX e le caspasi, formando una catena che guida l’apoptosi. Al contrario, l’overespressione di TMBIM6 attenuava l’attività di IRE1α, riduceva questi segnali di morte e proteggeva i mitocondri, senza modificare la quantità di aggregazione dell’alfa-sinucleina — indicando che TMBIM6 agisce sulla gestione dello stress cellulare piuttosto che sugli aggregati stessi.
Testare un approccio simile alla terapia genica nei topi
Per esplorare il potenziale terapeutico, gli autori hanno usato un virus adeno-associato innocuo (AAV) per veicolare la TMBIM6 umana direttamente nella substantia nigra dei topi. Due settimane dopo, hanno lesionato la via dopaminergica con una tossina standard per il Parkinson, la 6-idrossidopamina. I topi di controllo che avevano ricevuto solo un gene marcatore hanno sviluppato chiari problemi motori: ridotto uso dell’arto anteriore colpito e peggior equilibrio su una prova con una trave. I topi pretrattati con il virus contenente TMBIM6, tuttavia, hanno mostrato prestazioni significativamente migliori, commettendo meno passi falsi e completando i compiti più rapidamente. In neuroni primari coltivati, lo stesso costrutto AAV ha attenuato la morte cellulare e l’attivazione delle caspasi indotte da tossine o fibrille di alfa-sinucleina, rafforzando l’ipotesi che aumentare i livelli di TMBIM6 migliori la resilienza neuronale.
Cosa potrebbe significare per i trattamenti futuri
Nel complesso, questi risultati descrivono TMBIM6 come un guardiano dei neuroni dopaminergici che opera mantenendo sotto controllo un pericoloso sensore di stress, IRE1α, e prevenendo una cascata di eventi che porta al fallimento mitocondriale e all’apoptosi. Nelle fasi iniziali della malattia, le cellule sembrano aumentare TMBIM6 come strategia di adattamento, ma nei neuroni più a rischio il sistema alla fine cede, facendo pendere l’equilibrio verso stress cronico e morte cellulare. Ripristinare o amplificare TMBIM6 — attraverso farmaci che ne potenzino la funzione o terapie geniche come l’approccio AAV testato qui — potrebbe offrire un modo per rallentare o prevenire la perdita neuronale nella malattia di Parkinson, complementando i trattamenti attuali che sostituiscono principalmente la dopamina piuttosto che proteggere le cellule che la producono.
Citazione: Ahumada-Montalva, P., Muñoz-Carvajal, F., Bórquez-Macaya, S. et al. TMBIM6 enhances dopaminergic neuron survival by modulating the IRE1a pathway in Parkinson’s disease. Cell Death Dis 17, 385 (2026). https://doi.org/10.1038/s41419-025-08391-5
Parole chiave: Malattia di Parkinson, neuroni dopaminergici, stress del reticolo endoplasmatico, via IRE1α, neuroprotezione