Clear Sky Science · ru
TMBIM6 улучшает выживаемость дофаминергических нейронов, модулируя путь IRE1α при болезни Паркинсона
Почему это исследование важно для людей с болезнью Паркинсона
Болезнь Паркинсона лишает людей плавности движений, потому что ключевые клетки головного мозга, вырабатывающие дофамин, постепенно гибнут. В этом исследовании выявлен встроенный защитный белок TMBIM6, который помогает уязвимым нейронам справляться со стрессом внутри их белкового аппарата сворачивания. Показав, что усиление TMBIM6 может сохранять нейроны и улучшать подвижность в моделях животных, работа указывает на новую терапевтическую стратегию, выходящую за рамки простой замены дофамина.
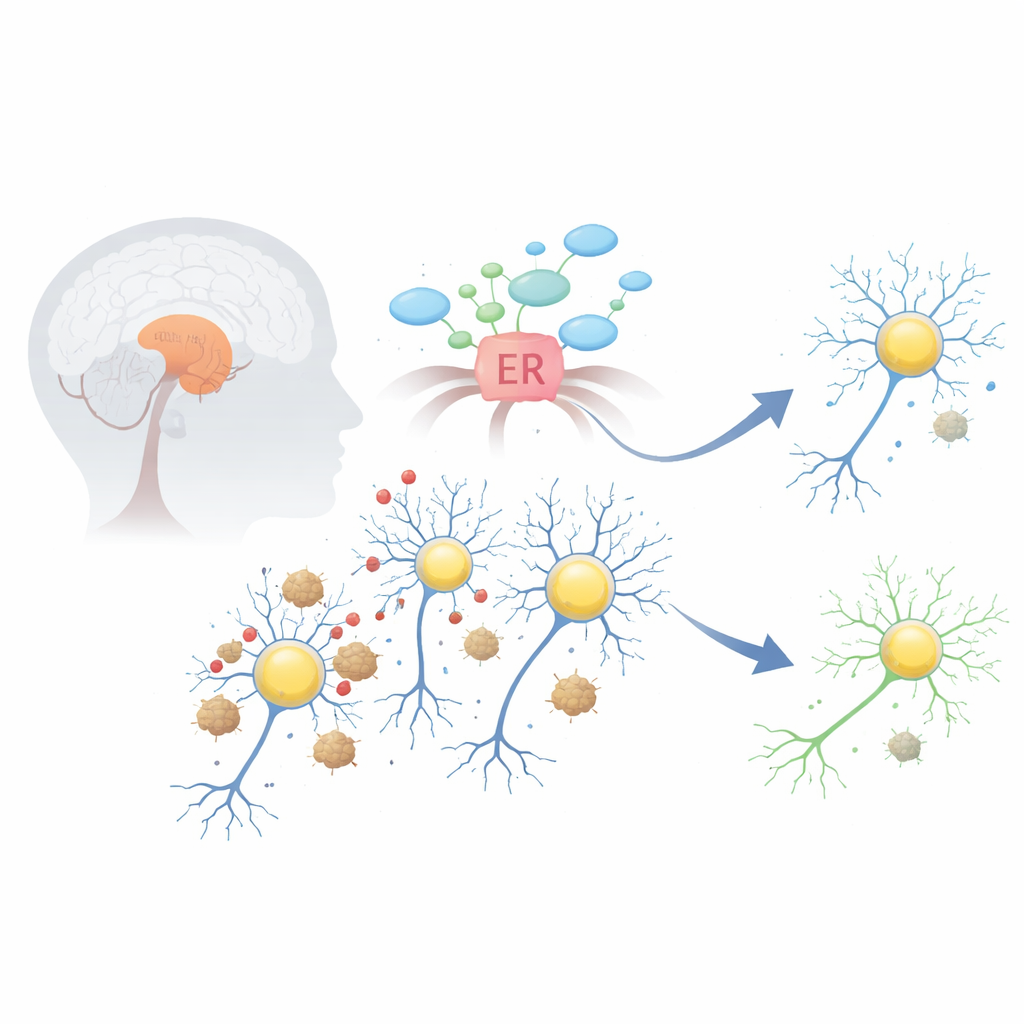
Проблема внутри дофамин-продуцирующих клеток мозга
При болезни Паркинсона белок альфа-синуклеин может неправильно сворачиваться и слипаться в вязкие агрегаты, образующие структуры, известные как тельца Леви. Эти сгустки нарушают несколько жизненно важных систем внутри дофаминергических нейронов в области средней части мозга, называемой субстанцией нигра. Одним из ранних и самых разрушительных эффектов является стресс эндоплазматического ретикулума — «фабрики» клетки по сворачиванию и обработке белков. Когда этот компартмент перегружен, он включает аварийную программу, называемую реакцией на незавернутые белки, которая сначала может помогать, но при длительной активации начинает толкать клетку к самоуничтожению.
Естественный щит: переключатель безопасности TMBIM6
Белок TMBIM6 располагается в мембране эндоплазматического ретикулума и обычно действует как тормоз для ключевого датчика стресса IRE1α. Исследователи сначала проверили, присутствует ли TMBIM6 в тех местах, где это имеет значение при болезни Паркинсона. Используя крупные базы данных экспрессии генов, они обнаружили, что TMBIM6 сильно экспрессируется в человеческом среднем мозге и других областях, богатых дофаминергическими нейронами. В культурах клеток и нейронах мышей, подвергнутых токсинам, имитирующим болезнь Паркинсона — таким как 6-гидроксидопамин, ротенон или фибриллы альфа-синуклеина — уровни TMBIM6 повышались на ранней стадии, что указывает на то, что клетки включают этот фактор как быстрый защитный ответ на стресс.
Когда защита дает сбой в уязвимых нейронах
Несмотря на эту очевидную защиту, дофаминергические нейроны по-прежнему гибнут при болезни Паркинсона. Чтобы понять, почему, команда изучила мозговую ткань и данные одиночноклеточной транскриптомики у людей с Паркинсоном. В целом белок TMBIM6 был выше в пораженной ткани среднего мозга по сравнению с контрольной, но более детальный анализ выявил важный нюанс: в том самом подтипе дофаминергических нейронов, который считается наиболее уязвимым, экспрессия TMBIM6 была фактически ниже, чем в более устойчивых нейронах. Одновременно была нарушена обычная тесная координация между TMBIM6 и другими генами, реагирующими на стресс. В совокупности эти наблюдения позволяют предположить, что хотя некоторые клетки наращивают TMBIM6, нейроны, которые больше всего нуждаются в защите, могут терять этот переключатель безопасности, оставшись подверженными хроническому стрессу и сигналам смерти.
Доказательство причины и следствия в клетках и дрозофилах
Чтобы проверить, действительно ли TMBIM6 влияет на выживаемость, исследователи варьировали его уровни в нескольких лабораторных моделях. При снижении TMBIM6 в дофаминоподобных клетках мыши эти клетки становились значительно более чувствительными к токсичным фибриллам альфа-синуклеина и к химическим токсинам, имитирующим Паркинсон. Клетки проявляли большую потерю функции митохондрий, повышенную активацию «исполнительных» ферментов, таких как каспаза-3, и большее протекание клеточных содержимых — признаки программируемой клеточной смерти. Похожие результаты наблюдались у плодовых мушек, генетически модифицированных так, чтобы синтезировать меньше аналога TMBIM6: у них гибли дофаминовые нейроны в глазу и мозге и развивались более выраженные нарушения движений, особенно при воздействии пестицида ротенона.
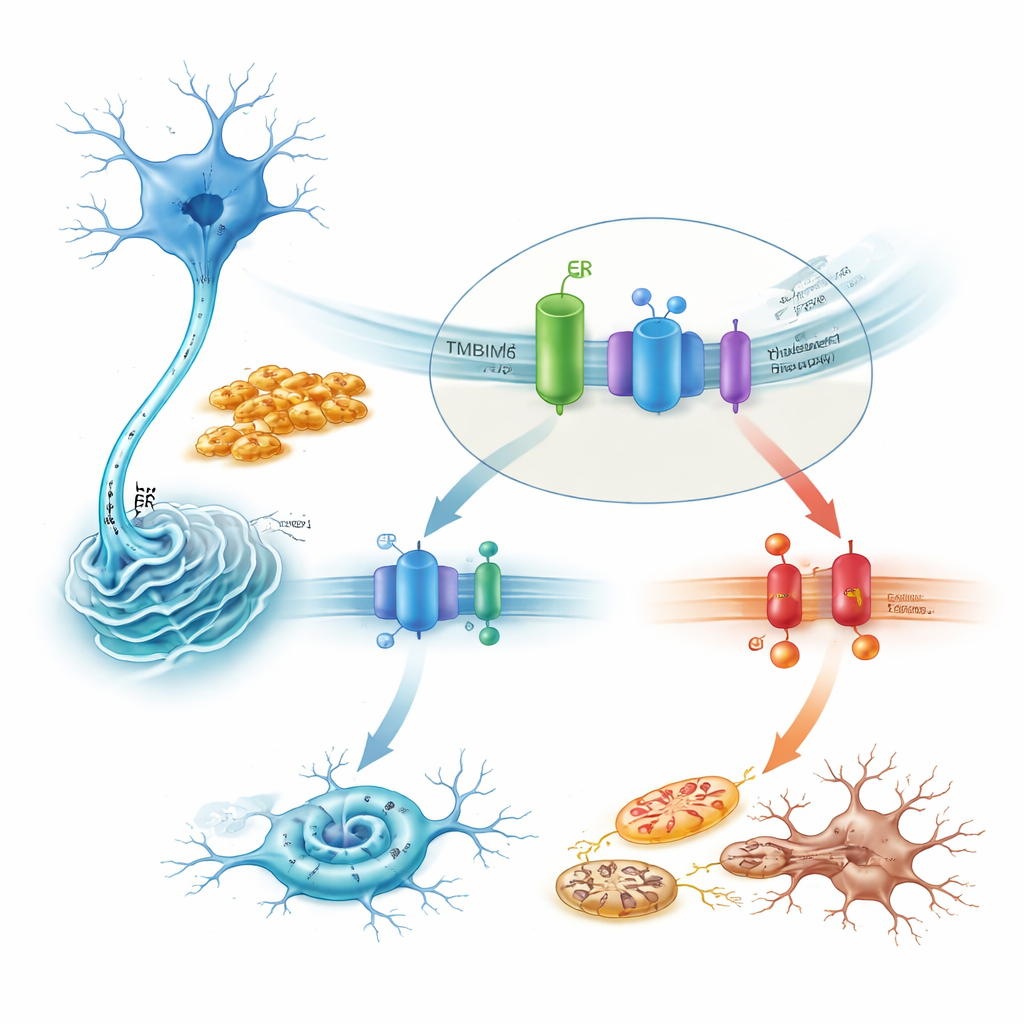
Как TMBIM6 укрощает смертоносный путь стресса
Углубляясь в механизм, исследование показывает, что TMBIM6 физически связывается с IRE1α в покое. Токсичные фибриллы альфа-синуклеина разрушают это партнерство, освобождая IRE1α для сильной активации. В клетках, лишенных TMBIM6, эта активация усиливается, о чем свидетельствует повышенное сплайсинг-событие матричной РНК для XBP1 и распад другой мишени IRE1α. Блокирование IRE1α препаратами или с помощью заглушения гена в основном спасало усиленную гибель клеток, наблюдавшуюся при отсутствии TMBIM6. Далее вредоносный путь проходил через стресс-киназу JNK, протеин, способствующий гибели BAX, и каспазы, образуя цепочку, приводящую к апоптозу. Напротив, сверхэкспрессия TMBIM6 подавляла активность IRE1α, уменьшала эти сигналы гибели и защищала митохондрии, не изменяя степени агрегации альфа-синуклеина — что указывает на то, что TMBIM6 действует на управление клеточным стрессом, а не на сами агрегаты.
Испытание подхода, похожего на генная терапию, у мышей
Чтобы оценить терапевтический потенциал, авторы использовали безопасный адено-ассоциированный вирус (AAV) для доставки человеческого TMBIM6 непосредственно в субстанцию нигра мышей. Через две недели они повредили дофаминовый путь стандартным токсином при Паркинсоне, 6-гидроксидопамином. Контрольные мыши, получившие только ген-маркер, проявили выраженные моторные нарушения: уменьшение использования пораженной передней конечности и худшую равновесие на бревенчатом тесте. Мыши, предварительно получившие вирус с TMBIM6, однако, выступали значительно лучше: делали меньше промахов и быстрее выполняли задания. В культуре первичных нейронов тот же AAV-конструкт ослаблял гибель клеток и активацию каспаз, вызванные токсинами или фибриллами альфа-синуклеина, что усиливает доказательства того, что повышение уровней TMBIM6 повышает устойчивость нейронов.
Что это может означать для будущих методов лечения
Вместе эти результаты рисуют TMBIM6 как стража дофаминергических нейронов, который действует, удерживая опасный датчик стресса IRE1α под контролем и предотвращая каскад событий, ведущих к сбою митохондрий и апоптозу. На ранних стадиях болезни клетки, по-видимому, повышают TMBIM6 как стратегию выживания, но в наиболее уязвимых нейронах система в конечном итоге дает сбой, сдвигая равновесие в сторону хронического стресса и гибели клеток. Восстановление или усиление TMBIM6 — с помощью препаратов, усиливающих его функцию, или генотерапии, подобной испытанному здесь подходу с AAV — может предложить способ замедлить или предотвратить потерю нейронов при болезни Паркинсона, дополняя существующие методы лечения, которые в основном заменяют дофамин, а не защищают клетки, его продуцирующие.
Цитирование: Ahumada-Montalva, P., Muñoz-Carvajal, F., Bórquez-Macaya, S. et al. TMBIM6 enhances dopaminergic neuron survival by modulating the IRE1a pathway in Parkinson’s disease. Cell Death Dis 17, 385 (2026). https://doi.org/10.1038/s41419-025-08391-5
Ключевые слова: болезнь Паркинсона, дофаминергические нейроны, стресс эндоплазматического ретикулума, путь IRE1α, нейропротекция