Clear Sky Science · ja
TMBIM6はパーキンソン病においてIRE1α経路を調節してドーパミン作動性ニューロンの生存を促進する
なぜこの研究がパーキンソン病の患者にとって重要か
パーキンソン病は、ドーパミンを産生する重要な脳細胞が徐々に失われることで滑らかな運動を奪います。本研究は、TMBIM6と呼ばれる内在的な保護タンパク質が、これら脆弱なニューロンがタンパク質折りたたみ装置内のストレスに対処するのを助けることを明らかにしました。TMBIM6を増強することでニューロンの生存が保たれ、動作が改善する動物モデルでの結果は、単にドーパミンを補うだけではない新たな治療の方向性を示唆します。
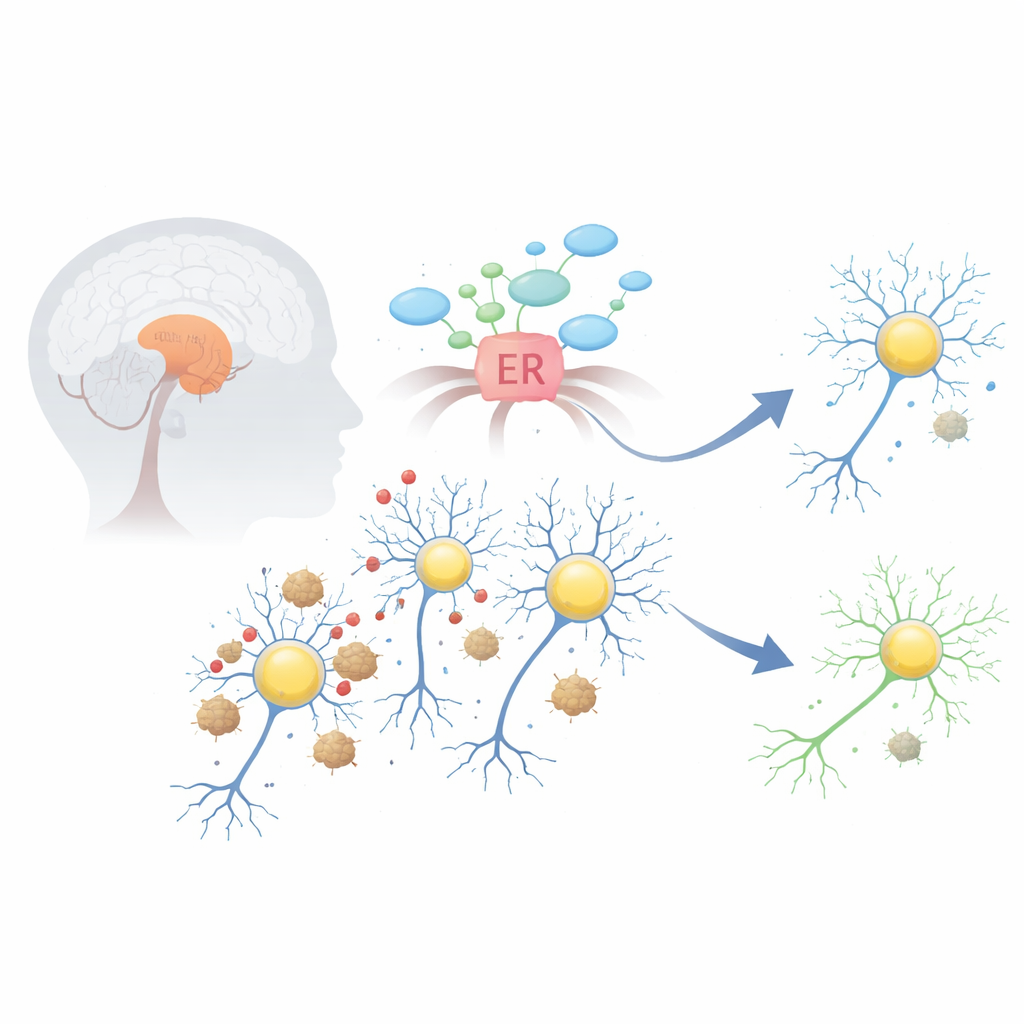
ドーパミン産生ニューロンの内部で起きている問題
パーキンソン病では、α-シヌクレインというタンパク質が誤った折りたたみを起こし、粘着性の凝集体を形成してレビー小体として知られる構造を作ります。これらの凝集体は中脳の黒質と呼ばれるドーパミン産生ニューロンに富む領域で、いくつかの重要な機能系を攪乱します。最も早期で有害な影響の一つは、小胞体(細胞のタンパク質折りたたみと処理の工場)におけるストレスです。このコンパートメントが過負荷になると、当初は助けとなるものの、長時間持続すると細胞を自己破壊へと追いやる「アンフォールデッド・プロテイン応答(UPR)」という緊急プログラムが作動します。
自然の盾:TMBIM6という安全装置
TMBIM6は小胞体膜に位置し、ストレスセンサーであるIRE1αの働きを通常は抑えるブレーキとして作用します。研究者らはまず、TMBIM6がパーキンソン病で重要な場所に存在するかを問いました。大規模な遺伝子発現データベースを用いると、TMBIM6はヒトの中脳やドーパミン神経が多い他の領域で高く発現していることが分かりました。培養細胞や6-ヒドロキシドーパミン、ロテノン、あるいはα-シヌクレイン線維のようなパーキンソン様毒素に曝露したマウスニューロンでは、TMBIM6レベルが早期に上昇し、細胞がストレスへの迅速な防御反応としてこの因子を活性化することを示唆しました。
脆弱なニューロンで防御が破綻するとき
これらの防御があるにもかかわらず、ドーパミンニューロンはパーキンソン病で死にます。その理由を探るために、研究チームはパーキンソン病の患者の脳組織と単一細胞遺伝子データを解析しました。全体としては、TMBIM6タンパク質は疾患のある中脳組織で対照より高かったものの、詳細に見ると重要なひねりがありました:最も脆弱とされるドーパミンニューロン亜型では、TMBIM6発現がより抵抗性のニューロンよりも実際には低下していました。同時に、TMBIM6と他のストレス応答遺伝子間の通常の密接な協調も乱れていました。これらの所見は、一部の脳細胞がTMBIM6を増やす一方で、最も保護を必要とするニューロンはこの安全装置を失い、慢性的なストレスと死の信号にさらされることを示唆します。
細胞とハエで因果関係を証明する
TMBIM6が実際に生存に影響を与えるかを検証するため、研究者らは複数の実験系でそのレベルを上下させました。ドーパミン様マウス細胞でTMBIM6を減らすと、これらの細胞は毒性のあるα-シヌクレイン線維やパーキンソン様の化学毒素に対して著しく感受性が高くなりました。細胞はミトコンドリア機能のより大きな損失、カスパーゼ-3などの実行酵素の活性化の増加、細胞内容物の漏出といったプログラムされた細胞死の特徴を示しました。TMBIM6相当物の発現が少ないよう遺伝子改変したショウジョウバエでも同様の結果が得られ、眼や脳のドーパミンニューロンが失われ、特に農薬ロテノンに曝露されたときに運動障害が悪化しました。
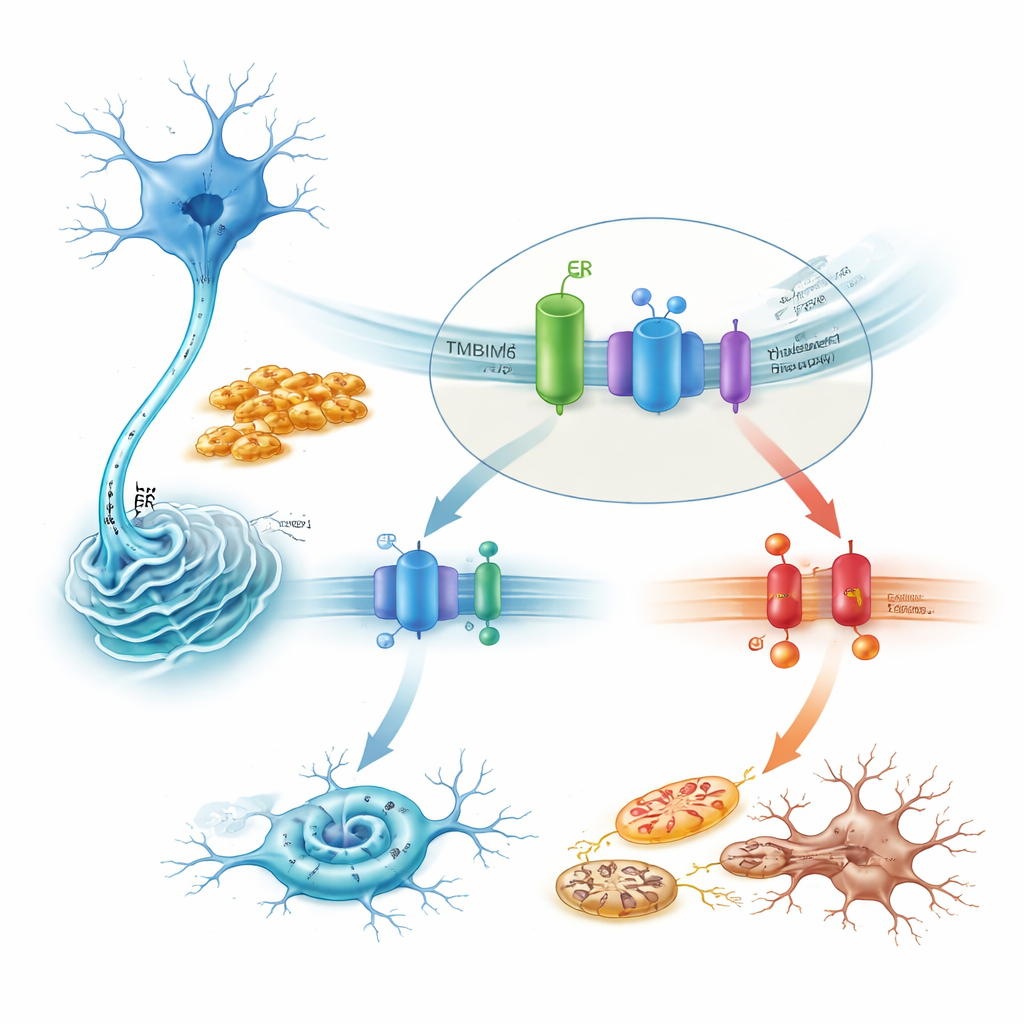
TMBIM6が致命的なストレス経路を抑える仕組み
メカニズムを詳しく調べると、TMBIM6は安静時にIRE1αと物理的に結合していることが示されました。毒性のあるα-シヌクレイン線維はこの結合を乱し、IRE1αが強く活性化されるようにします。TMBIM6欠損細胞では、この活性化が著しく増幅され、XBP1のmRNAスプライシングの増加や他のIRE1α標的の分解という形で現れました。IRE1αを薬剤で阻害するか遺伝子をサイレンシングすると、TMBIM6が欠損したときに見られた増大した細胞死の多くが救済されました。下流では、有害な経路はストレスキナーゼJNK、細胞死促進タンパク質BAX、およびカスパーゼを経てアポトーシスを駆動する連鎖を形成していました。逆に、TMBIM6を過剰発現させるとIRE1α活性が抑えられ、これらの死の信号が減少してミトコンドリアが保護されましたが、α-シヌクレインの凝集量は変わらなかったため、TMBIM6は凝集体そのものではなく細胞のストレス処理を作用点としていることが示唆されます。
マウスで遺伝子治療様アプローチを試す
治療の可能性を探るため、著者らは無害なアデノ随伴ウイルス(AAV)を用いてヒトTMBIM6をマウスの黒質に直接届けました。2週間後、彼らは標準的なパーキンソン毒素である6-ヒドロキシドーパミンでドーパミン経路を損傷させました。マーカー遺伝子のみを受け取った対照マウスは明らかな運動障害を示し、影響を受けた前肢の使用が減り、梁上テストでのバランスが悪化しました。しかし、TMBIM6を運ぶウイルスで前処置されたマウスは有意に良好な成績を示し、ミスステップが少なく課題をより速く完了しました。培養一次ニューロンでは、同じAAV構築体が毒素やα-シヌクレイン線維によって引き起こされる細胞死とカスパーゼ活性化を軽減し、TMBIM6レベルを高めることでニューロンの耐性が向上するという主張を補強しました。
将来の治療にとっての意味
これらの結果は、TMBIM6が致命的なストレスセンサーであるIRE1αを抑え、ミトコンドリア不全とアポトーシスに至る一連の出来事を防ぐことでドーパミンニューロンを守る番人であることを示しています。病初期には細胞が対処戦略としてTMBIM6を上げるようですが、最も危険にさらされたニューロンでは最終的にこのシステムが破綻し、慢性的なストレスと細胞死へと傾きます。TMBIM6の回復や増強は――その機能を高める薬剤やここで試されたAAVのような遺伝子療法を通じて――パーキンソン病におけるニューロン喪失を遅らせるか予防する手段を提供する可能性があり、主にドーパミンを補う現在の治療を補完するものとなり得ます。
引用: Ahumada-Montalva, P., Muñoz-Carvajal, F., Bórquez-Macaya, S. et al. TMBIM6 enhances dopaminergic neuron survival by modulating the IRE1a pathway in Parkinson’s disease. Cell Death Dis 17, 385 (2026). https://doi.org/10.1038/s41419-025-08391-5
キーワード: パーキンソン病, ドーパミン作動性ニューロン, 小胞体ストレス, IRE1α経路, 神経保護