Clear Sky Science · de
TMBIM6 fördert das Überleben dopaminerger Neurone, indem es den IRE1α-Weg bei Parkinson reguliert
Warum diese Forschung für Menschen mit Parkinson wichtig ist
Die Parkinson-Krankheit raubt Menschen die geschmeidige Bewegung, weil zentrale Nervenzellen, die Dopamin herstellen, nach und nach absterben. Diese Studie enthüllt ein körpereigenes Schutzprotein, TMBIM6, das diesen empfindlichen Neuronen hilft, mit Stress in ihrer Proteinfaltungsmaschine zurechtzukommen. Indem gezeigt wird, dass die Erhöhung von TMBIM6 Neuronen am Leben erhalten und die Beweglichkeit in Tiermodellen verbessern kann, weist die Arbeit auf einen neuen therapeutischen Ansatz hin, der über das bloße Ersetzen von Dopamin hinausgeht.
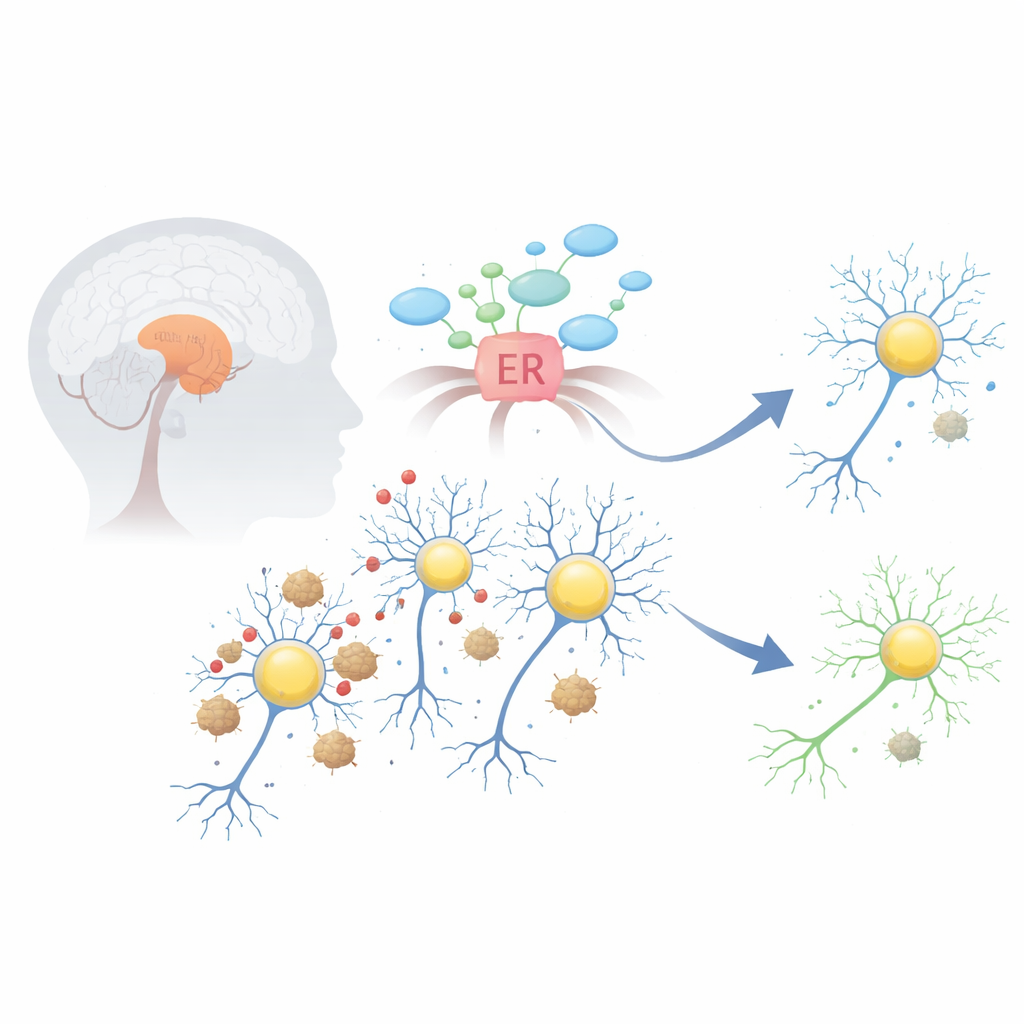
Das Problem innerhalb dopaminproduzierender Hirnzellen
Bei Parkinson kann ein Protein namens Alpha-Synuclein fehlgefaltet sein und sich zu klebrigen Aggregaten verklumpen, den sogenannten Lewy-Körpern. Diese Aggregatte stören mehrere lebenswichtige Systeme innerhalb der dopaminproduzierenden Neurone in einer Mittelhirnregion, der Substantia nigra. Eine der frühesten und schädlichsten Folgen ist Stress im endoplasmatischen Retikulum, der zellulären Fabrik für Proteinfaltung und -verarbeitung. Wenn dieses Kompartiment überlastet ist, schaltet es ein Notfallprogramm ein, die sogenannte unfolded protein response (UPR). Diese Reaktion kann anfangs helfen, führt aber bei anhaltender Aktivierung dazu, dass Zellen in Richtung Selbstzerstörung gedrängt werden.
Ein natürlicher Schutz: der TMBIM6-Sicherheitsmechanismus
Das Protein TMBIM6 sitzt in der Membran des endoplasmatischen Retikulums und wirkt normalerweise als Bremse für einen zentralen Stresssensor, IRE1α. Die Forschenden fragten zunächst, ob TMBIM6 an den relevanten Orten vorhanden ist, um bei Parkinson eine Rolle zu spielen. Mithilfe großer Genexpressionsdatenbanken stellten sie fest, dass TMBIM6 im menschlichen Mittelhirn und anderen Regionen mit vielen Dopaminneuronen stark exprimiert wird. In kultivierten Zellen und Mausneuronen, die Parkinson-ähnlichen Toxinen ausgesetzt waren – wie 6-Hydroxydopamin, Rotenon oder Alpha-Synuclein-Fibrillen – stiegen die TMBIM6-Spiegel früh an, was darauf hindeutet, dass Zellen diesen Faktor als schnelle Abwehrreaktion auf Stress hochfahren.
Wenn der Schutz in besonders anfälligen Neuronen versagt
Trotz dieser scheinbaren Abwehr sterben Dopaminneurone bei Parkinson. Um zu verstehen, warum, untersuchte das Team Hirngewebe und Einzelzell-Genetikdaten von Menschen mit Parkinson. Insgesamt war das TMBIM6-Protein im erkrankten Mittelhirn höher als in Kontrollen, doch eine genauere Betrachtung zeigte eine entscheidende Wendung: Innerhalb des Subtyps von Dopaminneuronen, die besonders anfällig sind, war die TMBIM6-Expression tatsächlich niedriger als in widerstandsfähigeren Neuronen. Gleichzeitig war die sonst enge Koordination zwischen TMBIM6 und anderen Stressantwortgenen gestört. Zusammengenommen legen diese Befunde nahe, dass, während einige Gehirnzellen TMBIM6 hochfahren, die Neurone, die am dringendsten Schutz bräuchten, diesen Sicherheitsmechanismus verlieren und so chronischem Stress und Todess Signalen ausgesetzt bleiben.
Ursache und Wirkung in Zellen und Fliegen nachweisen
Um zu testen, ob TMBIM6 tatsächlich das Überleben beeinflusst, veränderten die Forschenden dessen Menge in mehreren Labormodellen nach oben und unten. Als sie TMBIM6 in dopaminähnlichen Mauszellen reduzierten, wurden diese Zellen deutlich empfindlicher gegenüber toxischen Alpha-Synuclein-Fibrillen und chemischen Giften, die Parkinson nachahmen. Die Zellen zeigten stärkeren Verlust der Mitochondrienfunktion, stärkere Aktivierung von Ausführungsenzymen wie Caspase‑3 und mehr Austreten von Zellbestandteilen – Kennzeichen des programmierten Zelltods. Ähnliche Ergebnisse zeigten Fruchtfliegen, die so gentechnisch verändert wurden, dass sie weniger des TMBIM6-Äquivalents produzierten: Sie verloren Dopaminneurone in Auge und Gehirn und entwickelten stärkere Bewegungsstörungen, insbesondere nach Exposition gegenüber dem Insektizid Rotenon.
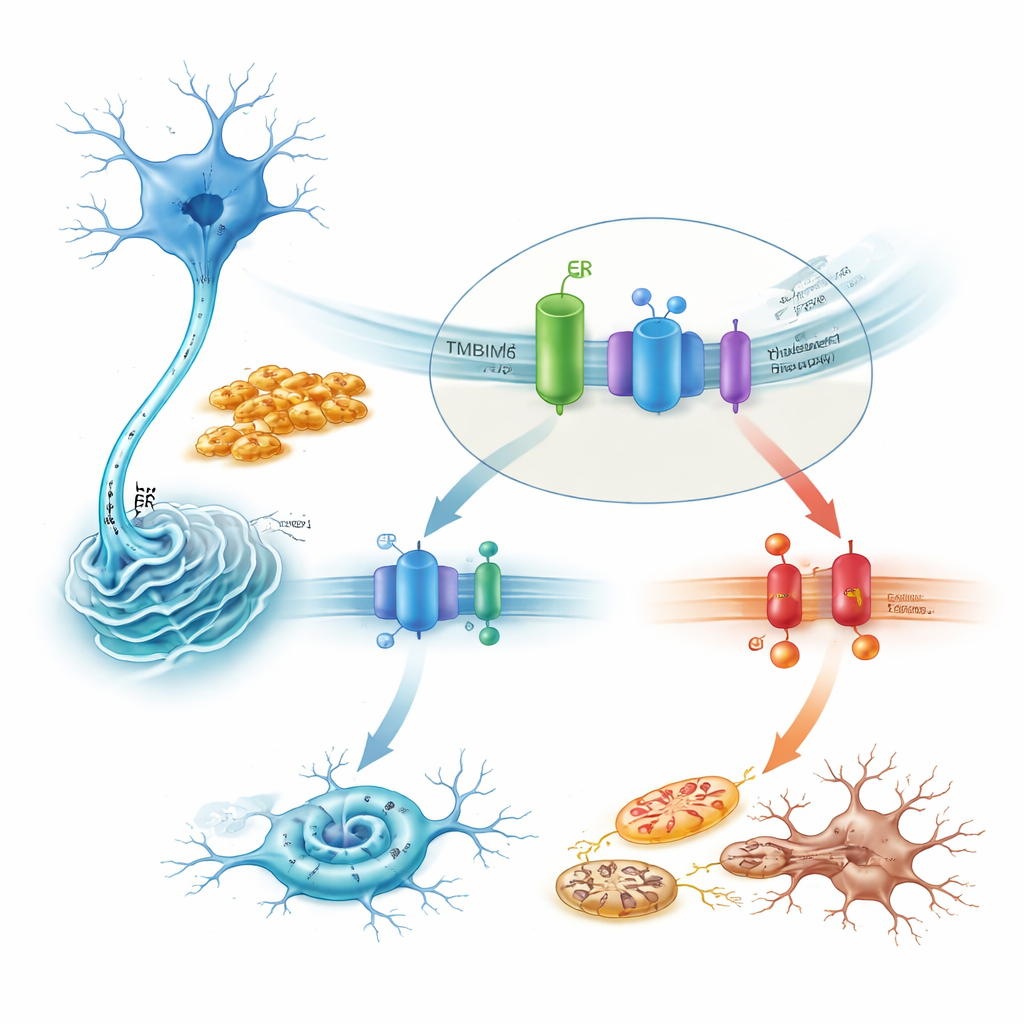
Wie TMBIM6 einen tödlichen Stressweg zügelt
Mechanistisch zeigt die Studie, dass TMBIM6 im Ruhezustand physisch mit IRE1α assoziiert ist. Toxische Alpha‑Synuclein‑Fibrillen stören diese Partnerschaft und befreien IRE1α, sodass es stark aktiviert werden kann. In TMBIM6-defizienten Zellen wird diese Aktivierung übermäßig, was sich in verstärktem Spleißen der mRNA für XBP1 und im Abbau eines weiteren IRE1α-Zielmoleküls zeigt. Die Blockade von IRE1α mit Medikamenten oder durch Stilllegung seines Gens rettete weitgehend den erhöhten Zelltod, der bei fehlendem TMBIM6 auftrat. Weiter downstream lief der schädliche Weg über die Stresskinase JNK, das pro‑apoptotische Protein BAX und Caspasen und bildete eine Kaskade, die zur Apoptose führt. Umgekehrt dämpfte die Überexpression von TMBIM6 die IRE1α‑Aktivität, verringerte diese Todessignale und schützte die Mitochondrien, ohne die Menge der Alpha‑Synuclein‑Aggregation zu verändern – was darauf hindeutet, dass TMBIM6 auf die Stressbewältigung der Zelle wirkt und nicht auf die Aggregate selbst.
Ein gen‑therapieähnlicher Ansatz in Mäusen testen
Um das therapeutische Potenzial zu erkunden, setzten die Autorinnen und Autoren ein harmloses Adeno‑assoziiertes Virus (AAV) ein, um menschliches TMBIM6 direkt in die Substantia nigra von Mäusen zu bringen. Zwei Wochen später verletzten sie den Dopaminweg mit dem Standard‑Parkinson‑Toxin 6‑Hydroxydopamin. Kontrollmäuse, die nur ein Markergen erhielten, zeigten deutliche motorische Defizite: reduzierte Nutzung der betroffenen Vorderpfote und schlechtere Balance bei einem Balkentest. Mäuse, die zuvor mit dem TMBIM6‑tragenden Virus behandelt worden waren, schnitten hingegen deutlich besser ab, machten weniger Fehltritte und bewältigten die Aufgaben schneller. In kultivierten Primärneuronen milderte derselbe AAV‑Konstrukt den durch Toxine oder Alpha‑Synuclein‑Fibrillen ausgelösten Zelltod und die Caspase‑Aktivierung, was die These stützt, dass die Erhöhung von TMBIM6 die Widerstandsfähigkeit von Neuronen verbessert.
Was das für zukünftige Behandlungen bedeuten könnte
Zusammen zeichnen diese Befunde TMBIM6 als Wächter dopaminerger Neurone, der wirkt, indem er den gefährlichen Stresssensor IRE1α unter Kontrolle hält und so eine Kaskade verhindert, die zu mitochondrialem Versagen und Apoptose führt. In frühen Krankheitsstadien scheinen Zellen TMBIM6 als Bewältigungsstrategie hochzufahren, doch in den am stärksten gefährdeten Neuronen versagt das System letztlich und kippt das Gleichgewicht zugunsten chronischen Stresses und Zelltods. Die Wiederherstellung oder Verstärkung von TMBIM6 – durch Wirkstoffe, die seine Funktion stärken, oder durch Gentherapien wie den hier getesteten AAV‑Ansatz – könnte einen Weg bieten, den Neuronenverlust bei Parkinson zu verlangsamen oder zu verhindern und die derzeitigen Therapien zu ergänzen, die hauptsächlich Dopamin ersetzen, statt die Zellen zu schützen, die es produzieren.
Zitation: Ahumada-Montalva, P., Muñoz-Carvajal, F., Bórquez-Macaya, S. et al. TMBIM6 enhances dopaminergic neuron survival by modulating the IRE1a pathway in Parkinson’s disease. Cell Death Dis 17, 385 (2026). https://doi.org/10.1038/s41419-025-08391-5
Schlüsselwörter: Morbus Parkinson, dopaminerge Neurone, Stress im endoplasmatischen Retikulum, IRE1α-Signalweg, Neuroprotektion