Clear Sky Science · sv
Antimikrobiellt peptidinducerad hyperpolarisering av innermembranet är kopplad till ökad känslighet för antibiotika och dämpad MIC‑ökning hos mångdrugresistenta Gramnegativa patogener
Varför denna forskning är viktig för vardagshälsa
Dödligt infektioner blir svårare att behandla när bakterier utvecklar motståndskraft mot våra starkaste antibiotika. Denna studie undersöker ett nytt sätt att få befintliga läkemedel att fungera igen genom att lägga till en liten, naturinspirerad molekyl kallad peptid. Arbetet antyder att vi inte alltid behöver helt nya antibiotika för varje hot; i stället kan vi "superladda" de vi redan har samtidigt som vi dämpar den okontrollerade inflammationen som gör sepsis så farligt.
En hjälpmolekyl för kämpande antibiotika
Forskarna fokuserade på en modifierad fisk‑härledd molekyl kallad TP2‑5, en positivt laddad peptid som i sig kan döda vissa bakterier. De undersökte om mycket små mängder av denna peptid i kombination med standardantibiotika kunde göra svåra, mångdrugresistenta smittämnen lättare att behandla. Genom att arbeta med problemstammar av Gramnegativa bakterier som läkemedelsresistent Escherichia coli och Acinetobacter baumannii fann de att tillsats av endast en fjärdedel av den minsta TP2‑5‑dos som krävs för att hämma tillväxten gjorde att flera olika antibiotika, inklusive meropenem, kolistin, ciprofloxacin och till och med vanligen ineffektiva vankomycin, fungerade mycket bättre. I laborationstester kunde kombinationer som använde svaga doser av båda substanserna tillsammans helt rensa ut bakterier som inget av läkemedlen ensam kunde kontrollera.
Hindra att resistensen stiger så snabbt
Antibiotikaresistens förvärras normalt över tid när bakterier utsätts upprepade gånger för ett läkemedel. För att efterlikna denna process odlade teamet resistenta E. coli i tre veckor med daglig exponering för antingen antibiotika ensamt, TP2‑5 ensamt eller antibiotika plus lågdos TP2‑5. När antibiotika användes ensamma steg den mängd som krävdes för att stoppa bakterietillväxt dramatiskt—upp till 128‑faldigt för vissa läkemedel—vilket signalerade stark ny resistens. När samma antibiotika kombinerades med TP2‑5 var denna eskalering mycket mildare, vilket tyder på att hjälppeptiden kan bromsa bakteriernas förmåga att anpassa sig. Under tiden visade bakterier som exponerades för TP2‑5 ensamt liten förändring i sin känslighet för peptiden, vilket antyder att det kan vara svårare för dem att utveckla starka försvar mot denna typ av membrantargeterande angrepp.
Hur peptiden omformar bakterieskalet
För att förstå varför TP2‑5 förstärker antibiotikaeffekten undersökte forskarna det yttre skalet hos Gramnegativa bakterier, som fungerar både som rustning och portvakt. Genom att använda kemiska färgämnen som lyser upp när membran läcker eller ändrar spänning, tillsammans med kryo‑elektrontomografi som avbildar frysta celler i tre dimensioner, visade de att mycket låga, icke‑dödliga doser av TP2‑5 subtilt tunnar ut och punkterar det yttre skiktet samtidigt som de för inre skiktet i ett ovanligt energirikt eller "hyperpolariserat" tillstånd. Vid högre doser sliter samma peptid isär membranen. Tidsförsök visade att när bakterier först förs in i detta hyperpolariserade, lätt läckande tillstånd av TP2‑5, leder senare exponering för antibiotika snabbt till kollaps av innermembranet och död. Peptiden föredrar att binda till negativt laddade komponenter kallade lipopolysackarider och specifika fosfolipider, som är rikliga i Gramnegativa envelopes, vilket förklarar dess selektivitet för dessa patogener.
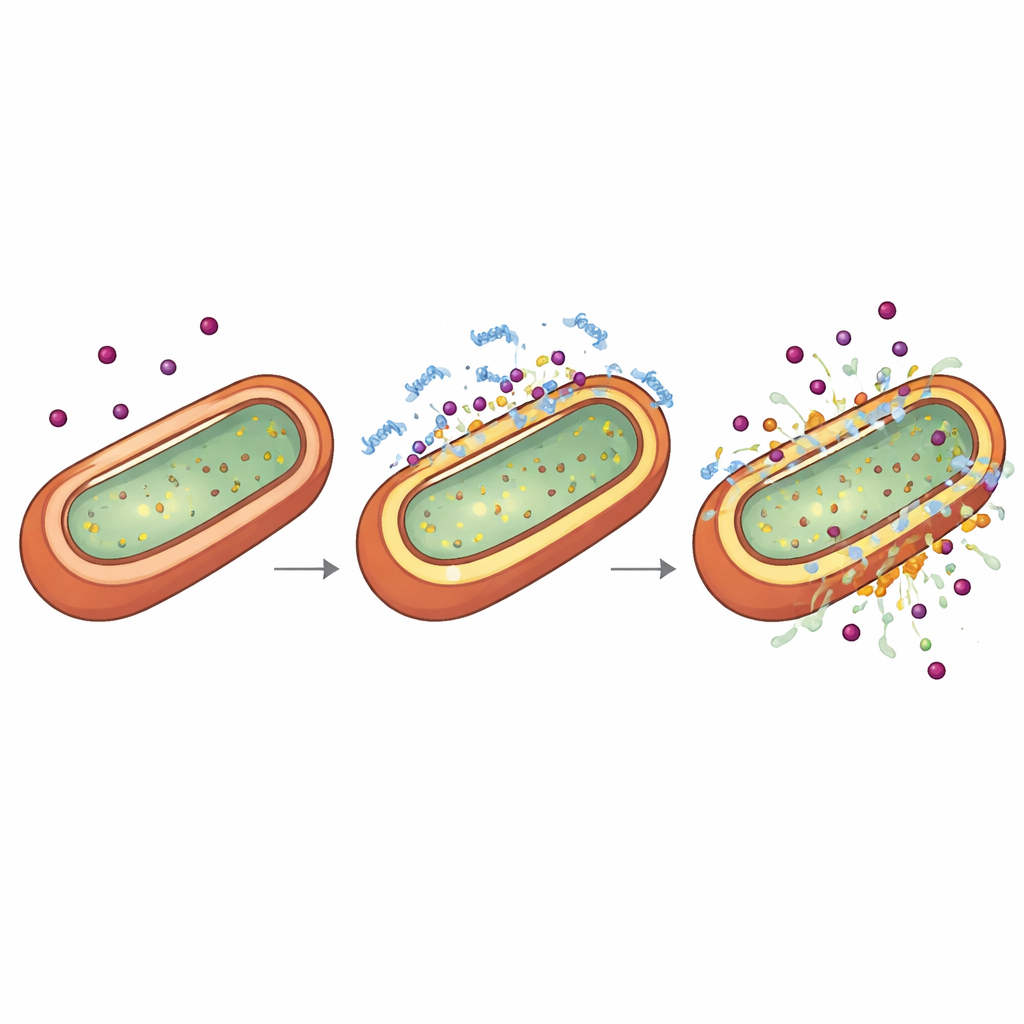
Tysta kroppens farliga överreaktion
Allvarliga infektioner beror inte bara på mikroben; kroppens egna immunsvar spiral ofta ur kontroll och leder till sepsis och organsvikt. Eftersom TP2‑5 binder till bakteriella ytmolekyler som utlöser inflammation, testade teamet om den också kunde dämpa immunöverreaktionen. I musimmunceller blockerade TP2‑5 bindningen av dessa bakteriella fragment, dämpade viktiga signalvägar och minskade brett aktiveringen av gener som driver inflammation. I djurmodeller, inklusive ett larvinfektionssystem, en läkemedelsresistent pneumonimodell och en standard mus‑sepsismodell efter operation, minskade TP2‑5 ensam eller i kombination med antibiotika bakteriemängder, sänkte markörer för organskada, reducerade inflammatoriska budbärare i blodet och gav anmärkningsvärt 100 % överlevnad i den polymikrobiella sepsismodellen, där standardantibiotika hjälpte men inte gav fullgott skydd.
Balans mellan effekt och säkerhet
Alla nya antiinfektiva måste skada mikrober mer än patienter. TP2‑5 visade denna typ av selektivitet i odlade humana och musceller, där skadliga effekter endast uppträdde vid koncentrationer många gånger högre än de som behövs för att hämma bakterier. Hos möss orsakade både intravenös och lunginriktad dosering ingen meningsfull viktminskning, organskada eller blodcellsavvikelser vid nivåer relevanta för behandling. Peptiden tenderade att ackumuleras främst i levern och rensades gradvis över flera dagar, vilket stöder idén att den kan ges i adjuvanta, hjälpdoser utan uppenbar toxicitet.
Vad detta innebär för framtida behandlingar
Detta arbete presenterar TP2‑5 som en "membran‑sensibiliserande" partner för befintliga antibiotika: den luckrar upp skyddsskiktet hos Gramnegativa superbugs i ett särskilt energirikt tillstånd som gör dem lättare att döda, samtidigt som den fångar upp inflammatoriska utlösare som kan föra patienter in i dödlig sepsis. Även om studien inte bevisade att det ovanliga hyperpolariserade tillståndet är den direkta orsaken till förbättrad läkemedelsaktivitet, tyder den starka länken i tid och effekt på att det är en viktig pusselbit. Om liknande peptider kan användas säkert hos människor kan de förlänga den nyttiga livslängden för våra nuvarande antibiotika och erbjuda en tvåprongad strategi—att slå mot bakterierna och dämpa kroppens svar—som är särskilt värdefull för svårbehandlade, mångdrugresistenta infektioner.
Citering: Yeh, JC., Hazam, P.K., Lin, YY. et al. Antimicrobial peptide-induced inner membrane hyperpolarization is associated with antibiotic sensitization and attenuated MIC escalation in multidrug-resistant Gram-negative pathogens. npj Antimicrob Resist 4, 33 (2026). https://doi.org/10.1038/s44259-026-00210-x
Nyckelord: antimikrobiella peptider, antibiotika‑adjuvanser, mångdrugresistenta bakterier, sepsis, Gramnegativa infektioner