Clear Sky Science · nl
Door antimicrobieel peptide geïnduceerde hyperpolarisatie van het binnenmembraan wordt geassocieerd met antibioticagevoeligheid en verminderde MIC‑toename bij multiresistente Gram‑negatieve pathogenen
Waarom dit onderzoek er toe doet voor de dagelijkse gezondheid
Dodelijke infecties worden moeilijker te behandelen naarmate bacteriën onze krachtigste antibiotica leren te weerstaan. Deze studie onderzoekt een nieuwe manier om bestaande medicijnen weer effectief te maken door een klein, natuurlijk geïnspireerd molecuul toe te voegen: een peptide. Het werk suggereert dat we niet voor elke nieuwe dreiging een compleet nieuw antibioticum nodig hebben; in plaats daarvan kunnen we de middelen die we al hebben "oppeppen" en tegelijkertijd de uit de hand gelopen ontsteking die sepsis zo gevaarlijk maakt dempen.
Een hulpstof voor worstelende antibiotica
De onderzoekers richtten zich op een aangepast visafgeleid molecuul genaamd TP2‑5, een positief geladen peptide dat op zichzelf sommige bacteriën kan doden. Ze vroegen zich af of zeer kleine hoeveelheden van dit peptide samen met standaardantibiotica harde, multiresistente kiemen behandelbaarder kunnen maken. Werkend met probleemstammen van Gram‑negatieve bacteriën zoals medicijnresistente Escherichia coli en Acinetobacter baumannii, ontdekten ze dat het toevoegen van slechts een kwart van de minimale TP2‑5‑dosis die nodig is om groei te remmen, verschillende antibiotica — waaronder meropenem, colistine, ciprofloxacine en zelfs normaal gesproken ineffectief vancomycine — aanzienlijk beter liet werken. In laboratoriumtests konden combinaties die zwakke doseringen van beide middelen gebruikten bacteriën volledig uitroeien die met elk middel afzonderlijk niet onder controle te krijgen waren.
Weerstand die minder snel toeneemt
Antibioticaresistentie verergert meestal in de loop van de tijd wanneer bacteriën herhaaldelijk aan een middel worden blootgesteld. Om dit proces na te bootsen, kweekte het team resistente E. coli drie weken lang met dagelijkse blootstelling aan óf antibiotica alleen, TP2‑5 alleen, óf antibiotica plus lage dosis TP2‑5. Wanneer antibiotica alleen werden gebruikt, steeg de hoeveelheid die nodig was om bacteriegroei te stoppen dramatisch — voor sommige middelen tot 128‑voudig — wat wijst op sterke nieuwe resistentie. Wanneer dezelfde antibiotica werden gecombineerd met TP2‑5, was deze escalatie veel milder, wat suggereert dat het hulp‑peptide het vermogen van de bacteriën om zich aan te passen kan vertragen. Ondertussen vertoonden bacteriën die alleen aan TP2‑5 werden blootgesteld weinig verandering in hun gevoeligheid voor het peptide, wat erop wijst dat het voor hen moeilijker kan zijn om sterke verdedigingsmechanismen tegen dit type membraanaanval te ontwikkelen.
Hoe het peptide de bacteriële omhulling herschikt
Om te begrijpen waarom TP2‑5 de werking van antibiotica versterkt, onderzochten de wetenschappers de buitenste schaal van Gram‑negatieve bacteriën, die zowel harnas als poortwachter is. Met chemische kleurstoffen die gaan oplichten wanneer membranen lekken of van spanning veranderen, en met cryo‑elektronentomografie die bevroren cellen in drie dimensies afbeeldt, toonden ze aan dat zeer lage, niet‑dodelijke doses TP2‑5 de buitenlaag subtiel dunner maken en doorprikken terwijl het binnenmembraan in een ongewoon geëlektriseerd of "gehyperpolariseerd" stadium wordt gebracht. Bij hogere doseringen scheurt hetzelfde peptide de membranen uit elkaar. Timingexperimenten lieten zien dat wanneer bacteriën eerst in deze gehyperpolariseerde, licht lekke toestand worden gebracht door TP2‑5, latere blootstelling aan antibiotica hun binnenmembraan snel doet instorten en hen doodt. Het peptide bindt bij voorkeur aan negatief geladen componenten genaamd lipopolysachariden en aan specifieke fosfolipiden, die overvloedig aanwezig zijn in Gram‑negatieve omhulsels, wat zijn selectiviteit voor deze pathogenen verklaart.
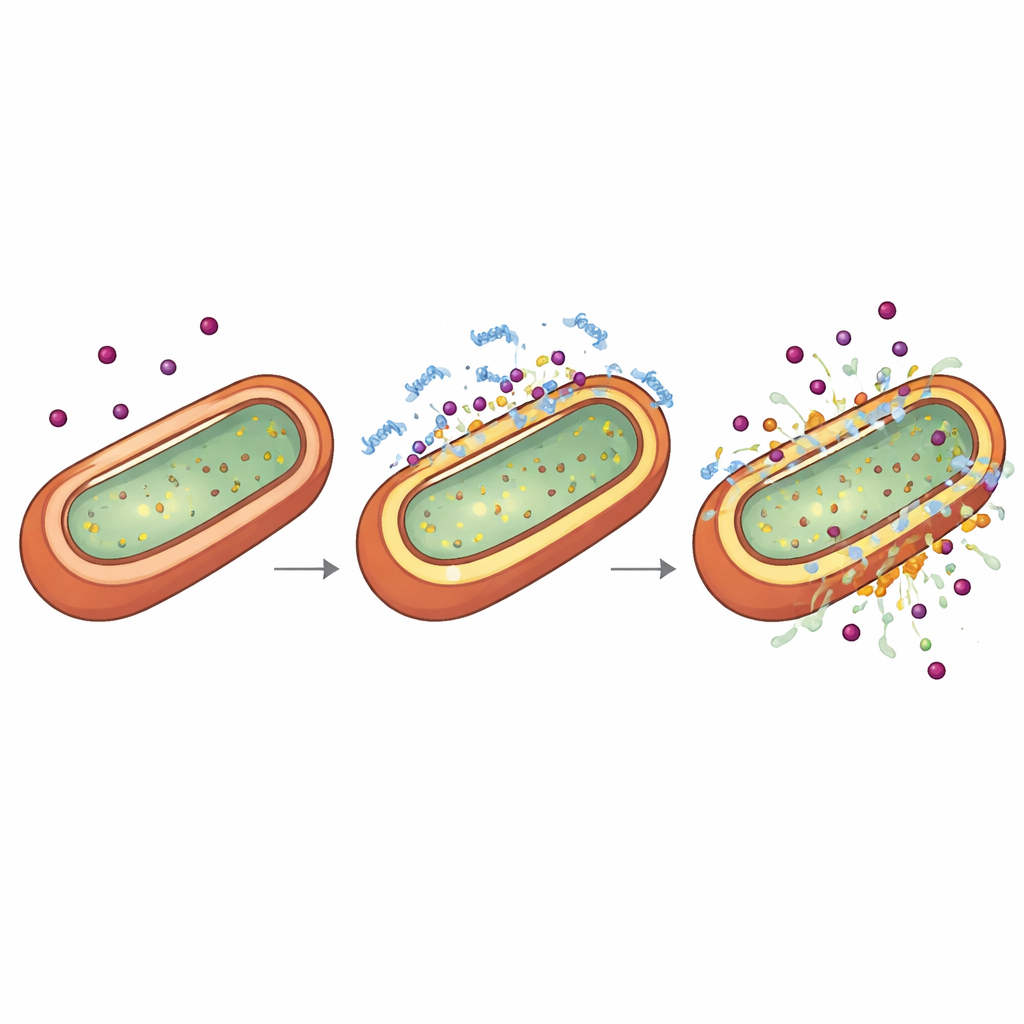
Het bedaren van de gevaarlijke overreactie van het lichaam
Ernstige infecties hangen niet alleen van de microbe af; de eigen immuunrespons van het lichaam loopt vaak uit de hand, wat leidt tot sepsis en orgaanfalen. Omdat TP2‑5 zich vasthecht aan bacteriële oppervlaktecomponenten die ontsteking veroorzaken, testte het team of het ook de immuunoveractivatie kon dempen. In immuuncellen van muizen blokkeerde TP2‑5 het binden van deze bacteriële fragmenten, verzwakte sleutel‑signaleringspaden en verminderde in brede zin de activering van genen die ontsteking aansturen. In diermodellen — waaronder een rupsinfectiesysteem, een geneesmiddelresistent longontstekingmodel en een standaard muis‑sepsisoperatie — verminderde TP2‑5, zowel alleen als in combinatie met antibiotica, het aantal bacteriën, verlaagde markers voor orgaanschade, verminderde ontstekingsboodschappers in het bloed en zorgde opvallend voor 100% overleving in het polymicrobiële sepsismodel, waar standaardantibiotica hielpen maar niet volledig beschermden.
Balanceren van effectiviteit en veiligheid
Elk nieuw anti‑infectivum moet meer schade toebrengen aan microben dan aan patiënten. TP2‑5 toonde dit soort selectiviteit in gekweekte humane en muizencellen, waar schadelijke effecten pas bij concentraties ontstonden die vele malen hoger waren dan die nodig om bacteriën te remmen. Bij muizen veroorzaakten zowel intraveneuze als rechtstreeks op de long gerichte toediening geen betekenisvol gewichtsverlies, orgaanschade of afwijkingen in bloedcellen bij behandelingsrelevante niveaus. Het peptide hoopte zich voornamelijk op in de lever en werd geleidelijk over enkele dagen geklaard, wat ondersteunt dat het in adjuvante, hulpdoses kan worden toegediend zonder duidelijke toxiciteit.
Wat dit betekent voor toekomstige behandelingen
Dit werk presenteert TP2‑5 als een "membraan‑sensibiliserende" partner voor bestaande antibiotica: het versoepelt de beschermende laag van Gram‑negatieve superbugs in een speciaal geëlektriseerde toestand die hen makkelijker te doden maakt, terwijl het ook ontstekingstrekkers opvangt die patiënten in dodelijke sepsis kunnen duwen. Hoewel de studie niet aantoonde dat de ongebruikelijke gehyperpolariseerde toestand de directe oorzaak is van de verbeterde medicijneffectiviteit, suggereert de sterke koppeling in timing en effect dat het een belangrijk stuk van de puzzel is. Als soortgelijke peptiden veilig bij mensen kunnen worden gebruikt, zouden ze de bruikbare levensduur van onze huidige antibiotica kunnen verlengen en een tweesnijdende aanpak bieden — zowel de bacterie raken als de reactie van het lichaam kalmeren — wat bijzonder waardevol is voor moeilijk te behandelen, multiresistente infecties.
Bronvermelding: Yeh, JC., Hazam, P.K., Lin, YY. et al. Antimicrobial peptide-induced inner membrane hyperpolarization is associated with antibiotic sensitization and attenuated MIC escalation in multidrug-resistant Gram-negative pathogens. npj Antimicrob Resist 4, 33 (2026). https://doi.org/10.1038/s44259-026-00210-x
Trefwoorden: antimicrobiële peptiden, antibiotica‑adjuvanten, multidrug‑resistente bacteriën, sepsis, Gram‑negatieve infecties