Clear Sky Science · ru
Индуцированная антимикробными пептидами гиперполяризация внутренней мембраны связана с повышенной чувствительностью к антибиотикам и замедлением роста MIC у мультирезистентных грамотрицательных патогенов
Почему это исследование важно для повседневного здоровья
Смертельные инфекции становятся всё труднее лечить по мере того, как бактерии вырабатывают устойчивость к нашим сильнейшим антибиотикам. В этом исследовании изучается новый способ вернуть эффективность существующих препаратов: добавление небольшой, натуралистично вдохновлённой молекулы — пептида. Работа показывает, что для борьбы с некоторыми угрозами нам необязательно создавать совершенно новые антибиотики; можно «усилить» уже имеющиеся препараты и одновременно приглушить неконтролируемое воспаление, которое делает сепсис особенно опасным.
Молекула‑помощник для ослабленных антибиотиков
Учёные сосредоточились на модифицированном пептиде TP2‑5, происходящем от рыбьих молекул, положительно заряженном и способном самостоятельно убивать некоторые бактерии. Они проверили, помогут ли очень малые количества этого пептида вместе со стандартными антибиотиками справляться с трудными мультирезистентными штаммами. На проблемных штаммах грамотрицательных бактерий, таких как резистентные Escherichia coli и Acinetobacter baumannii, выяснилось, что добавление лишь одной четверти минимальной концентрации TP2‑5, требующейся для подавления роста, значительно усиливало действие нескольких антибиотиков, включая меропенем, колистин, ципрофлоксацин и даже обычно неэффективный ванкомицин. В лабораторных тестах комбинации с низкими дозами обоих препаратов могли полностью уничтожать бактерии, с которыми ни один из них по отдельности не справлялся.
Замедление роста резистентности
Устойчивость к антибиотикам обычно усиливается со временем при повторном воздействии препарата. Чтобы смоделировать этот процесс, команда культивировала резистентные E. coli в течение трёх недель при ежедневном воздействии либо антибиотиков в одиночку, либо TP2‑5 в одиночку, либо антибиотиков в сочетании с низкой дозой TP2‑5. При использовании только антибиотиков требовавшаяся для подавления роста концентрация резко возрастала — до 128‑кратного увеличения для некоторых препаратов — что свидетельствовало о сильной появляющейся резистентности. При сочетании тех же антибиотиков с TP2‑5 это повышение было заметно слабее, что указывает на способность вспомогательного пептида замедлять адаптацию бактерий. В то же время бактерии, подвергавшиеся только TP2‑5, проявляли незначительные изменения чувствительности к пептиду, намекая на то, что им труднее выработать сильную защиту против такого типа атак, нацеленных на мембрану.
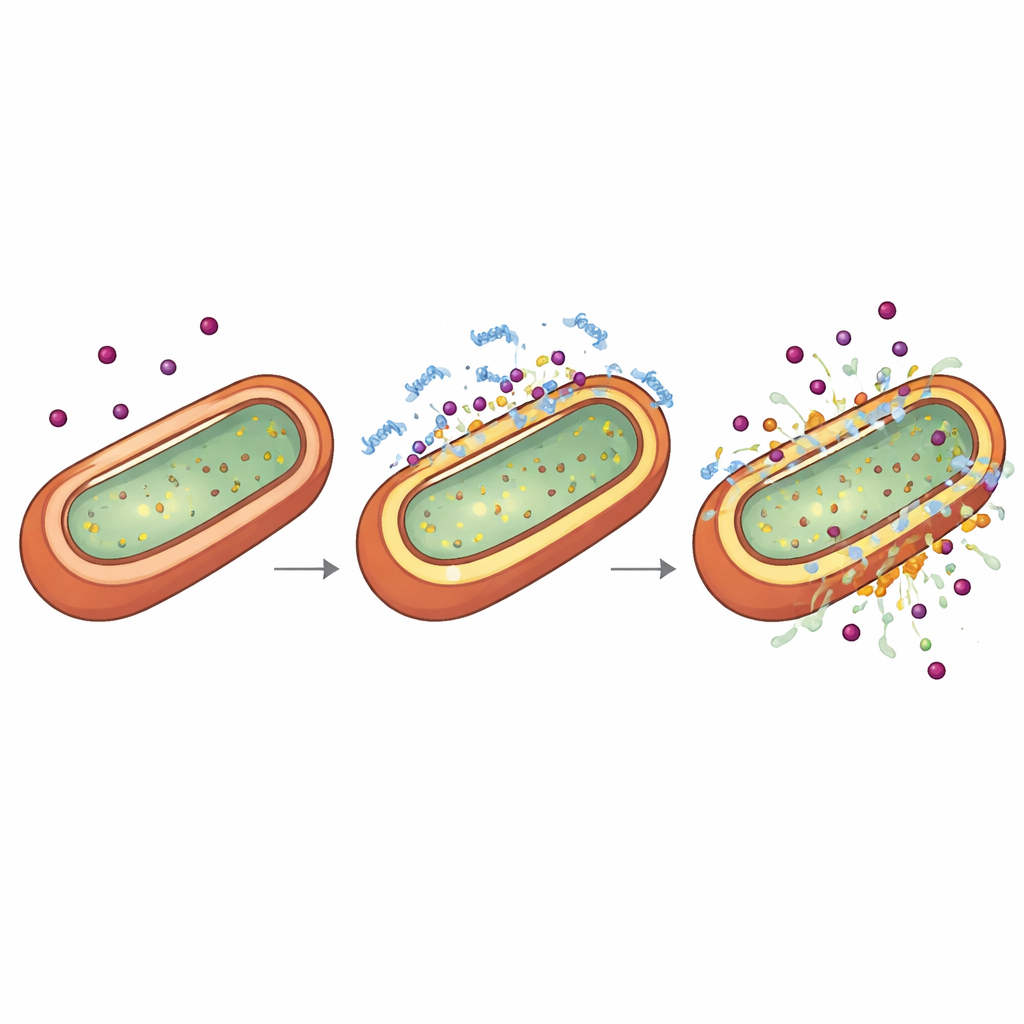
Как пептид изменяет оболочку бактерий
Чтобы понять, почему TP2‑5 усиливает действие антибиотиков, учёные изучили внешнюю оболочку грамотрицательных бактерий, выполняющую роль и брони, и привратника. Используя химические красители, светящиеся при протечках или изменениях электрического потенциала мембран, а также крио‑электронную томографию для трёхмерного изображения замороженных клеток, они показали, что очень низкие, неубийственные дозы TP2‑5 тонко истончают и прокалывают внешний слой, одновременно переводя внутреннюю мембрану в необычно возбужденное или «гиперполяризованное» состояние. При более высоких дозах тот же пептид разрывает мембраны. Эксперименты по времени показали, что когда бактерии сначала переводят в это гиперполяризованное, слегка проницаемое состояние под действием TP2‑5, последующее воздействие антибиотиков быстро вызывает коллапс внутренней мембраны и гибель клеток. Пептид преимущественно связывается с отрицательно заряженными компонентами, такими как липополисахариды и специфические фосфолипиды, которые обильно присутствуют в оболочке грамотрицательных бактерий, что объясняет его селективность по отношению к этим патогенам.
Усмирение опасной чрезмерной реакции организма
Тяжёлые инфекции зависят не только от микроба; собственный иммунный ответ организма часто выходит из под контроля, приводя к сепсису и отказу органов. Поскольку TP2‑5 связывается с бактериальными поверхностными молекулами, запускающими воспаление, команда проверила, может ли он также подавлять иммунную гиперактивность. В иммунных клетках мышей TP2‑5 блокировал связывание этих бактериальных фрагментов, ослаблял ключевые сигнальные пути и в целом снижал активацию генов, отвечающих за воспаление. В моделях на животных, включая систему с гусеницей в качестве модели инфекции, модель лекарственно‑устойчивой пневмонии и стандартную операцию по индукции сепсиса у мышей, TP2‑5 в одиночку или в комбинации с антибиотиками сокращал количество бактерий, снижал маркеры повреждения органов, уменьшал уровень провоспалительных медиаторов в крови и, что особенно заметно, обеспечивал 100% выживаемость в полимикробной модели сепсиса, где стандартные антибиотики помогали, но не давали полной защиты.
Баланс между эффективностью и безопасностью
Любое новое антимикробное средство должно наносить больший вред микробам, чем пациентам. TP2‑5 продемонстрировал такую селективность в культурах человеческих и мышиных клеток: вредные эффекты возникали только при концентрациях, многократно превышающих те, которые необходимы для подавления бактерий. У мышей как внутривенное, так и прицельное легочное введение не вызывало значительной потери веса, повреждения органов или отклонений в составе крови при уровнях, релевантных для лечения. Пептид, как правило, накапливался преимущественно в печени и постепенно выводился в течение нескольких дней, что поддерживает идею о возможности его применения в качестве адъюванта в лечебных дозах без очевидной токсичности.
Что это означает для будущих терапий
Эта работа представляет TP2‑5 как «модификатор мембраны» — партнёра для существующих антибиотиков: он ослабляет защитную оболочку грамотрицательных суперинфекций, переводя её в особое возбужденное состояние, которое делает бактерии более уязвимыми для уничтожения, одновременно поглощая воспалительные триггеры, способные привести пациента к смертельному сепсису. Хотя исследование не доказало, что необычное гиперполяризованное состояние напрямую вызывает улучшение действия антибиотиков, сильная временная и функциональная связь указывает на его важную роль в механизме. Если подобные пептиды удастся безопасно применить у людей, они могли бы продлить срок годности наших текущих антибиотиков и предложить двуфокусный подход — уничтожение бактерий и смягчение реакции организма — особенно ценный при трудно‑лечимых мультирезистентных инфекциях.
Цитирование: Yeh, JC., Hazam, P.K., Lin, YY. et al. Antimicrobial peptide-induced inner membrane hyperpolarization is associated with antibiotic sensitization and attenuated MIC escalation in multidrug-resistant Gram-negative pathogens. npj Antimicrob Resist 4, 33 (2026). https://doi.org/10.1038/s44259-026-00210-x
Ключевые слова: антибактериальные пептиды, адъюванты к антибиотикам, мультирезистентные бактерии, сепсис, грамотрицательные инфекции