Clear Sky Science · it
Iperpolarizzazione della membrana interna indotta da peptidi antimicrobici è associata a sensibilizzazione agli antibiotici e attenuazione dell’aumento della CIM in patogeni Gram‑negativi multiresistenti
Perché questa ricerca conta per la salute quotidiana
Le infezioni mortali stanno diventando più difficili da trattare man mano che i batteri imparano a resistere ai nostri antibiotici più potenti. Questo studio esplora un nuovo modo per far tornare efficaci i farmaci esistenti aggiungendo una piccola molecola di origine naturale chiamata peptide. Il lavoro suggerisce che non sempre serve un antibiotico completamente nuovo per ogni minaccia; possiamo invece “potenziare” quelli che già abbiamo, riducendo al contempo l’infiammazione fuori controllo che rende la sepsi così pericolosa.
Una molecola di supporto per antibiotici in difficoltà
I ricercatori si sono concentrati su una molecola modificata derivata da pesci chiamata TP2‑5, un peptide carico positivamente che da solo può uccidere alcuni batteri. Hanno verificato se dosi molto piccole di questo peptide, sommate agli antibiotici standard, potessero rendere più trattabili i germi multiresistenti. Lavorando con ceppi problematici di batteri Gram‑negativi come Escherichia coli resistente ai farmaci e Acinetobacter baumannii, hanno scoperto che aggiungendo solo un quarto della dose minima di TP2‑5 necessaria per inibire la crescita, diversi antibiotici — tra cui meropenem, colistina, ciprofloxacina e persino la vancomicina, normalmente inefficace — funzionavano molto meglio. Nei test di laboratorio, combinazioni che usavano dosi deboli di entrambi i composti potevano eliminare completamente batteri che nessuno dei due farmaci da solo riusciva a controllare.
Impedire che la resistenza aumenti troppo velocemente
La resistenza agli antibiotici di solito peggiora nel tempo se i batteri sono esposti ripetutamente a un farmaco. Per imitare questo processo, il team ha coltivato E. coli resistente per tre settimane con esposizione quotidiana a antibiotici da soli, a TP2‑5 da solo, o ad antibiotici più basse dosi di TP2‑5. Quando gli antibiotici venivano usati da soli, la quantità necessaria per bloccare la crescita batterica aumentava drasticamente — fino a 128 volte per alcuni farmaci — segnalando una forte acquisizione di resistenza. Quando gli stessi antibiotici venivano combinati con TP2‑5, questo incremento era molto più contenuto, suggerendo che il peptide di supporto può rallentare la capacità dei batteri di adattarsi. Nel frattempo, i batteri esposti solo a TP2‑5 mostravano scarsi cambiamenti nella loro sensibilità al peptide, suggerendo che potrebbe essere più difficile per loro evolvere difese forti contro questo tipo di attacco mirato alla membrana.
Come il peptide rimodella l’involucro batterico
Per capire perché TP2‑5 potenzia l’azione degli antibiotici, gli scienziati hanno esaminato l’involucro esterno dei batteri Gram‑negativi, che funge sia da corazza sia da guardiano. Usando coloranti chimici che si illuminano quando le membrane perdono contenuti o cambiano potenziale elettrico, insieme alla crio‑tomografia elettronica che fotografa le cellule congelate in tre dimensioni, hanno mostrato che dosi molto basse e non letali di TP2‑5 assottigliano e perforano leggermente lo strato esterno pur portando lo strato interno in uno stato insolitamente energizzato o “iperpolarizzato”. A dosi più alte, lo stesso peptide strappa le membrane. Esperimenti temporali hanno rivelato che quando i batteri sono prima indotti da TP2‑5 in questa condizione iperpolarizzata e leggermente permeabile, l’esposizione successiva agli antibiotici fa rapidamente collassare la membrana interna e li uccide. Il peptide tende a legarsi a componenti carichi negativamente chiamati lipopolisaccaridi e a specifici fosfolipidi, abbondanti negli involucri dei Gram‑negativi, spiegando la sua selettività per questi patogeni.
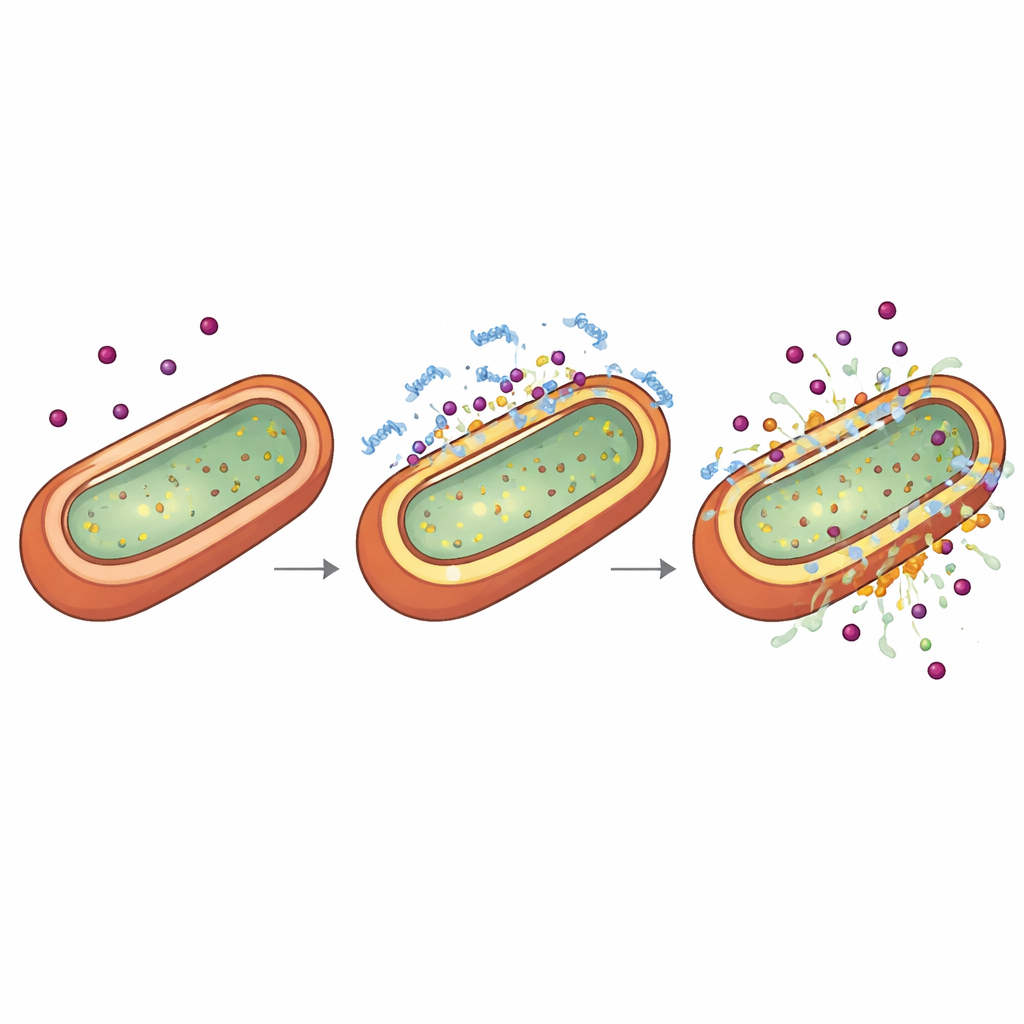
Attenuare la reazione eccessiva dell’organismo
Le infezioni gravi non dipendono solo dal microrganismo; la risposta immunitaria dell’ospite spesso precipita fuori controllo, portando a sepsi e insufficienza d’organo. Poiché TP2‑5 si lega a molecole di superficie batterica che scatenano l’infiammazione, il team ha testato se potesse anche ridurre l’iperattivazione immunitaria. In cellule immunitarie murine, TP2‑5 ha bloccato il legame di questi frammenti batterici, attenuato vie di segnalazione chiave e ridotto in modo ampio l’attivazione di geni che guidano l’infiammazione. In modelli animali, inclusi un sistema di infezione in bruchi, un modello di polmonite resistente ai farmaci e una procedura standard di sepsi nel topo, TP2‑5 da solo o in combinazione con antibiotici ha ridotto i conteggi batterici, abbassato i marcatori di danno d’organo, ridotto i messaggeri infiammatori nel sangue e, in modo notevole, ha prodotto il 100% di sopravvivenza nel modello di sepsi polimicrobica, dove gli antibiotici standard aiutavano ma non proteggevano completamente.
Bilanciare efficacia e sicurezza
Qualsiasi nuovo antivirale o antibatterico deve danneggiare più i microbi che i pazienti. TP2‑5 ha mostrato questo tipo di selettività in cellule umane e murine in coltura, dove gli effetti nocivi apparivano solo a concentrazioni molte volte superiori a quelle necessarie per bloccare i batteri. Nei topi, sia la somministrazione endovenosa sia quella diretta ai polmoni non hanno causato perdita di peso significativa, danni d’organo o anomalie degli elementi ematici a livelli utili per il trattamento. Il peptide tendeva ad accumularsi principalmente nel fegato ed è stato eliminato gradualmente nell’arco di diversi giorni, a sostegno dell’idea che può essere somministrato a dosi da adiuvante senza tossicità evidente.
Cosa significa per i trattamenti futuri
Questo lavoro presenta TP2‑5 come un partner “sensibilizzante della membrana” per antibiotici esistenti: allenta il rivestimento protettivo dei super‑batteri Gram‑negativi ponendoli in uno stato energetico speciale che li rende più facili da uccidere, oltre a sequestrare i fattori infiammatori che possono spingere i pazienti verso la sepsi letale. Sebbene lo studio non abbia dimostrato che lo stato iperpolarizzato sia la causa diretta della maggiore attività dei farmaci, il forte nesso temporale e d’effetto suggerisce che sia un pezzo importante del meccanismo. Se peptidi simili potranno essere usati in sicurezza nell’uomo, potrebbero estendere la vita utile dei nostri antibiotici attuali e offrire un approccio a doppio binario — colpire il batterio e calmare la risposta dell’ospite — particolarmente prezioso contro infezioni multiresistenti difficili da trattare.
Citazione: Yeh, JC., Hazam, P.K., Lin, YY. et al. Antimicrobial peptide-induced inner membrane hyperpolarization is associated with antibiotic sensitization and attenuated MIC escalation in multidrug-resistant Gram-negative pathogens. npj Antimicrob Resist 4, 33 (2026). https://doi.org/10.1038/s44259-026-00210-x
Parole chiave: peptidi antimicrobici, adiuvanti per antibiotici, batteri multiresistenti, sepsi, infezioni Gram‑negative